Hydrid hlinitý - Aluminium hydride

|
|
| Jména | |
|---|---|
|
Preferovaný název IUPAC
Hydrid hlinitý |
|
|
Systematický název IUPAC
Aluman |
|
| Ostatní jména
Alane
Hydrid |
|
| Identifikátory | |
|
3D model ( JSmol )
|
|
| ČEBI | |
| ChemSpider | |
| Informační karta ECHA |
100,029,139 |
| 245 | |
|
PubChem CID
|
|
| UNII | |
|
CompTox Dashboard ( EPA )
|
|
|
|
|
|
| Vlastnosti | |
| AlH 3 | |
| Molární hmotnost | 29,99 g/mol |
| Vzhled | bílé krystalické pevné, netěkavé, vysoce polymerizované, jehlicovité krystaly |
| Hustota | 1,477 g / cm 3 , pevný |
| Bod tání | 150 ° C (302 ° F; 423 K) se začíná rozkládat při 105 ° C (221 ° F) |
| reaguje | |
| Rozpustnost | rozpustný v etheru reaguje v ethanolu |
| Termochemie | |
|
Tepelná kapacita ( C )
|
40,2 J/mol K |
|
Standardní molární
entropie ( S |
30 J/mol K |
|
Standardní entalpie
tvorby (Δ f H ⦵ 298 ) |
-11,4 kJ/mol |
|
Gibbsova volná energie (Δ f G ˚)
|
46,4 kJ/mol |
| Související sloučeniny | |
|
Související sloučeniny
|
Lithiumaluminiumhydrid , diboran |
|
Pokud není uvedeno jinak, jsou údaje uvedeny pro materiály ve standardním stavu (při 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Reference na infobox | |
Aluminium hydrid (také známý jako alanu nebo alumane) je anorganická sloučenina se vzorcem Al H 3 . Je ve formě bílé pevné látky a může být zabarvený šedě s klesající velikostí částic a úrovněmi nečistot. V závislosti na podmínkách syntézy může být povrch alanu pasivován tenkou vrstvou oxidu hlinitého a/nebo hydroxidu. Alane a jeho deriváty se používají jako redukční činidla v organické syntéze .
Struktura
Alane je polymer. Z tohoto důvodu, jeho vzorec je někdy reprezentována vzorcem (ALH 3 ) n . Alane tvoří četné polymorfy , které jsou pojmenovány α-alane, α'-alane, β-alane, γ-alane, δ-alane, ε-alane a ζ-alane. α-Alane má kubickou nebo romboedrickou morfologii, zatímco α'-alane tvoří jehlicovité krystaly a γ-alane tvoří svazek roztavených jehel. Alane je rozpustný v tetrahydrofuranu (THF) a etheru. Rychlost srážení pevného alanu z etheru se mění podle způsobu přípravy.
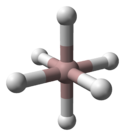
Krystalová struktura α-alanu byla stanovena a obsahuje atomy hliníku obklopené 6 atomy vodíku, které překlenují 6 dalších atomů hliníku. Vzdálenosti Al-H jsou ekvivalentní (172 pm) a úhel Al-H-Al je 141 °.
 |
 |

|
| buňka jednotky α-AlH 3 | Al koordinace | H koordinace |
α-Alane je tepelně nejstabilnější polymorf. P-alan a y-alan se vyrábějí společně a po zahřátí se převádějí na α-alan. δ, ε a θ-alan se vyrábějí za ještě jiných krystalizačních podmínek. Přestože jsou polymorfy δ, ε a θ po zahřátí méně tepelně stabilní.
Molekulární formy alane
Monomerní AlH 3 byl izolován při nízké teplotě v pevné vzácného plynu matrici a prokázáno, že je rovinná. Dimer Al 2 H 6 byl izolován v pevném vodíku. Je isostrukturální s diboranem (B 2 H 6 ) a digallanem (Ga 2 H 6 ).
Příprava
Hydridy hliníku a jejich různé komplexy jsou již dlouho známy. Jeho první syntéza byla publikována v roce 1947 a patent na syntézu byl přidělen v roce 1999. Aluminiumhydrid se připravuje zpracováním lithiumaluminiumhydridu s chloridem hlinitým . Postup je složitý: pozornost musí být věnována odstraňování chloridu lithného .
- 3 LiAlH 4 + AlCl 3 → 4 AlH 3 + 3 LiCl
Etherový roztok alanu vyžaduje okamžité použití, protože polymerní materiál se rychle vysráží jako pevná látka. Je známo, že roztoky hydridu hlinitého degradují po 3 dnech. Aluminiumhydrid je reaktivnější než LiAlH 4 .
Pro přípravu hydridu hlinitého existuje několik dalších metod:
- 2 LiAlH 4 + BeCl 2 → 2 AlH 3 + Li 2 BeH 2 Cl 2
- 2 LiAlH 4 + H 2 SO 4 → 2 AlH 3 + Li 2 SO 4 + 2 H 2
- 2 LiAlH 4 + ZnCl 2 → 2 AlH 3 + 2 LiCl + ZnH 2
- 2 LiAlH 4 + I 2 → 2 AlH 3 + 2 LiI + H 2
Elektrochemická syntéza
Několik skupin ukázalo, že alane lze vyrábět elektrochemicky . Byly patentovány různé způsoby výroby elektrochemických alanů. Elektrochemicky generující alan se vyhýbá chloridovým nečistotám. Jsou diskutovány dva možné mechanismy pro tvorbu alanu v Clasenově elektrochemickém článku obsahujícím THF jako rozpouštědlo, hydrid hlinito -sodný jako elektrolyt, hliníkovou anodu a železný (Fe) drát ponořený do rtuti (Hg) jako katoda. Sodík tvoří amalgám s katodou Hg, která brání vedlejším reakcím, a vodík vyrobený v první reakci by mohl být zachycen a zreagován zpět s amalgámem rtuti sodné za vzniku hydridu sodného. Clasenův systém nemá za následek ztrátu výchozího materiálu. U nerozpustných anod dochází k reakci 1, zatímco u rozpustných anod se očekává anodické rozpouštění podle reakce 2:
- AlH 4 - - e - → AlH 3 · nTHF + 1 / 2 H 2
- 3AlH 4 - + Al - 3e - → 4AlH 3 · nTHF
V reakci 2 je anoda hliníku spotřebována, což omezuje produkci hydridu hlinitého pro daný elektrochemický článek.
Byla prokázána krystalizace a regenerace hydridu hlinitého z elektrochemicky generovaného alanu.
Vysokotlaká hydrogenace kovového hliníku
α-AlH 3 lze vyrobit hydrogenací kovového hliníku v 10GPa a 600 ° C (1112 ° F). Reakce mezi zkapalněného vodíku vytváří α-ALH 3 , které by mohly být vrácena za podmínek okolního prostředí.
Reakce
Tvorba aduktů s Lewisovými bázemi
AlH 3 snadno tvoří adukty se silnými Lewisovými bázemi . S trimethylaminem se například tvoří komplexy 1: 1 i 1: 2 . Komplex 1: 1 je v plynné fázi čtyřboký, ale v pevné fázi je dimerní s přemosťujícími vodíkovými centry (NMe 3 Al (μ-H)) 2 . Komplex 1: 2 má trigonální bipyramidovou strukturu . Některé adukty (např. Dimethylethylamin alan, NMe 2 Et · AlH 3 ) se tepelně rozkládají za vzniku kovového hliníku a mohou být použity v aplikacích MOCVD .
Jeho komplex s diethyletherem se tvoří podle následující stechiometrie:
- AlH 3 + (C 2 H 5 ) 2 O → H 3 AI · O (C 2 H 5 ) 2
Reakce s hydridem lithným v etheru vytváří lithiumaluminiumhydrid :
- AlH 3 + LiH → LiAlH 4
Redukce funkčních skupin
V organické chemii se k redukci funkčních skupin používá hlavně hydrid hlinitý. Reaktivita hydridu hlinitého je v mnoha ohledech podobná reaktivitě lithiumaluminiumhydridu . Aluminiumhydrid sníží aldehydy , ketony , karboxylové kyseliny , anhydridy , chloridy kyselin , estery a laktony na odpovídající alkoholy . Amidy , nitrily a oximy jsou redukovány na odpovídající aminy .
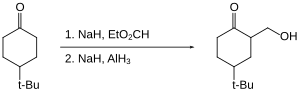
Pokud jde o selektivitu funkční skupiny, alane se liší od ostatních hydridových činidel. Například v následující redukci cyklohexanonu poskytuje lithiumaluminiumhydrid poměr trans: cis 1,9: 1, zatímco hydrid hlinitý poskytuje poměr trans: cis 7,3: 1.
Alan umožňuje hydroxymethylací určitých ketonů (to je nahrazení CH C-CH 2 OH v poloze alfa ). Samotný keton není redukován, protože je „chráněn“ jako svůj enolát.
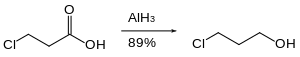
Organohalidy se redukují pomalu nebo vůbec ne hydridem hlinitým. Reaktivní funkční skupiny, jako jsou karboxylové kyseliny, lze proto redukovat v přítomnosti halogenidů.
Nitroskupiny nejsou redukovány hydridem hlinitým. Podobně může hydrid hlinitý dosáhnout redukce esteru v přítomnosti nitroskupin.
Při redukci acetálů na polovinu chráněných diolů lze použít hydrid hlinitý.
Hydrid hlinitý může být také použit v reakci na otevření epoxidového kruhu, jak je uvedeno níže.
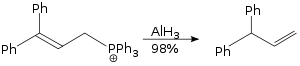
Allylová přesmyková reakce prováděná za použití hydridu hlinitého je reakce S N 2 a není stericky náročná.
Hydrid hliníku při zahřívání dokonce redukuje oxid uhličitý na metan :
- 4 AlH 3 + 3 CO 2 → 3 CH 4 + 2 Al 2 O 3
Hydroaluminace
Bylo ukázáno, že hydrid hlinitý se přidává k propargylovým alkoholům . Při použití společně s chloridem titaničitým může hydrid hlinitý přidat dvojné vazby . Hydroborace je podobná reakce.
Pohonné hmoty
Ve své pasivované formě je Alane aktivním kandidátem na skladování vodíku a lze jej použít k efektivní výrobě energie prostřednictvím aplikací palivových článků, včetně palivových článků a elektrických vozidel a dalších lehkých energetických aplikací. AlH 3 obsahuje až 10% hmotnostních vodíku, což odpovídá 148 g H 2 / l, nebo dvakrát hustotu vodíku kapalného H 2 . Ve své neaktivované podobě je alane také slibnou přísadou do raketových paliv , schopnou zajistit zvýšení impulzní účinnosti až o 10%.
Opatření
Alane není spontánně hořlavý. Mělo by se s ním zacházet podobně jako s jinými komplexními redukčními činidly na bázi kovových hydridů, jako je lithiumaluminiumhydrid. Alane se bude rozkládat ve vzduchu a ve vodě, ačkoli pasivace výrazně snižuje rychlost rozkladu. Pasivovanému alane je obecně přiřazena klasifikace nebezpečnosti 4,3 (chemikálie, které při styku s vodou uvolňují hořlavé plyny).
Reference
externí odkazy
- Hydrid hlinitý v chemické databázi EnvironmentalChemistry.com
- Skladování vodíku z Brookhaven National Laboratory
- Hliníkový trihydride na WebElements