Trisulfid antimonu - Antimony trisulfide
|
|

|
|
| Jména | |
|---|---|
|
Název IUPAC
disulfid diantimonitý, sulfid antimonitý (III)
|
|
| Ostatní jména
sulfid antimonitý, sulfid antimonní, seskvirid antimonitý, vermilion antimonu, černý antimon, sulfuretan antimonu
|
|
| Identifikátory | |
|
3D model ( JSmol )
|
|
| ChemSpider | |
| Informační karta ECHA |
100,014,285 |
|
PubChem CID
|
|
| UNII | |
|
CompTox Dashboard ( EPA )
|
|
|
|
|
|
| Vlastnosti | |
| Sb 2 S 3 | |
| Molární hmotnost | 339,715 |
| Vzhled | šedý / černý ortorombický krystal (stibnite) |
| Hustota | 4,562 g cm −3 (stibnite) |
| Bod tání | 550 ° C (1022 ° F; 823 K) (stibnit) |
| Bod varu | 1150 ° C (2100 ° F; 1420 K) |
| 0,00017 g/100 ml (18 ° C) | |
| -86,0 · 10 −6 cm 3 /mol | |
|
Index lomu ( n D )
|
4,046 |
| Termochemie | |
|
Tepelná kapacita ( C )
|
123,32 J/K mol |
|
Standardní entalpie
tvorby (Δ f H ⦵ 298 ) |
-157,8 kJ/mol |
| Nebezpečí | |
| NFPA 704 (ohnivý diamant) | |
| Smrtelná dávka nebo koncentrace (LD, LC): | |
|
LD 50 ( střední dávka )
|
> 2000 mg/kg (krysa, orální) |
| NIOSH (limity expozice USA pro zdraví): | |
|
PEL (přípustné)
|
PEL 0,5 mg/m 3 (jako Sb) |
|
REL (doporučeno)
|
PEL 0,5 mg/m 3 (jako Sb) |
| Související sloučeniny | |
|
Jiné anionty
|
Oxid antimonitý Triselenid antimonu Telurid antimonu |
|
Jiné kationty
|
Trisulfid arsenitý Sulfid bizmutu (III) |
|
Související sloučeniny
|
Pentasulfid antimonu |
|
Pokud není uvedeno jinak, jsou údaje uvedeny pro materiály ve standardním stavu (při 25 ° C [77 ° F], 100 kPa). |
|
| Reference na infobox | |
Trisulfid antimonu (Sb 2 S 3 ) se v přírodě vyskytuje jako krystalický minerál stibnit a amorfní červený minerál (vlastně mineraloid) metastibnit . Je vyroben pro použití v bezpečnostních zápasech , vojenské munici, výbušninách a ohňostrojích. Používá se také při výrobě rubínově zbarveného skla a v plastech jako zpomalovač hoření. Historicky byla stibnitová forma používána jako šedý pigment v obrazech vyrobených v 16. století. Sulfid antimonitý byl také použit jako fotovodič citlivý na obraz v tubách kamer vidicon . Jedná se o polovodič s přímou mezerou v pásmu 1,8–2,5 eV. Vhodným dopingem lze vyrábět materiály typu p a n .
Příprava a reakce
Sb 2 S 3 lze připravit z prvků při teplotě 500–900 ° C:
- 2 Sb + 3 S → Sb 2 S 3
Sb 2 S 3 se vysráží při H 2 S prochází okyseleného roztoku Sb (III). Tato reakce byla použita jako gravimetrickou metodou pro stanovení antimonu, probublávání H 2 S pomocí roztoku Sb (III) sloučeniny v teplé HCl vkladů oranžové forma Sb 2 S 3, který zčerná za reakčních podmínek.
Sb 2 S 3 se snadno oxiduje, přičemž prudce reaguje s oxidačními činidly. Hoří na vzduchu modrým plamenem. Reaguje žhavením s kadmiem, chlorečnany a zinečnatými chlorečnany. Směsi Sb 2 S 3 a chlorečnany mohou explodovat.
Při extrakci antimonu z antimonových rud se používá alkalický sulfidový proces, kde Sb 2 S 3 reaguje za vzniku solí thioantimonátu (III) (také nazývaného thioantimonit):
- 3 Na 2 S + Sb 2 S 3 → 2 Na 3 SbS 3
Množství soli, které obsahují jiný thioantimonate (III) ionty mohou být připraveny z Sb 2 S 3, mezi ně patří:
- [SbS 3 ] 3− , [SbS 2 ] - , [Sb 2 S 5 ] 4− , [Sb 4 S 9 ] 6− , [Sb 4 S 7 ] 2− a [Sb 8 S 17 ] 10−
„ Schlippeova sůl “, Na 3 SbS 4 · 9H 2 O, thioantimonátová (V) sůl vzniká, když se Sb 2 S 3 vaří se sírou a hydroxidem sodným. Reakci lze znázornit jako:
- Sb 2 S 3 + 3 S 2− + 2 S → 2 [SbS 4 ] 3−
Struktura
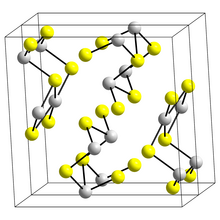
Struktura černé jehlicovité formy Sb 2 S 3 , stibnite , se skládá ze spojených stuh, ve kterých jsou atomy antimonu ve dvou různých koordinačních prostředích, trigonálním pyramidálním a čtvercovém pyramidálním. Podobné stuhy se vyskytují v Bi 2 S 3 a Sb 2 Se 3 . Červená forma, metastibnite, je amorfní. Nedávná práce naznačuje, že existuje řada teplotně závislých struktur stibnitu, které byly nazvány stibnite (I) vysokoteplotní forma, dříve identifikovaný, stibnite (II) a stibnite (III). Jiný článek ukazuje, že skutečné koordinační mnohostěny antimonu jsou ve skutečnosti SbS 7 , s (3+4) koordinací v místě M1 a (5+2) v místě M2. Tyto koordinace zvažují přítomnost sekundárních vazeb. Některé ze sekundárních vazeb dodávají soudržnost a jsou spojeny s balením.

