Baryum - Barium
 | ||||||||||||||||||||||||||||||||||||||||||||||
| Baryum | ||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Výslovnost |
/ B ɛər i ə m / ( BAIR -EE-əm ) |
|||||||||||||||||||||||||||||||||||||||||||||
| Vzhled | stříbřitě šedá; s bledě žlutým odstínem | |||||||||||||||||||||||||||||||||||||||||||||
| Standardní atomová hmotnost A r, std (Ba) | 137,327 (7) | |||||||||||||||||||||||||||||||||||||||||||||
| Barium v periodické tabulce | ||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||
| Atomové číslo ( Z ) | 56 | |||||||||||||||||||||||||||||||||||||||||||||
| Skupina | skupina 2 (kovy alkalických zemin) | |||||||||||||||||||||||||||||||||||||||||||||
| Doba | období 6 | |||||||||||||||||||||||||||||||||||||||||||||
| Blok | s-blok | |||||||||||||||||||||||||||||||||||||||||||||
| Konfigurace elektronů | [ Xe ] 6s 2 | |||||||||||||||||||||||||||||||||||||||||||||
| Elektrony na skořápku | 2, 8, 18, 18, 8, 2 | |||||||||||||||||||||||||||||||||||||||||||||
| Fyzikální vlastnosti | ||||||||||||||||||||||||||||||||||||||||||||||
| Fáze na STP | pevný | |||||||||||||||||||||||||||||||||||||||||||||
| Bod tání | 1000 K (727 ° C, 1341 ° F) | |||||||||||||||||||||||||||||||||||||||||||||
| Bod varu | 2118 K (1845 ° C, 3353 ° F) | |||||||||||||||||||||||||||||||||||||||||||||
| Hustota (blízko rt ) | 3,51 g / cm 3 | |||||||||||||||||||||||||||||||||||||||||||||
| při kapalině (při mp ) | 3,338 g / cm 3 | |||||||||||||||||||||||||||||||||||||||||||||
| Teplo fúze | 7,12 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||
| Teplo odpařování | 142 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||
| Molární tepelná kapacita | 28,07 J/(mol · K) | |||||||||||||||||||||||||||||||||||||||||||||
Tlak páry
| ||||||||||||||||||||||||||||||||||||||||||||||
| Atomové vlastnosti | ||||||||||||||||||||||||||||||||||||||||||||||
| Oxidační stavy | +1, +2 (silně zásaditý oxid) | |||||||||||||||||||||||||||||||||||||||||||||
| Elektronegativita | Paulingova stupnice: 0,89 | |||||||||||||||||||||||||||||||||||||||||||||
| Ionizační energie | ||||||||||||||||||||||||||||||||||||||||||||||
| Atomový poloměr | empirické: 222 hod | |||||||||||||||||||||||||||||||||||||||||||||
| Kovalentní poloměr | 215 ± 23 hodin | |||||||||||||||||||||||||||||||||||||||||||||
| Van der Waalsův poloměr | 268 hod | |||||||||||||||||||||||||||||||||||||||||||||
| Spektrální linie barya | ||||||||||||||||||||||||||||||||||||||||||||||
| Další vlastnosti | ||||||||||||||||||||||||||||||||||||||||||||||
| Přirozený výskyt | prvotní | |||||||||||||||||||||||||||||||||||||||||||||
| Krystalická struktura | tělo-krychlový (BCC) | |||||||||||||||||||||||||||||||||||||||||||||
| Rychlost zvuku tenký prut | 1620 m/s (při 20 ° C) | |||||||||||||||||||||||||||||||||||||||||||||
| Teplotní roztažnost | 20,6 µm/(m⋅K) (při 25 ° C) | |||||||||||||||||||||||||||||||||||||||||||||
| Tepelná vodivost | 18,4 W/(m⋅K) | |||||||||||||||||||||||||||||||||||||||||||||
| Elektrický odpor | 332 nΩ⋅m (při 20 ° C) | |||||||||||||||||||||||||||||||||||||||||||||
| Magnetické uspořádání | paramagnetický | |||||||||||||||||||||||||||||||||||||||||||||
| Molární magnetická citlivost | +20,6 × 10 −6 cm 3 /mol | |||||||||||||||||||||||||||||||||||||||||||||
| Youngův modul | 13 GPa | |||||||||||||||||||||||||||||||||||||||||||||
| Tažný modul | 4,9 GPa | |||||||||||||||||||||||||||||||||||||||||||||
| Hromadný modul | 9,6 GPa | |||||||||||||||||||||||||||||||||||||||||||||
| Mohsova tvrdost | 1,25 | |||||||||||||||||||||||||||||||||||||||||||||
| Číslo CAS | 7440-39-3 | |||||||||||||||||||||||||||||||||||||||||||||
| Dějiny | ||||||||||||||||||||||||||||||||||||||||||||||
| Objev | Carl Wilhelm Scheele (1772) | |||||||||||||||||||||||||||||||||||||||||||||
| První izolace | Humphry Davy (1808) | |||||||||||||||||||||||||||||||||||||||||||||
| Hlavní izotopy barya | ||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||
Barium je chemický prvek se symbolem Ba a atomovým číslem 56. Je pátým prvkem ve skupině 2 a je měkkým, stříbrným kovem alkalické zeminy . Kvůli své vysoké chemické reaktivitě se baryum v přírodě nikdy nenachází jako volný prvek.
Nejčastějšími minerály barya jsou baryt ( síran barnatý , BaSO 4 ) a witherit ( uhličitan barnatý , BaCO 3 ). Název barium pochází z alchymistického derivátu „baryta“, z řeckého βαρὺς ( barys ), což znamená „těžký“. Baric je adjektivní forma barya. Barium bylo identifikováno jako nový prvek v roce 1774, ale nebylo redukováno na kov až do roku 1808 s příchodem elektrolýzy .
Barium má málo průmyslových aplikací. Historicky byl používán jako getr pro vakuové trubice a v oxidové formě jako emisní povlak na nepřímo ohřívaných katodách . Je součástí YBCO ( vysokoteplotních supravodičů ) a elektrokeramiky a přidává se do oceli a litiny, aby se zmenšila velikost uhlíkových zrn v mikrostruktuře. Sloučeniny barya se přidávají do ohňostrojů, aby získaly zelenou barvu. Síran barnatý se používá jako nerozpustná přísada do kapaliny pro vrtání ropných vrtů , stejně jako v čistší formě, jako rentgenová radiokontrastní činidla pro zobrazování lidského gastrointestinálního traktu. Ve vodě rozpustné sloučeniny barya jsou jedovaté a používají se jako rodenticidy .
Charakteristika
Fyzikální vlastnosti
Barium je měkký, stříbřitě bílý kov, který má v ultračistém odstínu zlatavý odstín. Stříbřitě bílá barva barya rychle mizí po oxidaci na vzduchu za vzniku tmavě šedé vrstvy obsahující oxid . Baryum má střední měrnou hmotnost a vysokou elektrickou vodivost. Protože se baryum čistí obtížně, mnoho jeho vlastností nebylo přesně stanoveno.
Při pokojové teplotě a tlaku, kovové baryum přijímá kubické tělo- strukturu, s barnatý barnatého vzdálenosti 503 pikometrů , rozšiřuje se zahříváním rychlostí přibližně 1,8 x 10 - 5 / ° C. Jedná se o velmi měkký kov s Mohsovou tvrdostí 1,25. Jeho teploty tání 1 000 K (730 ° C; 1 340 ° F) jsou mezi teplotami lehčího stroncia (1 050 K nebo 780 ° C nebo 1 430 ° F) a těžšího radia (973 K nebo 700 ° C nebo 1292 ° F) ; jeho teplota varu 2 170 K (1 900 ° C; 3 450 ° F) však převyšuje teplotu varu stroncia (1 655 K nebo 1 382 ° C nebo 2 519 ° F). Hustota (3,62 g / cm 3 ) je opět mezi vlastnostmi stroncia (2,36 g / cm 3 ) a radium (≈5 g / cm 3 ).
Chemická reaktivita
Barium je chemicky podobné hořčíku, vápníku a stronciu, ale je ještě reaktivnější. Vždy vykazuje oxidační stav +2. Většina výjimek je v několika vzácných a nestabilních molekulárních druzích, které jsou charakterizovány pouze v plynné fázi, jako je BaF, ale v poslední době byl v interkalační sloučenině grafitu popsán druh barya (I). Reakce s chalkogeny jsou vysoce exotermické (uvolňování energie); reakce s kyslíkem nebo vzduchem probíhá při pokojové teplotě. Z tohoto důvodu je kovové baryum často skladováno pod olejem nebo v inertní atmosféře. Reakce s jinými nekovy , jako je uhlík, dusík, fosfor, křemík a vodík, jsou obecně exotermické a probíhají po zahřátí. Reakce s vodou a alkoholy jsou velmi exotermické a uvolňují plynný vodík:
- Ba + 2 ROH → Ba (OR) 2 + H 2 ↑ (R je alkylová skupina nebo atom vodíku)
Barya reaguje s amoniakem za vzniku komplexů, jako je například Ba (NH 3 ) 6 .
Kov je snadno napaden kyselinami. Kyselina sírová je významnou výjimkou, protože pasivace zastaví reakci vytvořením nerozpustného síranu barnatého na povrchu. Barium se spojuje s několika dalšími kovy, včetně hliníku , zinku , olova a cínu , za vzniku intermetalických fází a slitin.
Sloučeniny
|
Ó2− |
S2− |
F- |
Cl- |
TAK2- 4 |
CO2- 3 |
Ó2- 2 |
H- |
|
|---|---|---|---|---|---|---|---|---|
|
Ca2+ |
3,34 | 2,59 | 3.18 | 2.15 | 2,96 | 2,83 | 2.9 | 1.7 |
|
Sr2+ |
5.1 | 3.7 | 4.24 | 3,05 | 3,96 | 3.5 | 4,78 | 3.26 |
|
Ba2+ |
5,72 | 4.3 | 4,89 | 3,89 | 4,49 | 4.29 | 4,96 | 4.16 |
|
Zn2+ |
5.6 | 4,09 | 4,95 | 2,09 | 3,54 | 4.4 | 1,57 | - |
Soli barya jsou typicky bílé, když jsou pevné, a bezbarvé, když jsou rozpuštěny. Jsou hutnější než stroncium nebo analogy vápníku , kromě halogenidů (viz tabulka; pro srovnání je uveden zinek ).
Hydroxid barnatý („baryta“) byl znám alchymistům, kteří jej vyráběli zahříváním uhličitanu barnatého. Na rozdíl od hydroxidu vápenatého absorbuje velmi málo CO 2 ve vodných roztocích, a proto je necitlivý na atmosférické výkyvy. Tato vlastnost se používá při kalibraci pH zařízení.
Těkavé sloučeniny barya hoří zeleným až světle zeleným plamenem , což je účinný test k detekci sloučeniny barya. Barva pochází ze spektrálních čar při 455,4, 493,4, 553,6 a 611,1 nm.
Organobariové sloučeniny jsou rostoucí oblastí znalostí: nedávno byly objeveny dialkylbaria a alkylhalobaria.
Izotopy
Baryum nalezené v zemské kůře je směsí sedmi prvotních nuklidů , barya-130, 132 a 134 až 138. Barium-130 podléhá velmi pomalému radioaktivnímu rozpadu na xenon -130 dvojitým beta plus rozpadem , s poločasem rozpadu ( 0.5-2.7) × 10 21 let (v asi 10 11 krát větší než věk vesmíru). Jeho nadbytek je ≈0,1% přirozeného barya. Teoreticky může baryum-132 podobně podléhat dvojitému beta rozpadu jako xenon-132; tento rozpad nebyl detekován. Radioaktivita těchto izotopů je tak slabá, že nepředstavují žádné ohrožení života.
Ze stabilních izotopů baryum-138 tvoří 71,7% veškerého barya; ostatní izotopy mají klesající početnost s klesajícím hmotnostním číslem .
Celkem má barium asi 40 známých izotopů, jejichž hmotnost se pohybuje mezi 114 a 153. Nejstabilnějším umělým radioizotopem je barium-133 s poločasem rozpadu přibližně 10,51 roku. Pět dalších izotopů má poločasy delší než jeden den. Barium má také 10 meta států , z nichž je barium-133m1 nejstabilnější s poločasem rozpadu přibližně 39 hodin.
Dějiny

Alchymisté v raném středověku věděli o některých minerálech barya. Hladký oblázek, jako kameny minerální barytu byly nalezeny v sopečné skále poblíž Bologna , Itálie , a proto byl nazýván „Bologna kameny“. Alchymisty k nim přitahovalo, protože po vystavení světlu by svítily roky. Fosforeskující vlastnosti barytu zahřívaného organickými látkami popsal V. Casciorolus v roce 1602.
Carl Scheele zjistil, že baryt obsahuje nový prvek v roce 1774, ale nemohl izolovat baryum, pouze oxid barnatý . Johan Gottlieb Gahn také izoloval oxid barnatý o dva roky později v podobných studiích. Guyton de Morveau nazýval oxidované baryo nejprve „barote“ , jméno, které Antoine Lavoisier změnil na baryta . Také v 18. století zaznamenal anglický mineralog William Withering těžký minerál v olověných dolech v Cumberlandu , nyní známém jako vadnoucí . Barium bylo poprvé izolováno elektrolýzou roztavených barnatých solí v roce 1808 sirem Humphrym Davym v Anglii . Davy, analogicky s vápníkem , pojmenovaný „baryum“ podle baryty, přičemž konec „-ium“ znamenal kovový prvek. Robert Bunsen a Augustus Matthiessen získali čisté baryum elektrolýzou roztavené směsi chloridu barnatého a chloridu amonného .
Výroba čistého kyslíku v procesu Brin byla rozsáhlá aplikace peroxidu barnatého v 80. letech 19. století, než byla na počátku 20. století nahrazena elektrolýzou a frakční destilací zkapalněného vzduchu. V tomto procesu oxid barnatý reaguje při 500–600 ° C (932–1, 112 ° F) se vzduchem za vzniku peroxidu barnatého, který se rozkládá nad 700 ° C (1292 ° F) uvolňováním kyslíku:
- 2 BaO + O 2 ⇌ 2 BaO 2
Síran barnatý byl poprvé použit jako radiokontrastní činidlo při rentgenovém zobrazování trávicího systému v roce 1908.
Výskyt a produkce
Množství barya je 0,0425% v zemské kůře a 13 μg/l v mořské vodě. Primárním komerčním zdrojem barya je baryt (také nazývaný baryty nebo těžký nosník), minerál síranu barnatého. s vklady v mnoha částech světa. Dalším komerčním zdrojem, mnohem méně důležitým než baryt, je iserit, uhličitan barnatý. Hlavní ložiska se nacházejí v Británii, Rumunsku a bývalém SSSR.
Zásoby barytů se odhadují mezi 0,7 a 2 miliardami tun . Maximální produkce, 8,3 milionu tun, byla vyrobena v roce 1981, ale pouze 7–8% bylo použito na kov nebo sloučeniny baria. Produkce barytu od druhé poloviny 90. let vzrostla z 5,6 milionu tun v roce 1996 na 7,6 v roce 2005 a 7,8 v roce 2011. Na této produkci se podílí více než 50% Čína, následovaná Indií (14% v roce 2011), Marokem (8,3 %), USA (8,2%), Turecko (2,5%), Írán a Kazachstán (po 2,6%).
Vytěžená ruda se promyje, rozdrtí, roztřídí a oddělí se od křemene. Pokud křemen proniká příliš hluboko do rudy nebo je obsah železa, zinku nebo olova abnormálně vysoký, použije se pěnová flotace . Produktem je 98% čistý baryt (hmotnostně); čistota by neměla být menší než 95%, s minimálním obsahem železa a oxidu křemičitého . Poté se redukuje uhlíkem na sulfid barnatý :
- BaSO 4 + 2 C → BaS + 2 CO 2
Ve vodě rozpustný sirník barnatý je výchozím bodem pro další sloučeniny: reakcí BaS s kyslíkem vzniká síran, s kyselinou dusičnou dusičnanem, s vodným oxidem uhličitým a uhličitanem atd. Dusičnan lze tepelně rozložit za vzniku oxidu. Kov barya se vyrábí redukcí hliníkem při 1 100 ° C (2 010 ° F). Intermetalické sloučeniny Baal 4 se vyrábí první:
- 3 BaO + 14 Al → 3 BaAl 4 + Al 2 O 3
BaAl 4 je meziprodukt reagující s oxidem barnatým za vzniku kovu. Všimněte si, že ne všechny barya jsou redukovány.
- 8 BaO + BaAl 4 → Ba ↓ + 7 BaAl 2 O 4
Zbývající oxid barnatý reaguje s vytvořeným oxidem hlinitým:
- BaO + Al 2 O 3 → BaAl 2 O 4
a celková reakce je
- 4 BaO + 2 Al → 3 Ba ↓ + BaAl 2 O 4
Pary barya se kondenzují a balí do forem v atmosféře argonu. Tato metoda se používá komerčně a poskytuje ultračisté baryum. Běžně prodávaný barium má čistotu asi 99%, přičemž hlavními nečistotami je stroncium a vápník (až 0,8% a 0,25%) a další kontaminující látky přispívají méně než 0,1%.
Podobná reakce s křemíkem při 1200 ° C (2190 ° F) poskytne metakřemičitan barnatý a barnatý . Elektrolýza se nepoužívá, protože baryum se snadno rozpouští v roztavených halogenidech a produkt je poměrně nečistý.

Drahokam
Minerál barya, benitoit (křemičitan barya a titanu), se vyskytuje jako velmi vzácný modrý fluorescenční drahokam a je oficiálním státním klenotem Kalifornie .
Baryum v mořské vodě
Baryum existuje v mořské vodě jako iont Ba 2+ s průměrnou oceánskou koncentrací 109 nmol/kg. Baryum také existuje v oceánu jako BaSO 4 nebo baryt. Barium má profil podobný živinám s dobou pobytu 10 000 let.
Baryum vykazuje relativně konzistentní koncentraci v mořské vodě v horních oceánech, s výjimkou oblastí s vysokými přítoky řek a oblastí se silným vzestupem. V horním oceánu dochází k malému vyčerpání koncentrací barya pro ionty s profilem podobným živinám, takže je důležité boční míchání. Izotopické hodnoty barya ukazují zůstatky v povodí namísto lokálních nebo krátkodobých procesů.
Aplikace
Kov a slitiny
Barium, jako kov, nebo když je legováno hliníkem, se používá k odstranění nežádoucích plynů ( getrů ) z elektronek, jako jsou televizní obrazovky. Barium je pro tento účel vhodné kvůli svému nízkému tlaku par a reaktivitě vůči kyslíku, dusíku, oxidu uhličitému a vodě; může dokonce částečně odstranit vzácné plyny jejich rozpuštěním v krystalové mřížce. Tato aplikace postupně mizí kvůli rostoucí popularitě bezdušových LCD a plazmových sad.
Další použití elementárního barya jsou malá a zahrnují přísadu do siluminu (slitiny hliníku a křemíku), která vylepšuje jejich strukturu, stejně jako
- ložiskové slitiny ;
- slitiny pájení olovo - cín - ke zvýšení odolnosti proti tečení;
- slitina s niklem pro zapalovací svíčky ;
- přísada do oceli a litiny jako očkovací látka;
- slitiny s vápníkem, manganem, křemíkem a hliníkem jako vysoce kvalitní deoxidátory oceli.
Síran barnatý a baryt
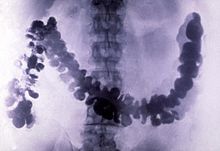
Síran barnatý (minerální baryt, BaSO 4 ) je důležitý pro ropný průmysl jako vrtná kapalina v ropných a plynových vrtech . Sraženina sloučeniny (nazývaná „blanc fixe“, z francouzštiny „stálá bílá“) se používá v barvách a lacích; jako plnivo do vyzváněcího inkoustu, plastů a kaučuků; jako pigment pro potahování papíru; a v nanočásticích ke zlepšení fyzikálních vlastností některých polymerů, jako jsou epoxidy.
Síran barnatý má nízkou toxicitu a relativně vysokou hustotu cca. 4,5 g/cm 3 (a tedy opacita k rentgenovým paprskům). Z tohoto důvodu se používá jako radiokontrastní činidlo při rentgenovém zobrazování trávicího systému („ baryová jídla “ a „ baryové klystýry “). Lithopone , pigment, který obsahuje síran barnatý a sulfid zinečnatý , je trvale bílý s dobrou krycí schopností, který při působení sulfidů neztmavne.
Jiné sloučeniny baria
Jiné sloučeniny baria nacházejí pouze specializované aplikace, omezené toxicitou iontů Ba 2+ (uhličitan barnatý je jed na krysy ), což pro nerozpustný BaSO 4 není problém .
- Barnatý oxidu povlak na elektrodách v zářivkách usnadňuje uvolňování elektronů .
- Uhličitan barnatý díky své velké atomové hustotě zvyšuje index lomu a lesk skla a snižuje únik rentgenových paprsků z televizorů s katodovými trubicemi (CRT).
- Barium, typicky jako dusičnan barnatý, dodává ohňostrojům žlutou nebo „jablkovou“ zelenou barvu; pro brilantní zelenou se používá monochlorid barnatý.
- Peroxid barnatý je katalyzátorem v aluminotermické reakci ( termit ) pro svařování kolejových drah. Je to také zelená světlice ve stopovací munici a bělícím prostředku.
- Titaničitan barnatý je slibný elektrokeramik .
- Fluorid barnatý se používá pro optiku v infračervených aplikacích, protože má široký rozsah průhlednosti 0,15–12 mikrometrů.
- YBCO byl první vysokoteplotní supravodič chlazený kapalným dusíkem, s přechodovou teplotou 93 K (-180,2 ° C; -292,3 ° F), která překročila bod varu dusíku (77 K nebo -196,2 ° C nebo -321,1 ° F).
- Ferit , druh slinuté keramiky složené z oxidu železa (Fe 2 O 3 ) a oxidu barnatého (BaO), je elektricky nevodivý i ferimagnetický a může být dočasně nebo trvale magnetizován.
Paleoceanografie
Boční míchání barya je způsobeno mícháním vodní hmoty a oceánskou cirkulací. Globální oceánská cirkulace odhaluje silnou korelaci mezi rozpuštěným baryem a kyselinou křemičitou. Velký oceánský oběh v kombinaci s remineralizací barya vykazuje podobnou korelaci mezi rozpuštěným baryem a zásaditostí oceánů.
Korelaci rozpuštěného barya s kyselinou křemičitou lze vidět vertikálně i prostorově. Částicový barium vykazuje silnou korelaci s částicovým organickým uhlíkem nebo POC. Baryum se stává stále oblíbenějším pro použití jako základ pro paleoceanografické proxy. Díky propojení rozpuštěného i částicového barya s kyselinou křemičitou a POC je možné jej použít k určení historických variací biologické pumpy, uhlíkového cyklu a globálního klimatu.
Barit částicového barya (BaSO 4 ), jako jeden z mnoha proxy, lze použít k poskytnutí řady historických informací o procesech v různých oceánských podmínkách (vodní sloupec, sedimenty a hydrotermální lokality). V každém nastavení existují rozdíly v izotopickém a elementárním složení barytových částic. Baryt ve vodním sloupci, známý jako mořský nebo pelagický baryt, odhaluje informace o změnách chemie mořské vody v průběhu času. Baryt v sedimentech, známý jako diagenetický nebo studený prosakuje baryt, poskytuje informace o sedimentárních redoxních procesech. Baryt vytvořený hydrotermální aktivitou v hydrotermálních otvorech, známý jako hydrotermální baryt, odhaluje změny v stavu zemské kůry kolem těchto průduchů.
Toxicita
| Nebezpečí | |
|---|---|
| Piktogramy GHS |

|
| Signální slovo GHS | Nebezpečí |
| H261 | |
| P231+232 , P335+334 , P370+378 , P402+404 | |
| NFPA 704 (ohnivý diamant) | |
Vzhledem k vysoké reaktivitě kovu jsou toxikologická data k dispozici pouze pro sloučeniny. Rozpustné sloučeniny barya jsou jedovaté. V nízkých dávkách působí ionty barya jako svalový stimulant a vyšší dávky ovlivňují nervový systém , což způsobuje srdeční nepravidelnosti, třes, slabost, úzkost , dušnost a paralýzu . Tato toxicita může být způsobena blokováním kanálů iontů draslíku Ba 2+ , které jsou rozhodující pro správnou funkci nervového systému. Další orgány poškozené ve vodě rozpustnými sloučeninami barya (tj. Ionty barya) jsou oči, imunitní systém, srdce, dýchací systém a kůže způsobující například oslepnutí a senzibilizaci.
Baryum není karcinogenní a není bioakumulativní . Vdechovaný prach obsahující nerozpustné sloučeniny barya se může hromadit v plicích, což způsobuje benigní stav nazývaný baritóza . Nerozpustný síran je netoxický a není v přepravních předpisech klasifikován jako nebezpečné zboží.
Aby se zabránilo potenciálně silné chemické reakci, je kov barya uchováván v argonové atmosféře nebo pod minerálními oleji. Kontakt se vzduchem je nebezpečný a může způsobit vznícení. Je třeba se vyvarovat vlhkosti, tření, horka, jisker, plamenů, otřesů, statické elektřiny a působení oxidačních činidel a kyselin. Cokoli, co se může dotýkat barya, by mělo být elektricky uzemněno. Každý, kdo pracuje s kovem, by měl nosit předem vyčištěné nejiskřivé boty, gumové oděvy odolné proti ohni, gumové rukavice, zástěru, brýle a plynovou masku. Kouření v pracovním prostoru je obvykle zakázáno. Po manipulaci s baryem je nutné důkladné umytí.
Viz také
- Purpurová a Hanova modrá - syntetické pigmenty křemičitanu barnatého a mědi, vyvinuté a používané ve starověké a císařské Číně
Reference
externí odkazy
- Barium v periodické tabulce videí (University of Nottingham)
- Elementymologie a prvky Multidict
- 3-D holografický displej s použitím niobátu strontnatého a barnatého







