Kysličník uhelnatý - Carbon monoxide
|
|
|||
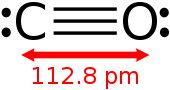
|
|||
| Jména | |||
|---|---|---|---|
|
Preferovaný název IUPAC
Kysličník uhelnatý |
|||
| Ostatní jména
Kysličník uhličitý oxid
Carbon protoxide oxid oxidu protoxide oxidu uhlíku mono-oxid Carbonous oxid carbonei oxidum kysličníkem de Carbone Carbon (II), oxidu carbonii halitus carboneum oxgenisatum karbátového karbonyl Kohlenoxyd plyn vody Spaliny uhličitý hořlavý vzduch těžký hořlavý vzduch hydrogenuhličitanu sycené vodíkové bílá vlhké důlní plyn práškový plyn osvětlovací plyn Dowson plyn Mond plynová energie výrobce plynu plynová vysoká pec plyn uhelný plyn phlogiston |
|||
| Identifikátory | |||
|
3D model ( JSmol )
|
|||
| 3587264 | |||
| ČEBI | |||
| CHEMBL | |||
| ChemSpider | |||
| Informační karta ECHA |
100,010,118 |
||
| Číslo ES | |||
| 421 | |||
| KEGG | |||
| Pletivo | Oxid uhelnatý+oxid uhelnatý | ||
|
PubChem CID
|
|||
| Číslo RTECS | |||
| UNII | |||
| UN číslo | 1016 | ||
|
CompTox Dashboard ( EPA )
|
|||
|
|||
|
|||
| Vlastnosti | |||
| CO | |||
| Molární hmotnost | 28,010 g/mol | ||
| Vzhled | Bezbarvý plyn | ||
| Zápach | Bez zápachu | ||
| Hustota | |||
| Bod tání | -205,02 ° C (-337,04 ° F; 68,13 K) | ||
| Bod varu | -191,5 ° C (-312,7 ° F; 81,6 K) | ||
| 27,6 mg/l (25 ° C) | |||
| Rozpustnost | rozpustný v chloroformu , kyselině octové , ethylacetátu , ethanolu , hydroxidu amonném , benzenu | ||
|
Henryho
konstanta ( k H ) |
1,04 atm · m 3 /mol | ||
| −9,8 · 10 −6 cm 3 /mol | |||
|
Index lomu ( n D )
|
1.0003364 | ||
| 0,122 D | |||
| Termochemie | |||
|
Tepelná kapacita ( C )
|
29,1 J/(K · mol) | ||
|
Standardní molární
entropie ( S |
197,7 J/(K · mol) | ||
|
Standardní entalpie
tvorby (Δ f H ⦵ 298 ) |
−110,5 kJ/mol | ||
|
Standardní entalpie
spalování (Δ c H ⦵ 298 ) |
−283,4 kJ/mol | ||
| Farmakologie | |||
| V04CX08 ( WHO ) | |||
| Nebezpečí | |||
| Bezpečnostní list |
Viz: datová stránka ICSC 0023 |
||
| Piktogramy GHS |
  
|
||
| Signální slovo GHS | Nebezpečí | ||
| H220 , H331 , H360 , H372 | |||
| P201 , P202 , P210 , P260 , P261 , P264 , P270 , P271 , P281 , P304 + 340 , P308 + 313 , P311 , P314 , P321 , P377 , P381 , P403 , P403 + 233 , P405 , P501 | |||
| NFPA 704 (ohnivý diamant) | |||
| Bod vzplanutí | -191 ° C (-311,8 ° F; 82,1 K) | ||
| 609 ° C (1 128 ° F; 882 K) | |||
| Výbušné limity | 12,5–74,2% | ||
| Smrtelná dávka nebo koncentrace (LD, LC): | |||
|
LC 50 ( střední koncentrace )
|
|||
|
LC Lo ( nejnižší publikované )
|
|||
| NIOSH (limity expozice USA pro zdraví): | |||
|
PEL (přípustné)
|
PEL 50 ppm (55 mg/m 3 ) | ||
|
REL (doporučeno)
|
|||
|
IDLH (bezprostřední nebezpečí)
|
1200 str./min | ||
| Související sloučeniny | |||
|
Jiné anionty
|
Monosulfid uhlíku | ||
|
Jiné kationty
|
Oxid křemičitý Oxid německý Oxid cínatý Oxid olovnatý |
||
|
Související oxidy uhlíku
|
Oxid uhličitý Suboxid uhličitý Oxokarbony |
||
| Stránka doplňkových údajů | |||
|
Index lomu ( n ), dielektrická konstanta (ε r ) atd. |
|||
|
Termodynamická
data |
Fázové chování pevná látka – kapalina – plyn |
||
| UV , IR , NMR , MS | |||
|
Pokud není uvedeno jinak, jsou údaje uvedeny pro materiály ve standardním stavu (při 25 ° C [77 ° F], 100 kPa). |
|||
|
|
|||
| Reference na infobox | |||
Oxid uhelnatý ( chemický vzorec CO ) je bezbarvý hořlavý plyn bez chuti a zápachu, který je o něco méně hustý než vzduch. Oxid uhelnatý se skládá z jednoho atomu uhlíku a jednoho atomu kyslíku . Je to nejjednodušší molekula z rodiny oxokarbonů . V koordinačních komplexech se ligand oxidu uhelnatého nazývá karbonyl .
Tepelné spalování je nejběžnějším zdrojem oxidu uhelnatého, existuje však řada environmentálních a biologických zdrojů, které generují a emitují značné množství oxidu uhelnatého. Lidé využívají oxid uhelnatý k různým průmyslovým procesům, včetně syntetické chemické výroby a metalurgie , je to však také problematická látka znečišťující ovzduší vyplývající z průmyslových činností. Po emisi do atmosféry může mít oxid uhelnatý role, které potenciálně ovlivňují změnu klimatu .
Oxid uhelnatý má důležité biologické role napříč fylogenetickými královstvími. V savčích fyziologii, oxid uhelnatý je klasickým příkladem hormese kde nízké koncentrace slouží jako vnitřní neurotransmiteru ( gasotransmitter ) a vysokých koncentracích jsou toxické, což vede ke otrava oxidem uhelnatým .
Dějiny
Pravěk
Lidé si udržují komplexní vztah s oxidem uhelnatým od doby, kdy se poprvé naučili ovládat oheň kolem roku 800 000 př. N. L. Primitivní jeskynní muž pravděpodobně objevil toxicitu otravy oxidem uhelnatým po zavedení ohně do svých obydlí. Počáteční vývoj metalurgie a technologií tavení vznikajících kolem roku 6 000 př. N. L. V době bronzové také sužoval lidstvo z expozice oxidu uhelnatého. Kromě toxicity oxidu uhelnatého mohli domorodí domorodí Američané zažít neuroaktivní vlastnosti oxidu uhelnatého prostřednictvím šamanistických ohňových rituálů.
Dávná historie
Rané civilizace vyvinuly mytologické příběhy vysvětlující původ ohně, například Prometheus z řecké mytologie, který sdílel oheň s lidmi. Aristoteles (384–322 př. N. L.) Poprvé zaznamenal, že hořící uhlí produkuje toxické výpary. Řecký lékař Galen (129-199 nl), spekuloval, že došlo ke změně ve složení vzduchu, který způsobil škodu při vdechování, a mnoho dalších éry vytvořil základ znalostí o oxidu uhelnatého v rámci uhelného toxicity kouře. Kleopatra možná zemřela na otravu oxidem uhelnatým .
Moderní historie
Georg Ernst Stahl zmínil carbonarii halitus v roce 1697 v odkazu na toxické páry považované za oxid uhelnatý. Friedrich Hoffmann provedl první moderní vědecký výzkum otravy oxidem uhelnatým z uhlí v roce 1716. Herman Boerhaave provedl první vědecké experimenty o účinku oxidu uhelnatého (uhelné výpary) na zvířata ve 30. letech 17. století.
Má se za to, že Joseph Priestley poprvé syntetizoval oxid uhelnatý v roce 1772. Carl Wilhelm Scheele podobně izoloval oxid uhelnatý z dřevěného uhlí v roce 1773 a domníval se, že by to mohla být uhlíková entita produkující toxické zplodiny. Torbern Bergman izolovaný oxid uhelnatý z kyseliny šťavelové v roce 1775. Později v roce 1776, francouzský chemik de Lassone vyrobené CO zahříváním oxidu zinečnatého s koksem , ale chybně dospěl k závěru, že se plynný produkt byl atom vodíku , jak je to spáleno modrým plamenem. V přítomnosti kyslíku, včetně atmosférických koncentrací, hoří oxid uhelnatý modrým plamenem a vzniká oxid uhličitý. Antoine Lavoisier provedeny podobné experimenty neprůkazné Lassone v roce 1777. Tento plyn byl identifikován jako sloučenina, obsahující uhlík a kyslík, od William Cruickshank v roce 1800.
Thomas Beddoes a James Watt rozpoznali oxid uhelnatý (jako uhlovodík ) k zesvětlení žilní krve v roce 1793. Watt navrhl, že uhelné výpary mohou působit jako protijed na kyslík v krvi, a Beddoes a Watt rovněž navrhli, že uhlovodík má větší afinitu k živočišným vláknům než kyslík v roce 1796. V roce 1854 Adrien Chenot podobně navrhl oxid uhelnatý k odstranění kyslíku z krve a poté v těle oxiduje na oxid uhličitý. Mechanismus otravy oxidem uhelnatým je široce připisován Claude Bernardovi, jehož paměti začínající v roce 1846 a publikované v roce 1857, které formulovaly, „zabraňují tomu, aby se arteriální krev stala žilní“. Felix Hoppe-Seyler nezávisle publikoval podobné závěry v následujícím roce.
Fyzikální a chemické vlastnosti
Oxid uhelnatý je nejjednodušší oxokarbon a je izoelektronický s dalšími trojitě vázanými diatomickými druhy s 10 valenčními elektrony, včetně kyanidového aniontu, nitrosoniového kationtu, monofluoridu boritého a molekulárního dusíku . Má molární hmotnost 28,0, což jej podle zákona o ideálním plynu činí o něco méně hustým než vzduch, jehož průměrná molární hmotnost je 28,8.
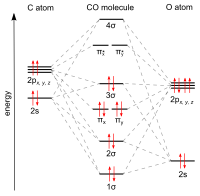
Uhlík a kyslík jsou spojeny trojnou vazbou, která se skládá ze sítě dvou pí vazeb a jedné sigma vazby . Délka vazby mezi atomem uhlíku a atomem kyslíku je 112,8 pm . Tato délka vazby je v souladu s trojnou vazbou, jako v molekulární dusík (N 2 ), který má podobnou délku vazby (109,76 pm) a téměř stejnou molekulovou hmotnost . Dvojné vazby uhlík -kyslík jsou podstatně delší, například 120,8 pm ve formaldehydu . Bod varu (82 K) a s teplotou tání (68 K), jsou velmi podobné těm, N 2 (77 K a 63 K, v tomto pořadí). Vazba-disociace energie z 1072 kJ / mol, je silnější než N 2 (942 kJ / mol) a představuje nejsilnější chemickou vazbu známý.
Důvod elektronový stav oxidu uhelnatého je singlet stav , protože nejsou k dispozici žádné nepárové elektrony.
Spojovací a dipólový moment
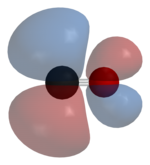
Uhlík a kyslík mají dohromady ve valenčním obalu celkem 10 elektronů . Podle oktetového pravidla pro uhlík i kyslík tvoří tyto dva atomy trojnou vazbu se šesti sdílenými elektrony ve třech vazebných molekulárních orbitalech, než s obvyklou dvojnou vazbou, která se nachází v organických karbonylových sloučeninách. Protože čtyři ze sdílených elektronů pocházejí z atomu kyslíku a pouze dva z uhlíku, je jeden spojovací orbitál obsazen dvěma elektrony z kyslíku a tvoří dativní nebo dipolární vazbu . To způsobí polarizaci molekuly C ← O s malým záporným nábojem na uhlíku a malým kladným nábojem na kyslíku. Zbylé dva vazebné orbitaly jsou obsazeny jedním elektronem z uhlíku a jedním z kyslíku, čímž vznikají (polární) kovalentní vazby s reverzní polarizací C → O, protože kyslík je elektronegativnější než uhlík. Ve volném oxidu uhelnatého molekuly, čistý negativní náboj δ - zůstává na konci uhlíku a molekula má malou dipólový moment z 0,122 D .
Molekula je tedy asymetrická: kyslík má větší elektronovou hustotu než uhlík a je také mírně kladně nabitý ve srovnání s negativním uhlíkem. Naproti tomu isoelektronická molekula dinitrogenu nemá dipólový moment.
Oxid uhelnatý má vypočítaný řád frakčních vazeb 2,6, což naznačuje, že „třetí“ vazba je důležitá, ale představuje poněkud méně než úplná vazba. Z hlediska valenčních vazeb je tedy - C≡O + nejdůležitější struktura, zatímco: C = O je neoktetový, ale má neutrální formální náboj na každém atomu a představuje druhého nejdůležitějšího přispěvatele rezonance. Vzhledem k osamělému páru a dvojmocnosti uhlíku v této rezonanční struktuře je oxid uhelnatý často považován za mimořádně stabilizovaný karben . Isocyanidy jsou sloučeniny, ve kterých je O nahrazen skupinou NR (R = alkyl nebo aryl) a mají podobné schéma vazby.
Pokud oxid uhelnatý působí jako ligand , polarita dipólu se může obrátit s čistým záporným nábojem na konci kyslíku v závislosti na struktuře koordinačního komplexu . Viz také níže uvedenou sekci „Koordinační chemie“ .
Polarita vazby a oxidační stav
Teoretické a experimentální studie ukazují, že navzdory větší elektronegativitě kyslíku dipólový moment směřuje od negativnějšího konce uhlíku k pozitivnějšímu konci kyslíku. Tyto tři vazby jsou ve skutečnosti polární kovalentní vazby, které jsou silně polarizované. Vypočítaná polarizace vůči atomu kyslíku je 71% pro σ-vazbu a 77% pro obě π-vazby .
Oxidační uhlíku v oxidu uhelnatého je 2 v každé z těchto struktur. Vypočítává se počítáním všech spojovacích elektronů, které patří k elektronegativnějšímu kyslíku. Uhlíku jsou přiřazeny pouze dva nevazebné elektrony na uhlíku. V tomto počtu má uhlík v molekule pouze dva valenční elektrony ve srovnání se čtyřmi ve volném atomu.
Výskyt
Oxid uhelnatý se vyskytuje v různých přírodních a umělých prostředích. Typické koncentrace v částech na milion jsou následující:
| Koncentrace (ppmv) | Zdroj |
|---|---|
| 0,1 | Hladina přirozené atmosféry ( MOPITT ) |
| 0,5–5 | Průměrná úroveň v domácnostech |
| 5–15 | V blízkosti správně nastavených plynových kamen v domácnostech moderní emise výfukových plynů z vozidel |
| 17 | Atmosféra Venuše |
| 100–200 | Výfuk z automobilů v centrální oblasti Mexico City v roce 1975 |
| 700 | Atmosféra Marsu |
| <1000 | Výfukové plyny z auta po průchodu katalyzátorem |
| 5 000 | Odsávání z domácího dřevěného ohně |
| 30 000–100 000 | Neředěný teplý výfuk auta bez katalyzátoru |
Atmosférická přítomnost
Oxid uhelnatý (CO) je v zemské atmosféře přítomen v malém množství (asi 80 ppb) . Většina zbytku pochází z chemických reakcí s organickými sloučeninami emitovanými lidskou činností a přírodním původem v důsledku fotochemických reakcí v troposféře, které generují přibližně 5 × 10 12 kilogramů ročně. Další přírodní zdroje CO patří sopky, lesní a bushfires požárů, a různé jiné formy, jako je spalování fosilních paliv . Malé množství je také emitováno z oceánu az geologické činnosti, protože oxid uhelnatý se rozpouští v roztavené vulkanické hornině při vysokých tlacích v zemském plášti . Protože jsou přírodní zdroje oxidu uhelnatého rok od roku tak proměnlivé, je obtížné přesně měřit přirozené emise plynu.
Oxid uhelnatý má nepřímý účinek na radiační působení zvýšením koncentrací přímých skleníkových plynů , včetně metanu a troposférického ozonu . CO může chemicky reagovat s jinými atmosférickými složkami (především s hydroxylovým radikálem , OH . ), Které by jinak zničily metan. Přirozenými procesy v atmosféře se oxiduje na oxid uhličitý a ozon. Oxid uhelnatý má v atmosféře krátkou životnost (s průměrnou životností přibližně jeden až dva měsíce) a v koncentraci je prostorově variabilní.
Díky své dlouhé životnosti ve střední troposféře se oxid uhelnatý používá také jako indikátor pro oblaky znečišťujících látek.
Znečištění
Městské znečištění
Oxid uhelnatý je v některých městských oblastech dočasnou látkou znečišťující ovzduší, zejména z výfuků spalovacích motorů (včetně vozidel, přenosných a záložních generátorů, sekaček na trávu, myček atd.), Ale také z neúplného spalování různých jiných paliv ( včetně dřeva, uhlí, dřevěného uhlí, ropy, parafinu, propanu, zemního plynu a odpadu).
Z vesmíru nad městy lze pozorovat velké události znečištění CO.
Role při tvorbě přízemního ozónu
Oxid uhelnatý je spolu s aldehydy součástí řady cyklů chemických reakcí, které tvoří fotochemický smog . Reaguje s hydroxylovým radikálem ( • OH) za vzniku radikálního meziproduktu • HOCO, který rychle přenáší svůj radikální vodík na O 2 za vzniku peroxylového radikálu (HO 2 • ) a oxidu uhličitého (CO 2 ). Peroxylový radikál následně reaguje s oxidem dusičitým (NO) za vzniku oxidu dusičitého (NO 2 ) a hydroxylového radikálu. NO 2 poskytuje O ( 3 P) fotolýzou, čímž se vytvoří O 3 po reakci s O 2 . Vzhledem k tomu, že při tvorbě NO 2 vzniká hydroxylový radikál , rovnováha posloupnosti chemických reakcí počínaje oxidem uhelnatým a vedoucí k tvorbě ozónu je:
- CO + 2O 2 + hν → CO 2 + O 3
(kde hν označuje foton světla absorbovaný molekulou NO 2 v sekvenci)
Přestože je tvorba NO 2 kritickým krokem vedoucím k nízké tvorbě ozónu , zvyšuje také tento ozon jiným, poněkud vzájemně se vylučujícím způsobem, snížením množství NO, které je k dispozici pro reakci s ozonem.
Vnitřní znečištění
V uzavřených prostředích může koncentrace oxidu uhelnatého stoupnout až na smrtelné úrovně. V průměru 170 lidí ve Spojených státech zemře každý rok na oxid uhelnatý produkovaný neautomobilovými spotřebními výrobky. Mezi tyto produkty patří nefunkční zařízení na spalování paliva, jako jsou pece, sporáky, ohřívače vody a plynové a petrolejové ohřívače místností; zařízení poháněná motorem, jako jsou přenosné generátory (a auta ponechaná v provozu v přidružených garážích); krby; a dřevěné uhlí, které se spaluje v domech a jiných uzavřených prostorách. Během výpadků elektřiny v důsledku nepříznivého počasí, jako je hurikán Katrina a energetická krize v Texasu v roce 2021, došlo k mnoha úmrtím .
Astronomie
Kromě Země je oxid uhelnatý po molekulárním vodíku druhou nejběžnější diatomickou molekulou v mezihvězdném prostředí . Díky své asymetrii tato polární molekula produkuje mnohem jasnější spektrální čáry než molekula vodíku, což výrazně usnadňuje detekci CO. Mezihvězdný CO byl poprvé detekován pomocí radioteleskopů v roce 1970. Nyní je nejběžněji používaným indikátorem molekulárního plynu obecně v mezihvězdném prostředí galaxií, protože molekulární vodík lze detekovat pouze pomocí ultrafialového světla, které vyžaduje vesmírné teleskopy . Pozorování oxidu uhelnatého poskytuje mnoho informací o molekulárních mracích, ve kterých vzniká většina hvězd .
Beta Pictoris , druhá nejjasnější hvězda v souhvězdí Pictor , vykazuje nadbytek normálních hvězd ve srovnání s normálními hvězdami svého druhu, což je způsobeno velkým množstvím prachu a plynu (včetně oxidu uhelnatého) poblíž hvězdy.
V atmosféře Venuše dochází k oxidu uhelnatému v důsledku fotodisociace oxidu uhličitého elektromagnetickým zářením o vlnových délkách kratších než 169 nm . Byl také spektroskopicky identifikován na povrchu Neptunova měsíce Triton .
Pevný oxid uhelnatý je součástí komet . Halleyova kometa je asi 15% oxidu uhelnatého. Při pokojové teplotě a atmosférickém tlaku je oxid uhelnatý ve skutečnosti pouze metastabilní (viz Boudouardova reakce ) a totéž platí při nízkých teplotách, kde CO a CO
2jsou solidní, ale přesto mohou v kometách existovat miliardy let. V atmosféře Pluta , které se zdá být vytvořeno z komet, je velmi málo CO . Důvodem může být to, že uvnitř Pluta je (nebo byla) kapalná voda.
Oxid uhelnatý může reagovat s vodou za vzniku oxidu uhličitého a vodíku:
- CO + H 2 O → H
2+ CO
2
Toto se nazývá reakce posunu vody a plynu, když se vyskytuje v plynné fázi, ale může také probíhat (velmi pomalu) ve vodném roztoku. Pokud je parciální tlak vodíku dostatečně vysoký (například v podzemním moři), vytvoří se kyselina mravenčí :
- CO + H 2 O → HCOOH
Tyto reakce mohou proběhnout za několik milionů let i při teplotách, jaké se vyskytují na Plutu.
Niche používá
Oxid uhelnatý byl navržen pro použití jako palivo na Marsu. Uhelnatý / kyslík motory Carbon byly navrženy pro povrchové použití předčasného dopravy jako jak oxidu uhelnatého a kyslíku nemohou být přímo vyrobené z oxidu uhličitého atmosféry Marsu u oxidu zirkoničitého elektrolýzou , bez použití jakýchkoli Marsu vodních zdrojů pro získání vodíku, které by bylo zapotřebí, aby se metan nebo jakékoli palivo na bázi vodíku.
Chemie
Oxid uhelnatý má širokou škálu funkcí napříč všemi obory chemie. Čtyři hlavní kategorie reaktivity zahrnují kovovou karbonylovou katalýzu, radikálovou chemii, kationtovou a aniontovou chemii.
Koordinační chemie
Většina kovů tvoří koordinační komplexy obsahující kovalentně navázaný oxid uhelnatý. Pouze kovy v nižších oxidačních stavech budou tvořit komplex s ligandy oxidu uhelnatého . Důvodem je, že musí existovat dostatečná elektronová hustota, aby se usnadnilo zpětné darování z kovu d xz -orbitální, na π* molekulární orbitál z CO. Osamělý pár na atomu uhlíku v CO také daruje elektronovou hustotu d x² − y² na kov, aby se vytvořila vazba sigma . Toto darování elektronů je také vystaveno cis efektem nebo labilizací CO ligandů v cis poloze. Například karbonyl niklu vzniká přímou kombinací oxidu uhelnatého a niklu :
- Ni + 4 CO → Ni (CO) 4 (1 bar, 55 ° C)
Z tohoto důvodu nesmí nikl v žádné trubce nebo části přijít do dlouhodobého kontaktu s oxidem uhelnatým. Karbonyl niklu se při kontaktu s horkými povrchy snadno rozkládá zpět na Ni a CO a tato metoda se používá k průmyslovému čištění niklu v procesu Mond .
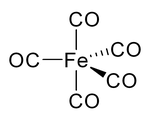
V karbonylu niklu a dalších karbonylech interaguje elektronový pár na uhlíku s kovem; oxid uhelnatý daruje elektronový pár kovu. V těchto situacích se oxid uhelnatý nazývá karbonylový ligand . Jedním z nejdůležitějších kovových karbonylů je pentakarbonyl železa , Fe (CO) 5 :
Mnoho kov-CO komplexy se připraví dekarbonylace organických rozpouštědel, a ne z CO. Například, iridium chloridu a trifenylfosfin reagovat ve vroucím 2-methoxyethanolu nebo DMF , čímž se získá IrCl (CO) (PPh 3 ) 2 .
Kovové karbonyly v koordinační chemii se obvykle studují pomocí infračervené spektroskopie .
Organická a hlavní skupinová chemie
V přítomnosti silných kyselin a vody reaguje oxid uhelnatý s alkeny za vzniku karboxylových kyselin v procesu známém jako Koch -Haafova reakce. V reakci Gattermann-Koch , arenů jsou převedeny na benzaldehydu derivátů v přítomnosti chloridu hlinitého 3 a kyseliny chlorovodíkové . Organolithné sloučeniny (např. Butyllithium ) reagují s oxidem uhelnatým, ale tyto reakce mají jen malé vědecké využití.
Přestože CO reaguje s karbokationty a karbanionty , vůči organickým sloučeninám je relativně nereaktivní bez zásahu kovových katalyzátorů.
U činidel hlavní skupiny prochází CO několika pozoruhodnými reakcemi. Chlorace CO je průmyslovou cestou k důležité sloučenině fosgenu . S boranem CO tvoří adukt H 3 BCO , který je isoelektronický s kationtem acetylia [H 3 CCO] + . CO reaguje s sodíku , čímž se získá produkty vznikající CC spojovacího jako je acetylenediolate sodný 2 Na+
· C
2Ó2-
2. Reaguje s roztaveným draslíkem za vzniku směsi organokovové sloučeniny, acetylenediolátu draselného 2 K+
· C
2Ó2-
2, benzenhexolát draselný 6 K+
C
6Ó6-
6a rhodizonát draselný 2 K.+
· C
6Ó2-
6.
Sloučeniny cyklohexanhexon nebo trichinoyl (C 6 O 6 ) a cyklopentanepenton nebo kyselina leukonová (C 5 O 5 ), které byly dosud získány pouze ve stopových množstvích, lze považovat za polymery oxidu uhelnatého.
Laboratorní příprava
Oxid uhelnatý se výhodně vyrábí v laboratoři pomocí dehydratace z kyseliny mravenčí nebo kyseliny šťavelové , například s koncentrovanou kyselinou sírovou . Další metodou je zahřívání intimní směsi práškového zinku a uhličitanu vápenatého , které uvolňují CO a zanechávají za sebou oxid zinečnatý a oxid vápenatý :
- Zn + CaCO 3 → ZnO + CaO + CO
Dusičnan stříbrný a jodoform také poskytují oxid uhelnatý:
- CHI 3 + 3AgNO 3 + H 2 O → 3HNO 3 + CO + 3AgI
A konečně, oxalátové soli kovů uvolňují CO po zahřátí a zanechávají uhličitan jako vedlejší produkt:
-
Na
2C
2Ó
4→ Na
2CO
3+ CO
Výroba
Tepelné spalování je nejběžnějším zdrojem oxidu uhelnatého. Oxid uhelnatý se vyrábí částečnou oxidací sloučenin obsahujících uhlík ; vzniká, když není dostatek kyslíku k produkci oxidu uhličitého (CO 2 ), například při provozu kamen nebo spalovacího motoru v uzavřeném prostoru. Například během druhé světové války byla plynová směs obsahující oxid uhelnatý používána k udržování motorových vozidel v částech světa, kde bylo málo benzínu a nafty . Byly namontovány externí (až na několik výjimek) dřevěné uhlí nebo generátory dřevoplynu a směs atmosférického dusíku, vodíku, oxidu uhelnatého a malého množství dalších plynů produkovaných zplyňováním byla vedena do míchačky plynu. Plynná směs vyrobená tímto způsobem je známá jako dřevoplyn .
Během oxidačních procesů výroby chemikálií vzniká velké množství vedlejších produktů CO. Z tohoto důvodu musí být procesní odpadní plyny čištěny. Na druhé straně je vynaloženo značné úsilí v oblasti výzkumu s cílem optimalizovat podmínky procesu, vyvinout katalyzátor se zlepšenou selektivitou a porozumět reakčním cestám vedoucím k cílovému produktu a vedlejším produktům.
Pro výrobu oxidu uhelnatého bylo vyvinuto mnoho metod.
Průmyslová produkce
Hlavním průmyslovým zdrojem CO je produkční plyn , směs obsahující převážně oxid uhelnatý a dusík, vznikající spalováním uhlíku ve vzduchu při vysoké teplotě při přebytku uhlíku. V peci prochází vzduch ložem koksu . Původně vyrobený CO 2 ekvilibruje se zbývajícím horkým uhlíkem za vzniku CO. Reakce CO 2 s uhlíkem za vzniku CO je popsána jako Boudouardova reakce . Nad 800 ° C je převládajícím produktem CO:
- CO 2 + C → 2 CO (ΔH = 170 kJ/mol)
Dalším zdrojem je „ vodní plyn “, směs vodíku a oxidu uhelnatého vyráběná endotermickou reakcí páry a uhlíku:
- H 2 O + C → H 2 + CO (ΔH = +131 kJ/mol)
Další podobné „ syntézní plyny “ lze získat ze zemního plynu a jiných paliv.
Oxid uhelnatý lze také vyrábět vysokoteplotní elektrolýzou oxidu uhličitého elektrolyzéry s pevnými oxidy : Jedna metoda vyvinutá ve společnosti DTU Energy používá katalyzátor na bázi oxidu ceru a nemá žádné problémy s ucpáváním katalyzátoru.
- 2 CO 2 → 2 CO + O 2
Oxid uhelnatý je také vedlejším produktem redukce rud oxidu kovu uhlíkem, který je ve zjednodušené formě znázorněn následovně:
- MO + C → M + CO
Oxid uhelnatý se také vyrábí přímou oxidací uhlíku v omezeném množství kyslíku nebo vzduchu.
- 2 C (s) + O 2 → 2 CO (g)
Vzhledem k tomu, že CO je plyn, může být redukční proces řízen zahříváním s využitím pozitivní (příznivé) entropie reakce. Tyto Ellingham diagram ukazuje, že tvorba CO je zvýhodněné během CO 2 ve vysokých teplotách.
Chemický průmysl
Oxid uhelnatý je průmyslový plyn, který má mnoho aplikací v hromadné výrobě chemikálií. Hydroformylační reakcí alkenů , oxidu uhelnatého a H 2 vzniká velké množství aldehydů . Hydroformylace je spojena s procesem Shell s vyšším olefinem za vzniku prekurzorů detergentů .
Fosgen , užitečný pro přípravu isokyanátů, polykarbonátů a polyurethanů, se vyrábí průchodem vyčištěného oxidu uhelnatého a plynného chloru ložem porézního aktivního uhlí , které slouží jako katalyzátor . Světová produkce této sloučeniny byla v roce 1989 odhadována na 2,74 milionu tun.
- CO + Cl 2 → COCl 2
Methanol se vyrábí hydrogenací oxidu uhelnatého. V související reakci je hydrogenace oxidu uhelnatého spojena s tvorbou vazby CC, jako je tomu ve Fischerově -Tropschově procesu, kde je oxid uhelnatý hydrogenován na kapalná uhlovodíková paliva. Tato technologie umožňuje přeměnu uhlí nebo biomasy na naftu.
V procesu Cativa oxid uhelnatý a methanol reagují v přítomnosti homogenního iridiového katalyzátoru a kyseliny jodovodíkové za vzniku kyseliny octové . Tento proces je zodpovědný za většinu průmyslové výroby kyseliny octové .
Hutnictví
Oxid uhelnatý je silné redukční činidlo a již od starověku se používá v pyrometalurgii ke snižování kovů z rud . Oxid uhelnatý odizoluje oxidy kovů z kyslíku, při vysokých teplotách je redukuje na čistý kov a při tomto procesu vzniká oxid uhličitý . Oxid uhelnatý se obvykle nedodává tak, jak je, v plynné fázi, do reaktoru, ale spíše se tvoří při vysoké teplotě v přítomnosti rudy nesoucí kyslík nebo karbonského činidla, jako je koks, a při vysoké teplotě. Proces ve vysoké peci je typickým příkladem procesu redukce kovu z rudy oxidem uhelnatým.
Podobně vysokopecní plyn shromažďovaný v horní části vysoké pece stále obsahuje přibližně 10% až 30% oxidu uhelnatého a používá se jako palivo v Cowperových kamnech a v pecích Siemens-Martin při výrobě oceli v otevřeném ohništi .
Hornictví
Těžaři označují oxid uhelnatý jako „ whitedamp “ nebo „tichý zabiják“. Lze jej nalézt v omezených oblastech se špatným větráním v povrchových i podzemních dolech. Nejčastějšími zdroji oxidu uhelnatého v těžebních operacích jsou spalovací motory a výbušniny, nicméně v uhelných dolech lze oxid uhelnatý nalézt také díky nízkoteplotní oxidaci uhlí. Idiom „ kanárek v uhelném dole “ se týkalo včasného varování o přítomnost oxidu uhelnatého.
Biologické a fyziologické vlastnosti
Fyziologie
Oxid uhelnatý je bioaktivní molekula, která působí jako plynná signální molekula . Přirozeně je produkován mnoha enzymatickými a neenzymatickými cestami, z nichž nejlépe porozumíme katabolickému působení hem oxygenázy na hem odvozený od hemoproteinů , jako je hemoglobin . Po první zprávě, že oxid uhelnatý je normální neurotransmiter v roce 1993, se oxidu uhelnatému jako biologickému regulátoru dostává značné klinické pozornosti.
Vzhledem k roli oxidu uhelnatého v těle jsou abnormality v jeho metabolismu spojeny s řadou chorob, včetně neurodegenerací, hypertenze, srdečního selhání a patologického zánětu. V mnoha tkáních působí oxid uhelnatý jako protizánětlivý , vazodilatační a povzbuzuje neovaskulární růst. Ve studiích na zvířecích modelech oxid uhelnatý snižoval závažnost experimentálně indukované bakteriální sepse , pankreatitidy, poškození ischemie/reperfúze jater, kolitidy, osteoartritidy, poranění plic, odmítnutí transplantace plic a neuropatické bolesti při podpoře hojení kožních ran. Proto existuje značný zájem o terapeutický potenciál, aby se oxid uhelnatý stal farmaceutickým činidlem a klinickým standardem péče.
Lék
Studie zahrnující oxid uhelnatý byly provedeny v mnoha laboratořích po celém světě pro jeho protizánětlivé a cytoprotektivní vlastnosti. Tyto vlastnosti mají potenciál být použity k prevenci vývoje řady patologických stavů, včetně ischemického reperfuzního poranění, odmítnutí transplantátu, aterosklerózy, těžké sepse, závažné malárie nebo autoimunity. Mnoho iniciativ pro dodávání farmaceutických léčiv vyvinulo metody bezpečného podávání oxidu uhelnatého a následné kontrolované klinické studie hodnotily terapeutický účinek oxidu uhelnatého.
Mikrobiologie
Microbiota může také využívat oxid uhelnatý jako plynový vysílač . Snímání oxidu uhelnatého je signální dráha usnadněná proteiny, jako je CooA . Rozsah biologických rolí pro snímání oxidu uhelnatého je stále neznámý.
Lidský mikrobiom produkuje, spotřebovává a reaguje na oxid uhelnatý. Například u některých bakterií je oxid uhelnatý produkován redukcí oxidu uhličitého pomocí enzymu oxid uhelnatý dehydrogenázy s příznivou bioenergetikou pro napájení navazujících buněčných operací. V dalším příkladu je oxid uhelnatý živinou pro methanogenní archea, která jej pomocí vodíku redukuje na metan.
Oxid uhelnatý má určité antimikrobiální vlastnosti, které byly studovány pro léčbu proti infekčním chorobám .
Věda o jídle
Oxid uhelnatý se v USA používá v obalových systémech s upravenou atmosférou , hlavně s čerstvými masnými výrobky, jako je hovězí, vepřové a ryby, aby vypadaly svěží. Výhoda je dvojnásobná, oxid uhelnatý chrání před mikrobiálním zkažením a zvýrazňuje barvu masa, aby byla přitažlivá pro spotřebitele. Oxid uhelnatý se spojuje s myoglobinem za vzniku karboxymyoglobinu, jasně třešňově červeného pigmentu. Karboxymyoglobin je stabilnější než okysličená forma myoglobinu, oxymyoglobin, který může oxidovat na hnědý pigment metmyoglobin . Tato stabilní červená barva může přetrvávat mnohem déle než u běžně baleného masa. Typické hladiny oxidu uhelnatého používané v zařízeních, která používají tento proces, jsou mezi 0,4% až 0,5%.
Tato technologie byla poprvé udělena statusem „ obecně uznávaného jako bezpečného “ (GRAS) americkým úřadem pro kontrolu potravin a léčiv (FDA) v roce 2002 pro použití jako sekundární balicí systém a nevyžaduje označování. V roce 2004 FDA schválila CO jako primární metodu balení a prohlásila, že CO nemaskuje zápach zkažení. Tento proces je v současné době neoprávněný v mnoha dalších zemích, včetně Japonska, Singapuru a Evropské unie .
Toxicita
Otrava oxidem uhelnatým je v mnoha zemích nejběžnějším typem smrtelné otravy vzduchem. Na Centra pro kontrolu a prevenci nemocí odhaduje, že několik tisíc lidí jít do nemocničních nouzových pokojích každý rok má být léčen na otravu oxidem uhelnatým. Podle floridského ministerstva zdravotnictví „každý rok zemře více než 500 Američanů na náhodné vystavení oxidu uhelnatému a tisíce dalších v USA vyžadují neodkladnou lékařskou péči o nefatální otravu oxidem uhelnatým“. Americká asociace center pro kontrolu jedů (AAPCC) informovala o 15 769 případech otravy oxidem uhelnatým, která si v roce 2007 vyžádala 39 úmrtí. V roce 2005 CPSC hlásila 94 úmrtí na otravu oxidem uhelnatým související s generátorem.
Oxid uhelnatý je bez barvy, bez zápachu a chuti. Jako takový je relativně nezjistitelný. Snadno se kombinuje s hemoglobinem za vzniku karboxyhemoglobinu, který potenciálně ovlivňuje výměnu plynu ; expozice tedy může být vysoce toxická. Koncentrace již od 667 ppm mohou způsobit přeměnu až 50% hemoglobinu v těle na karboxyhemoglobin. Hladina 50% karboxyhemoglobinu může mít za následek záchvat, kóma a smrt. Ve Spojených státech OSHA omezuje dlouhodobé úrovně expozice na pracovišti nad 50 ppm.
Kromě ovlivnění dodávky kyslíku se oxid uhelnatý také váže na jiné hemoproteiny, jako je myoglobin a mitochondriální cytochrom oxidáza , kovové a nekovové buněčné cíle, které ovlivňují mnoho buněčných operací.
Pozoruhodné úmrtí
Ačkoli nejsou k dispozici přesvědčivé důkazy, s otravou oxidem uhelnatým souvisí následující úmrtí:
Weaponizace
V dávné historii Hannibal během druhé punské války popravoval římské zajatce uhelnými výpary .
Oxid uhelnatý byl použit při genocidě během holocaustu v některých vyhlazovacích táborech , nejpozoruhodnější v dodávkách plynu v Chełmnu , a v programu „ eutanazie “ Akce T4 .
Při tlacích přes 5 gigapascalů se oxid uhelnatý mění na pevný polymer uhlíku a kyslíku . To je metastabilní při atmosférickém tlaku, ale je to silná výbušnina.
Smíšený
Lasery
Oxid uhelnatý byl také použit jako laserové médium ve vysoce výkonných infračervených laserech .
Viz také
- Oxid uhelnatý (stránka s údaji) - stránka s chemickými údaji
- Dýchejte oxid uhelnatý
- Detektor oxidu uhelnatého - Zařízení, které měří oxid uhelnatý (CO)
- Uhlovodík (plyn)
- Kritéria látky znečišťující ovzduší
- Seznam vysoce toxických plynů - článek seznamu Wikipedie
- Kuřácký paradox
- Podmořská a hyperbarická lékařská společnost - USA založila organizaci pro výzkum a vzdělání v hyperbarické fyziologii a medicíně. - hyperbarická léčba otravy CO
- Rubicon Foundation -nezisková organizace pro podporu výzkumu a přístup k informacím pro podvodní potápěčské výzkumné články o otravě CO
Reference
externí odkazy
- Globální mapa distribuce oxidu uhelnatého
- Vysvětlení struktury
- Sdružení pro bezpečnost oxidu uhelnatého
- Mezinárodní karta chemické bezpečnosti 0023
- Kapesní průvodce CDC NIOSH k chemickým nebezpečím: Oxid uhelnatý - Národní institut pro bezpečnost a ochranu zdraví při práci (NIOSH), Americká centra pro kontrolu a prevenci nemocí (CDC)
- Externí datový list MSDS
- Umístění detektoru oxidu uhelnatého
- Proces čištění oxidu uhelnatého
- Chemické experimenty s mikroskopickým plynem s oxidem uhelnatým
- „Okamžitý vhled: neobviňujte posla“ . Chemická biologie (11: Research News). 18. října 2007. Archivováno od originálu dne 28. října 2007 . Citováno 27. října 2019 . Nastínit fyziologii oxidu uhelnatého od Královské chemické společnosti .CS1 maint: postscript ( odkaz )