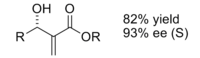Kyselina chirální Lewis - Chiral Lewis acid
Chirální Lewisovy kyseliny (CLA) jsou typem katalyzátoru Lewisových kyselin . Tyto kyseliny ovlivňují chiralitu substrátu, když s ním reagují. Při takových reakcích syntéza podporuje tvorbu specifického enantiomeru nebo diastereomeru . Metoda je enantioselektivní reakce asymetrické syntézy . Protože ovlivňují chiralitu, vyrábějí opticky aktivní produkty z opticky neaktivních nebo smíšených výchozích materiálů. Tento typ preferenční tvorby jednoho enantiomeru nebo diastereomeru před druhým je formálně známý jako asymetrická indukce . U tohoto druhu Lewisovy kyseliny je atom přijímající elektrony typicky kov, jako je indium , zinek , lithium , hliník , titan nebo bór . V chirální -altering ligandy použité pro syntézu tyto kyseliny mají často několik základních Lewisových míst (často diolu nebo strukturu dusný), které umožňují tvorbu kruhovou strukturu zahrnující atom kovu.
Kyseliny Achiral Lewis se používají po celá desetiletí k podpoře syntézy racemických směsí v nesčetných různých reakcích. Od šedesátých let minulého století chemici používají k vyvolání enantioselektivních reakcí kyseliny Chiral Lewis. To je užitečné, když je požadovaným produktem specifický enantiomer, jak je běžné při syntéze léčiv. Běžné typy reakce zahrnují Diels- reakcích en reakce , [2 + 2] cykloadiční reakce, kyanovodíku a aldehydů , a především, Sharpless epoxidations .
Teorie
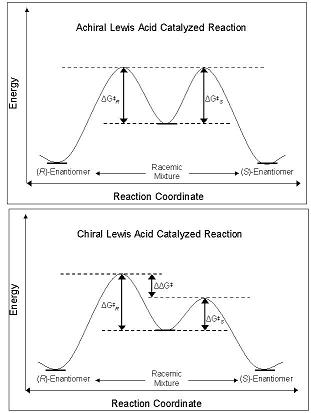
Enantioselektivita CLA je odvozena z jejich schopnosti narušit bariéru volné energie spolu s dráhou reakčních souřadnic , která vede buď k R- nebo S- enantiomeru. Diastereomery a enantiomery základního stavu mají v základním stavu stejnou energii a při reakci s achirální Lewisovou kyselinou mají jejich diastereomerní meziprodukty, přechodové stavy a produkty stejnou energii. To vede k výrobě racemických směsí . Pokud se však ve stejné reakci použije CLA, je energetická bariéra tvorby jednoho diastereomeru menší než u jiné; reakce je pod kinetickou kontrolou . Pokud jsou rozdíly v energetických bariérách mezi diastereomerními přechodovými stavy dostatečné velikosti, je pozorován vysoký enantiomerní přebytek jednoho izomeru.
Asymetrická syntéza
Diels-Alderova reakce
Diels-Alderovy reakce se vyskytují mezi konjugovaným dienem a alkenem (běžně známý jako dienofil ). Tento cykloadiční proces umožňuje stereoselektivní tvorbu cyklohexenových kruhů schopných mít až čtyři sousedící stereogenní centra.
Diels-Alderovy reakce mohou vést k tvorbě různých strukturních izomerů a stereoizomerů. Molekulární orbitální teorie se domnívá, že je preferován přechodový stav endo místo přechodového stavu exo (pravidlo přidání endo). Také se předpokládá, že rozšířené sekundární orbitální interakce jsou zdrojem vylepšené diastereoselace endo.
Obvykle se k aktivaci dienofilu používají CLA. Typický CLA katalyzátor je odvozen od chirálního centra Mg 2+ vyrobeného připojením esteru binol - fosfátu. CLA byly aplikovány na řadu intramolekulárních Diels-Alderových reakcí.
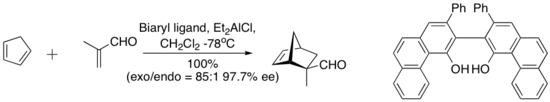
Komplex odvozený od diethylaluminiumchloridu a níže „klenutého“ biarylového ligandu katalyzuje enantioselektivní Diels-Alderovu reakci mezi cyklopentadienem a methakroleinem. Chirální ligand se získá kvantitativně chromatografií na silikagelu .
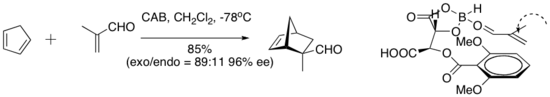
Chirální (acyloxy) boranový (CAB) komplex je účinný při katalýze řady aldehydových Diels-Alderových reakcí. NMR spektroskopické experimenty ukázaly těsnou blízkost aldehydu a arylového kruhu. Stohování pí mezi arylovou skupinou a aldehydem bylo navrženo jako organizační vlastnost, která cykloadici dodává vysokou enantioselektivitu.
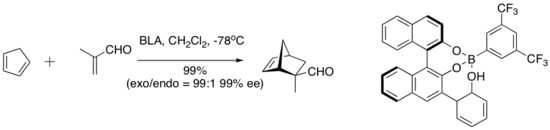
Chirální Lewisova kyselina (BLA) s Bronstedovou kyselinou katalyzuje řadu cykleničních reakcí dien-aldehyd.
Aldolová reakce
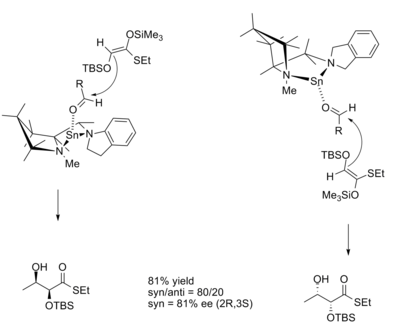
V aldolové reakci je diastereoselektivita produktu často dána geometrií enolátu. Model Zimmerman-Traxler předpovídá, že Z enolát poskytne syn produkty a že E enoláty anti produkty. Reakce katalyzované CLA na bázi cínu umožňují produktům odchýlit se od tohoto vzorce.
Přechodové struktury pro reakce s enantiomery katalyzátoru R i S jsou:
Baylis-Hillmanova reakce
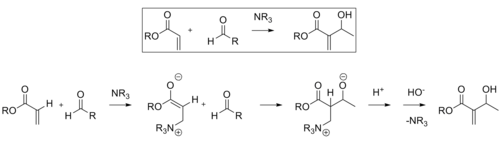
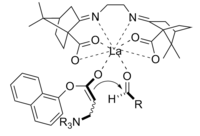
Baylis-Hillman reakce je cesta pro tvorbu CC vazby mezi alfa, beta-nenasycené karbonylové skupiny a aldehydu , který vyžaduje nukleofilní katalyzátor, obvykle terciární amin , pro přidání Michael-typu a eliminace. Stereoselektivita těchto reakcí je obvykle špatná. Bylo prokázáno, že CLA obsahující lanthan (III) zlepšují stereoselektivitu. Podobně může být také použit chirální amin pro dosažení stereoselektivity.
Produkt získaný reakcí za použití chirálního katalyzátoru byl získán v dobrém výtěžku s vynikající enantioselektivitou.
Ene reakce
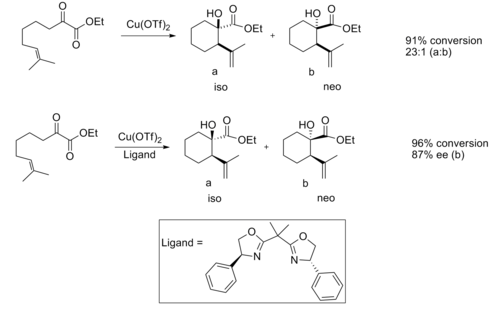
Chirální Lewisovy kyseliny se osvědčily v enové reakci . Když je katalyzována achirální Lewisovou kyselinou, reakce obvykle poskytuje dobrou diastereoselektivitu.
Při použití chirálního katalyzátoru na bázi Lewisovy kyseliny byla pozorována dobrá enantioselektivita.
Předpokládá se, že enantioselektivita je způsobena sterickými interakcemi mezi methylovou a fenylovou skupinou, což činí přechodovou strukturu izo produktu značně příznivější.
Kyseliny Achiral Lewis ve stereoselektivní syntéze
V některých případech může achirální Lewisova kyselina poskytovat dobrou stereoselektivitu. Kimura a kol. demonstroval regio- a diastereoselektivní kopulaci 1,3- dienů s aldehydy za použití niklového katalyzátoru.