Kyselina chlorovodíková - Chloric acid
|
|

|
|
| Jména | |
|---|---|
| Ostatní jména
Chlorová (V) kyselina
|
|
| Identifikátory | |
|
3D model ( JSmol )
|
|
| ChemSpider | |
| Informační karta ECHA |
100.029.303 |
| Číslo ES | |
|
PubChem CID
|
|
| UNII | |
| UN číslo | 2626 |
|
Řídicí panel CompTox ( EPA )
|
|
|
|
|
|
| Vlastnosti | |
| HClO 3 | |
| Molární hmotnost | 84,45914 g mol -1 |
| Vzhled | bezbarvý roztok |
| Hustota | 1 g / ml, roztok (přibližný) |
| > 40 g / 100 ml (20 ° C) | |
| Kyselost (p K a ) | ~ −1 |
| Konjugovaná základna | Chlorát |
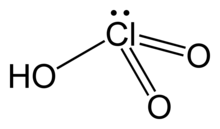
| Struktura | |
| pyramidový | |
| Nebezpečí | |
| Hlavní nebezpečí | Oxidant, Žíravý |
| Bezpečnostní list | Viz: datová stránka |
| Piktogramy GHS |
 
|
| Signální slovo GHS | Nebezpečí |
| H271 , H314 | |
| P210 , P220 , P221 , P260 , P264 , P280 , P283 , P301 + 330 + 331 , P303 + 361 + 353 , P304 + 340 , P305 + 351 + 338 , P306 + 360 , P310 , P321 , P363 , P370 + 378 , P371 + 380 + 375 , P405 , P501 | |
| NFPA 704 (ohnivý diamant) | |
| Související sloučeniny | |
|
Jiné anionty
|
kyselina bromová kyselina jodičná |
|
Jiné kationty
|
chlorečnan amonný chlorečnan sodný chlorečnan draselný |
|
Související sloučeniny
|
kyselina chlorovodíková kyselina chlorná kyselina chloritá kyselina chloristá |
| Stránka s doplňkovými údaji | |
|
Index lomu ( n ), dielektrická konstanta (ε r ) atd. |
|
|
Termodynamické
údaje |
Fázové chování pevná látka-kapalina-plyn |
| UV , IR , NMR , MS | |
|
Není-li uvedeno jinak, jsou uvedeny údaje o materiálech v jejich standardním stavu (při 25 ° C [77 ° F], 100 kPa). |
|
| Reference Infoboxu | |
Chlorečná kyselina , H Cl O 3 , je oxokyseliny z chloru , a formální předchůdce chlorečnanu solí. Je to silná kyselina ( p K a ≈ -2,7) a oxidační činidlo .
Vlastnosti
Kyselina chlorovodíková je termodynamicky nestabilní z hlediska disproporcionality .
Kyselina chlorovodíková je stabilní ve studeném vodném roztoku až do koncentrace přibližně 30% a roztok až do 40% lze připravit opatrným odpařováním za sníženého tlaku. Nad těmito koncentracemi se roztoky kyseliny chlorovodíkové rozkládají za vzniku různých produktů, například:
- 8 HClO 3 → 4 HClO 4 + 2 H 2 O + 2 Cl 2 + 3 O 2
- 3 HClO 3 → HClO 4 + H 2 O + 2 ClO 2
Nebezpečí
Kyselina chlorovodíková je silné oxidační činidlo. Většina organických látek a hořlavin bude při kontaktu deflagrovat.
Výroba
Může být připraven reakcí kyseliny sírové s chlorečnanem barnatým , přičemž nerozpustný síran barnatý je odstraněn srážením:
- Ba (ClO 3 ) 2 + H 2 SO 4 → 2 HCI O 3 + BaSO 4
Další metodou je ohřev kyseliny chlorné za vzniku kyseliny chlorovodíkové a chlorovodíku :
- 3 HClO → HClO 3 + 2 HCl
Viz také
- Chlorát
- Kyselina chlorná
- Kyselina chlorovodíková
- Kyselina chloristá
- Oxidující kyselina
- Oxid dichlornatý
Reference
- Greenwood, Norman N .; Earnshaw, Alan (1997). Chemistry of the Elements (2. vyd.). Butterworth-Heinemann . ISBN 978-0-08-037941-8 .
- R. Bruce King, vyd. (1994). „Kyselina chlorová“. Encyclopedia of Anorganic Chemistry . 2 . Chichester: Wiley. str. 658. ISBN 0-471-93620-0 .

