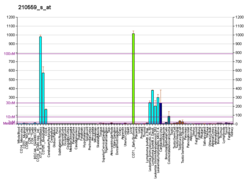
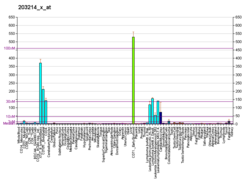
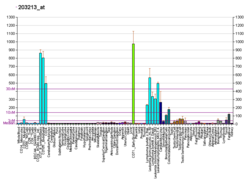
Cyklin -dependentní kináza 1 - Cyclin-dependent kinase 1
Cdk1 také známý jako CDK1 nebo cyklus proteinu buněčného dělení 2 homolog je vysoce konzervovaný protein, který působí jako serin / threonin kináza , a je klíčovým hráčem v buněčného cyklu regulace. Bylo velmi studována začínající kvasinek S. cerevisiae , a štěpení kvasinky S. pombe , kde je kódována geny CDC28 a cdc2 , v tomto pořadí. U lidí je Cdk1 kódován genem CDC2 . Se svými partnery pro cyklin vytváří Cdk1 komplexy, které fosforylují různé cílové substráty (v pučících kvasinkách bylo identifikováno více než 75); fosforylace těchto proteinů vede k progresi buněčného cyklu.
Struktura
Cdk1 je malý protein (přibližně 34 kilodaltonů) a je vysoce konzervovaný. Lidský homolog Cdk1, CDC2 , sdílí přibližně 63% identitu aminokyselin se svým kvasinkovým homologem. Kromě toho je lidský CDC2 schopen zachránit štěpné kvasinky nesoucí mutaci cdc2 . Cdk1 je tvořen převážně motivem holé protein kinázy, který sdílejí jiné protein kinázy. Cdk1, stejně jako ostatní kinázy, obsahuje rozštěp, do kterého se vejde ATP . Substráty Cdk1 se vážou v blízkosti ústí rozštěpu a zbytky Cdk1 katalyzují kovalentní vazbu y-fosfátu na kyslík hydroxylového serinu/threoninu substrátu.
Kromě tohoto katalytického jádra obsahuje Cdk1, stejně jako jiné cyklin-dependentní kinázy , T-smyčku, která v nepřítomnosti interagujícího cyklinu brání vazbě substrátu na aktivní místo Cdk1. Cdk1 také obsahuje šroubovici PSTAIRE, která se po vazbě na cyklin pohybuje a přeskupuje aktivní místo, což usnadňuje aktivity Cdk1 kinázy.
Funkce
Při navázání na své cyklinové partnery vede fosforylace Cdk1 k progresi buněčného cyklu. Aktivitu Cdk1 lze nejlépe pochopit u S. cerevisiae , takže zde je popsána aktivita Cdk1 S. cerevisiae .
U pučících kvasinek je počáteční vstup do buněčného cyklu řízen dvěma regulačními komplexy, SBF (SCB-binding factor) a MBF (MCB-binding factor). Tyto dva komplexy kontrolují transkripci genu G 1 /S; jsou však normálně neaktivní. SBF je inhibován proteinem Whi5 ; když je však fosforylován pomocí Cln3-Cdk1, Whi5 je ejekční z jádra, což umožňuje transkripci G 1 /S regulonu , který zahrnuje G 1 /S cyklinů Cln1,2. Aktivita G 1 /S cyklin-Cdk1 vede k přípravě na vstup do S fáze (např. Duplikace centromer nebo těla vřetenového pólu) a vzestup S cyklinů (Clb5,6 v S. cerevisiae ). Komplexy Clb5,6-Cdk1 přímo vedou k zahájení počátku replikace; jsou však inhibovány Sic1 , což brání předčasnému zahájení S fáze.
Aktivní aktivita Cln1,2 a/nebo Clb5,6-Cdk1 vede k náhlému poklesu hladin Sic1, což umožňuje koherentní vstup do S fáze. Nakonec fosforylace pomocí M cyklinů (např. Clb1, 2, 3 a 4) v komplexu s Cdk1 vede k sestavení vřetene a sesterskému chromatidovému vyrovnání. Fosforylace Cdk1 také vede k aktivaci ubikvitin-proteinové ligázy APC Cdc20 , aktivaci, která umožňuje segregaci chromatidů a dále degradaci cyklinů M-fáze. Tato destrukce M cyklinů vede ke konečným událostem mitózy (např. Demontáž vřetene, mitotický výstup).
Nařízení
Vzhledem ke své zásadní roli v progresi buněčného cyklu je Cdk1 vysoce regulován. Nejzjevnější je, že Cdk1 je regulován vazbou na své cyklinové partnery. Cyklinová vazba mění přístup k aktivnímu místu Cdk1, což umožňuje aktivitu Cdk1; kromě toho cykliny propůjčují specificitu aktivitě Cdk1. Alespoň některé cykliny obsahují hydrofobní náplast, která může přímo interagovat se substráty, což propůjčuje cílovou specificitu. Cykliny navíc mohou cílit Cdk1 na konkrétní subcelulární místa.
Kromě regulace cykliny je Cdk1 regulován také fosforylací. Konzervovaný tyrosin (Tyr15 u lidí) vede k inhibici Cdk1; předpokládá se, že tato fosforylace mění orientaci ATP a brání účinné kinázové aktivitě. Například v S. pombe může neúplná syntéza DNA vést ke stabilizaci této fosforylace, což brání mitotické progresi. Wee1 , konzervovaný mezi všemi eukaryoty, fosforyluje Tyr15, zatímco členy rodiny Cdc25 jsou fosfatázy, které působí proti této aktivitě. Předpokládá se, že rovnováha mezi nimi pomáhá řídit průběh buněčného cyklu. Wee1 je řízen proti proudu Cdr1, Cdr2 a Pom1 .
Komplexy Cdk1-cyklin jsou také řízeny přímou vazbou proteinů inhibitoru Cdk (CKI). Jeden takový protein, o kterém již byla řeč, je Sic1. Sic1 je stechiometrický inhibitor, který se váže přímo na komplexy Clb5,6-Cdk1. Předpokládá se, že multisite fosforylace pomocí Cdk1-Cln1/2 Sic1 načasuje ubikvitinaci a destrukci Sic1 a v širším smyslu načasování vstupu S-fáze. Pouze do doby, než bude překonána inhibice Sic1, může dojít k aktivitě Clb5,6 a může začít iniciace S fáze.
Interakce
Bylo ukázáno, že Cdk1 interaguje s:
Viz také
Mastl
Reference
Další čtení
- Draetta G, Eckstein J (1997). „Cdc25 protein fosfatázy v buněčné proliferaci“. Biochim. Biofy. Acta . 1332 (2): M53–63. doi : 10,1016/S0304-419X (96) 00049-2 . PMID 9141461 .
- Kino T, Pavlakis GN (2004). „Partnerské molekuly pomocného proteinu Vpr viru lidské imunodeficience typu 1“ . DNA Cell Biol . 23 (4): 193–205. doi : 10,1089/104454904773819789 . PMID 15142377 .
- Kino T, Chrousos GP (2004). "Doplňkový protein Vpr viru lidské imunodeficience typu 1: původce syndromu inzulínové rezistence/lipodystrofie související s AIDS?" . Ann. NY Acad. Sci . 1024 (1): 153–167. Bibcode : 2004NYASA1024..153K . doi : 10,1196/anály.1321.013 . PMID 15265780 . S2CID 23655886 .
- Zhao LJ, Zhu H (2005). „Struktura a funkce pomocného regulačního proteinu Vpr HIV-1: nové vodítka k designu léčiv“. Curr. Drug Targets Immune Endocr. Metabol. Disord . 4 (4): 265–275. doi : 10,2174/1568008043339668 . PMID 15578977 .
- Le Rouzic E, Benichou S (2006). „Vpr protein z HIV-1: odlišné role v průběhu životního cyklu viru“ . Retrovirologie . 2 : 11. doi : 10,1186/1742-4690-2-11 . PMC 554975 . PMID 15725353 .
- Zhao RY, Elder RT (2005). „Virové infekce a regulace G2/M buněčného cyklu“ . Cell Res . 15 (3): 143–149. doi : 10,1038/sj.cr.7290279 . PMID 15780175 .
- Zhao RY, Bukrinsky M, Elder RT (2005). „HIV-1 virový protein R (Vpr) a hostitelské buněčné odpovědi“. Indián J. Med. Res . 121 (4): 270–86. PMID 15817944 .
- Kaldis P, Aleem E (2007). „Souboj sourozenců buněčného cyklu: Cdc2 vs. Cdk2“ . Buněčný cyklus . 4 (11): 1491–1494. doi : 10,4161/cc.4.11.2124 . PMID 16258277 .
- Li L, Li HS, Pauza CD, Bukrinsky M, Zhao RY (2006). „Role pomocných proteinů HIV-1 ve virové patogenezi a interakcích hostitel-patogen“ . Cell Res . 15 (11–12): 923–934. doi : 10,1038/sj.cr.7290370 . PMID 16354571 .
- Rietbrock N, Keller F (1977). „[Biologická dostupnost a efekt 1. průchodu léků]“. Fortschr. Med . 95 (28): 1765–6, 1774–80. PMID 914146 .
- Azzi L, Meijer L, Reed SI, Pidikiti R, Tung HY (1992). "Interakce mezi proteiny kontrolujícími buněčný cyklus p34cdc2 a p9CKShs2. Důkaz pro dvě spolupracující vazebné domény v p9CKShs2" . Eur. J. Biochem . 203 (3): 353–360. doi : 10.1111/j.1432-1033.1992.tb16557.x . PMID 1310466 .
- Dutta A, Stillman B (1992). „kinázy rodiny cdc2 fosforylují replikační faktor DNA lidských buněk RPA a aktivují replikaci DNA“ . EMBO J . 11 (6): 2189–99. doi : 10.1002/j.1460-2075.1992.tb05278.x . PMC 556686 . PMID 1318195 .
- Koff A, Giordano A, Desai D, Yamashita K, Harper JW, Elledge S, Nishimoto T, Morgan DO, Franza BR, Roberts JM (1992). „Tvorba a aktivace cyklinového komplexu E-cdk2 během fáze G1 cyklu lidských buněk“. Věda . 257 (5077): 1689–1694. Bibcode : 1992Sci ... 257.1689K . doi : 10,1126/věda.1388288 . PMID 1388288 .
- Russo GL, Vandenberg MT, Yu IJ, Bae YS, Franza BR, Marshak DR (1992). „Kasein kináza II fosforyluje p34cdc2 kinázu ve fázi G1 cyklu dělení buněk HeLa“ . J. Biol. Chem . 267 (28): 20317–25. doi : 10,1016/S0021-9258 (19) 88704-5 . PMID 1400350 .
- Rubinfeld B, Crosier WJ, Albert I, Conroy L, Clark R, McCormick F, Polakis P (1992). „Lokalizace katalytické domény rap1GAP a míst fosforylace mutační analýzou“ . Mol. Buňka. Biol . 12 (10): 4634–42. doi : 10.1128/MCB.12.10.4634 . PMC 360390 . PMID 1406653 .
- van der Sluijs P, Hull M, Huber LA, Mâle P, Goud B, Mellman I (1992). „Reverzibilní fosforylace-defosforylace určuje lokalizaci rab4 během buněčného cyklu“ . EMBO J . 11 (12): 4379–89. doi : 10.1002/j.1460-2075.1992.tb05538.x . PMC 557012 . PMID 1425574 .
- Seth A, Alvarez E, Gupta S, Davis RJ (1992). „Fosforylační místo umístěné v NH2-koncové doméně c-Myc zvyšuje transaktivaci genové exprese“ . J. Biol. Chem . 266 (35): 23521–4. doi : 10,1016/S0021-9258 (18) 54312-X . PMID 1748630 .
- Lees JA, Buchkovich KJ, Marshak DR, Anderson CW, Harlow E (1992). „Retinoblastomový protein je fosforylován na více místech lidským cdc2“ . EMBO J . 10 (13): 4279–90. doi : 10.1002/j.1460-2075.1991.tb05006.x . PMC 453181 . PMID 1756735 .
- Nazarenko SA, Ostroverhova NV, Spurr NK (1991). „Regionální přiřazení řídícího genu CDC2 lidského buněčného cyklu chromozomu 10q21 hybridizací in situ“. Hučení. Genet . 87 (5): 621–2. doi : 10,1007/BF00209025 . PMID 1916766 . S2CID 25673088 .
- Nissen MS, Langan TA, Reeves R (1991). „Fosforylace pomocí cdc2 kinázy moduluje vazebnou aktivitu DNA vysokohistaminového chromatinového proteinu skupiny I“ . J. Biol. Chem . 266 (30): 19945–52. doi : 10,1016/S0021-9258 (18) 54874-2 . PMID 1939057 .