Dehydratační reakce - Dehydration reaction
V chemii je dehydratační reakce (neboli kondenzační reakce ), známá také jako Zimmerova hydrogeneze , přeměna, která zahrnuje ztrátu vody z reagující molekuly nebo iontu. Dehydratační reakce jsou běžné procesy, opak hydratační reakce . Mezi běžná dehydratační činidla používaná při organické syntéze patří kyselina sírová a oxid hlinitý . Dehydratační reakce se často provádějí zahříváním.
Dehydratační reakce
Klasickým příkladem dehydratační reakce je Fischerova esterifikace , která zahrnuje zpracování karboxylové kyseliny alkoholem v přítomnosti dehydratačního činidla:
- RCO 2 H + R'OH ⇌ RCO 2 R ′ + H 2 O
Dva monosacharidy , jako je glukóza a fruktóza , lze spojit dohromady (za vzniku sacharózy ) pomocí dehydratační syntézy. Nová molekula, skládající se ze dvou monosacharidů, se nazývá disacharid .
Proces hydrolýzy je reverzní reakcí, což znamená, že voda se rekombinuje se dvěma hydroxylovými skupinami a disacharid se vrací k monosacharidům.
Při související kondenzační reakci se voda uvolňuje ze dvou různých reaktantů.
V organické syntéze existuje mnoho příkladů dehydratační reakce, například dehydratace alkoholů nebo cukrů.
| Reakce | Obecná rovnice | Příklady |
|---|---|---|
| Konverze dvou alkoholů na ether ( substituce ) | 2 R – OH → R – O – R + H 2 O | |
| Konverze kyseliny a alkoholu na ester ( Fischer-Speierova esterifikace ) | R-COOH + R'-OH → R-COO-R‘+ H 2 O 
|
|
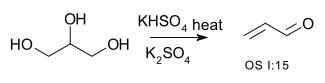
| Přeměna alkoholu na alken ( eliminace ) | R-CH 2- CHOH-R → R-CH = CH-R + H 2 O | například přeměna glycerolu na akrolein :
nebo dehydratace 2-methyl-cyklohexan-1-olu na (hlavně) 1-methylcyklohexen , za použití Martinova siru Konverze ethanolu na eten
|
| Konverze dvou karboxylových kyselin s acylanhydrid | 2 RCOOH → (RCO) 2 O + H 2 O | |
| Konverze amidu na nitril | RCONH 2 → R – CN + H 2 O | |
| Dienol – benzenové přesmyky |
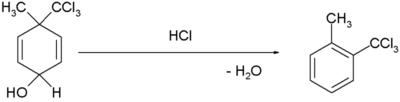
|
Dalšími příklady reakcí dehydratační syntézy jsou tvorba triglyceridů z mastných kyselin a tvorba glykosidových vazeb mezi molekulami sacharidů, jako je tvorba maltózy ze dvou molekul glukózy.