Hydrazin - Hydrazine
|
|
|||
|
|
|||
 Hydrazinový hydrát
|
|||
| Jména | |||
|---|---|---|---|
|
Systematický název IUPAC
Hydrazin |
|||
| Ostatní jména
Diamant; Diazane; Tetrahydridodinitrogen ( N - N ); diamidogen
|
|||
| Identifikátory | |||
|
3D model ( JSmol )
|
|||
| 3DMet | |||
| 878137 | |||
| ČEBI | |||
| CHEMBL | |||
| ChemSpider | |||
| Informační karta ECHA |
100,005,560 |
||
| Číslo ES | |||
| 190 | |||
| KEGG | |||
| Pletivo | Hydrazin | ||
|
PubChem CID
|
|||
| Číslo RTECS | |||
| UNII | |||
| UN číslo | 2029 | ||
|
CompTox Dashboard ( EPA )
|
|||
|
|||
|
|||
| Vlastnosti | |||
|
N. 2H 4 |
|||
| Molární hmotnost | 32,0452 g · mol −1 | ||
| Vzhled | Bezbarvá, dýmavá, olejovitá kapalina | ||
| Zápach | amoniak -like | ||
| Hustota | 1,021 g · cm −3 | ||
| Bod tání | 2 ° C; 35 ° F; 275 K. | ||
| Bod varu | 114 ° C; 237 ° F; 387 K. | ||
| Mísitelné | |||
| log P | 0,67 | ||
| Tlak páry | 1 kPa (při 30,7 ° C) | ||
| Kyselost (p K a ) | 8,10 (N 2 H 5 + ) | ||
| Bazicita (p K b ) | 5,90 | ||
| Konjugovaná kyselina | Hydrazinium | ||
|
Index lomu ( n D )
|
1,46044 (při 22 ° C) | ||
| Viskozita | 0,876 cP | ||
| Struktura | |||
| Trojúhelníkový pyramidový na N. | |||
| 1,85 D | |||
| Termochemie | |||
|
Standardní molární
entropie ( S |
121,52 J · K −1 · mol −1 | ||
|
Standardní entalpie
tvorby (Δ f H ⦵ 298 ) |
50,63 kJ · mol −1 | ||
| Nebezpečí | |||
| Bezpečnostní list | ICSC 0281 | ||
| Piktogramy GHS |
    
|
||
| Signální slovo GHS | Nebezpečí | ||
| H226 , H301 , H311 , H314 , H317 , H331 , H350 , H410 | |||
| P201 , P261 , P273 , P280 , P301+310 , P305+351+338 | |||
| NFPA 704 (ohnivý diamant) | |||
| Bod vzplanutí | 52 ° C (126 ° F; 325 K) | ||
| 24 až 270 ° C (75 až 518 ° F; 297 až 543 K) | |||
| Výbušné limity | 1,8–99,99% | ||
| Smrtelná dávka nebo koncentrace (LD, LC): | |||
|
LD 50 ( střední dávka )
|
59–60 mg/kg (orálně u potkanů, myší) | ||
|
LC 50 ( střední koncentrace )
|
260 ppm (krysa, 4 hodiny) 630 ppm (krysa, 1 hodina) 570 ppm (krysa, 4 hodiny) 252 ppm (myš, 4 hodiny) |
||
| NIOSH (limity expozice USA pro zdraví): | |||
|
PEL (přípustné)
|
PEL 1 ppm (1,3 mg/m 3 ) [kůže] | ||
|
REL (doporučeno)
|
Ca C 0,03 ppm (0,04 mg/m 3 ) [2 hodiny] | ||
|
IDLH (bezprostřední nebezpečí)
|
Ca [50 ppm] | ||
| Související sloučeniny | |||
|
Jiné anionty
|
Tetrafluorohydrazin Peroxid vodíku Diphosphane Difosforečnan tetrojodid |
||
|
Jiné kationty
|
Organické hydraziny | ||
|
Související binární azany
|
Amoniak Triazane |
||
|
Související sloučeniny
|
Diazene triazen tetrazen Diphosphene |
||
|
Pokud není uvedeno jinak, jsou údaje uvedeny pro materiály ve standardním stavu (při 25 ° C [77 ° F], 100 kPa). |
|||
|
|
|||
| Reference na infobox | |||
Hydrazin je anorganická sloučenina s chemickým vzorcem N
2H
4. Je to jednoduchý hydrid pniktogenu a je to bezbarvá hořlavá kapalina se zápachem podobným amoniaku .
Hydrazin je vysoce toxický, pokud s ním není zacházeno v roztoku, například jako hydrazinový hydrát ( NH
2NH
2 · XH
2O ). V roce 2015 dosáhl světový trh s hydrazinhydrátem 350 milionů dolarů. Hydrazin se používá hlavně jako nadouvadla při přípravě polymerní pěny , ale aplikace také zahrnují jeho použití jako prekurzor na polymeračních katalyzátorů , léčiv a agrochemikálií, jakož i dlouhodobou skladovatelný hnacího prostředku pro in- space kosmické pohonu.
V roce 2015 byly do nadouvadel pěny použity asi dva miliony tun hydrazinhydrátu. Hydrazin se navíc používá v různých raketových palivech a k přípravě plynových prekurzorů používaných ve vzduchových vakech . Hydrazin se používá v parních cyklech jaderných i konvenčních elektráren jako zachycovač kyslíku k řízení koncentrací rozpuštěného kyslíku ve snaze snížit korozi.
Hydraziny označují třídu organických látek odvozených nahrazením jednoho nebo více atomů vodíku v hydrazinu organickou skupinou.
Využití
Producenti plynu a pohonné hmoty
Většina hydrazinu se používá jako prekurzor nadouvadel . Mezi specifické sloučeniny patří azodikarbonamid a azobisizobutyronitril , které produkují 100–200 ml plynu na gram prekurzoru. V související aplikaci se azid sodný , činidlo vytvářející plyn ve vzduchových vakech , vyrábí z hydrazinu reakcí s dusitanem sodným .
Hydrazin se také používá jako dlouhodobě skladovatelný pohonný plyn na palubě vesmírných vozidel, jako je mise Dawn do Ceres a Vesta, a jednak ke snížení koncentrace rozpuštěného kyslíku ve vodě a také k regulaci pH vody používané ve velkých průmyslových kotlích. F-16 stíhačka, Eurofighter Typhoon , Space Shuttle , a U-2 špionážní letadlo použití hydrazinu na pohonné hmoty jejich pomocné energetické jednotky .
Předchůdce pesticidů a léčiv
Hydrazin je předchůdcem několika léčiv a pesticidů. Tyto aplikace často zahrnují konverzi hydrazinu na heterocyklické kruhy, jako jsou pyrazoly a pyridaziny . Mezi příklady komerčně dostupných bioaktivních derivátů hydrazinu patří cefazolin , rizatriptan , anastrozol , flukonazol , metazachlor , metamitron , metribuzin , paclobutrazol , diclobutrazol , propiconazol , hydrazinsulfát , diimid , triadimefon a dibenzoylhydrazin .
Hydrazinové sloučeniny mohou být účinné jako aktivní složky ve směsi s jinými zemědělskými chemikáliemi nebo v kombinaci s nimi, jako jsou insekticidy, miticidy, nematocidy, fungicidy, antivirová činidla, atraktanty, herbicidy nebo regulátory růstu rostlin.
Drobné, specializované a výzkumné
Italský výrobce katalyzátorů Acta (chemická společnost) navrhl použití hydrazinu jako alternativy k vodíku v palivových článcích . Hlavní výhodou použití hydrazinu je, že se může vyrábět více než 200 m W / cm 2 více než podobné vodíku buňky bez nutnosti použití drahých platinových katalyzátorů. Protože je palivo při pokojové teplotě kapalné, lze s ním manipulovat a skladovat ho snáze než s vodíkem. Uložením hydrazinu do nádrže plné dvojné vazby uhlík - kyslíkový karbonyl palivo reaguje a vytváří bezpečnou pevnou látku zvanou hydrazon . Poté propláchnutím nádrže teplou vodou se uvolní kapalný hydrazinový hydrát. Hydrazin má vyšší elektromotorickou sílu 1,56 V oproti 1,23 V u vodíku. Hydrazin se v buňce rozkládá za vzniku dusíku a vodíku, který se váže s kyslíkem a uvolňuje vodu. Hydrazin byl použit v palivových článcích vyráběných společností Allis-Chalmers Corp. , včetně těch, které v šedesátých letech zajišťovaly elektrickou energii ve vesmírných satelitech.
Směs 63% hydrazinu, 32% dusičnanu hydrazinu a 5% vody je standardním hnacím plynem pro experimentální dělostřelectvo s kapalným pohonem . Hnací směs výše je jednou z nejpředvídatelnějších a nejstabilnějších, s plochým tlakovým profilem během střelby. Selhání zapalování je obvykle způsobeno nedostatečným zapalováním. Pohyb skořepiny po nesprávném zapálení způsobuje velkou bublinu s větší plochou zapalovacího povrchu a vyšší rychlost produkce plynu způsobuje velmi vysoký tlak, někdy včetně katastrofických poruch trubek (tj. Výbuchů). Od ledna do června 1991 prováděla americká armádní výzkumná laboratoř přezkum raných programů velkoobjemových pistolí na kapalné palivo, které by mohly být relevantní pro program elektrotepelného chemického pohonu.
United States Air Force (USAF) pravidelně využívá H-70, 70% hydrazin 30% směsi s vodou, do operací používajících General Dynamics F-16 „Fighting Falcon“ stíhací letouny a Lockheed U-2 „Dragon Lady“ průzkumná letadla . Jednosměrný motor F-16 využívá hydrazin k napájení své nouzové napájecí jednotky (EPU), která poskytuje nouzovou elektrickou a hydraulickou energii v případě zhasnutí plamene motoru. EPU se aktivuje automaticky nebo ručně pilotním řízením v případě ztráty hydraulického tlaku nebo elektrické energie za účelem zajištění nouzového řízení letu. Jednosměrný motor U-2 využívá hydrazin k napájení svého systému nouzového startování (ESS), který poskytuje vysoce spolehlivý způsob restartování motoru za letu v případě zastavení.
Raketové palivo

Hydrazin byl poprvé použit jako součást raketových paliv během druhé světové války . 30% hmotnostní směs s 57% methanolu ( v německé Luftwaffe pojmenovaná M-Stoff ) a 13% vody nazývali Němci C-Stoff . Směs byla použita k pohonu stíhacího letounu s raketovým pohonem Messerschmitt Me 163B , ve kterém byl jako oxidant použit německý vysoce testovaný peroxid T-Stoff . Nemíchaný hydrazin byl Němci označován jako B-Stoff , toto označení bylo také později použito pro palivo ethanol/voda pro raketu V-2 .
Hydrazin se používá jako nízkoenergetický monopropelent pro manévrovací rakety kosmických lodí a byl používán k pohonu pomocných energetických jednotek (APU) raketoplánu . Kromě toho se v koncovém sestupu kosmických lodí často používají raketové motory s jedním pohonem s hydrazinovým pohonem. Takové motory byly použity na přistávacích programech Vikingů v 70. letech minulého století, stejně jako na Marsu Lounge Phoenix (květen 2008), Curiosity (srpen 2012) a Perseverance (únor 2021).
U všech hydrazinových jednopalivových motorů je hydrazin veden přes katalyzátor, jako je iridiový kov nesený oxidem hlinitým s vysokým povrchem , což způsobuje, že se rozkládá na amoniak , plynný dusík a plynný vodík podle následujícího reakce:
První dvě reakce jsou extrémně exotermické (katalyzátorová komora může dosáhnout 800 ° C během několika milisekund) a produkují velké objemy horkého plynu z malého objemu kapaliny, což z hydrazinu dělá poměrně účinný propulzní pohon s impulsem specifickým pro vakuum asi 220 sekund. Reakce 2 je nejvíce exotermická, ale produkuje menší počet molekul než reakce 1. Reakce 3 je endotermická a vrací účinek reakce 2 zpět na stejný účinek jako samotná reakce 1 (nižší teplota, větší počet molekul). Struktura katalyzátoru má vliv na podíl NH 3 , která disociuje v reakci 3; vyšší teplota je žádoucí pro raketové rakety, zatímco více molekul je žádoucí, když reakce mají produkovat větší množství plynu.
Protože je hydrazin pevnou látkou pod 2 ° C, není vhodný jako univerzální raketový pohon pro vojenské aplikace. Další varianty hydrazinu , které se používají jako palivo pro rakety jsou monomethylhydrazinu , (CH 3 ), NH (NH 2 ), také známý jako MMH (teplota tání: -52 ° C), a nesymetrického dimethylhydrazinu , (CH 3 ) 2, N (NH 2 ) , také známý jako UDMH (mp: -57 ° C). Tyto deriváty se používají ve dvousložkových raketových palivech, často společně s oxidem dusičitým , N 2 O 4 . Směs hydrazinu a UDMA v poměru 50:50 byla použita v ICBM Titan II a je známá jako Aerozine 50 . Tyto reakce jsou extrémně exotermické a pálení je také hypergolické (začíná hořet bez jakéhokoli vnějšího vznícení).
V leteckém průmyslu pokračují snahy nahradit hydrazin a další vysoce toxické látky. Mezi slibné alternativy patří hydroxylamoniumnitrát , 2-dimethylaminoethylazid (DMAZ) a energetické iontové kapaliny.
Pracovní rizika
Zdravé efekty
Potenciální cesty expozice hydrazinu zahrnují dermální, oční, vdechnutí a požití.
Expozice hydrazinu může způsobit podráždění kůže/kontaktní dermatitidu a pálení, podráždění očí/nosu/hrdla, nevolnost/zvracení, dušnost, plicní edém, bolest hlavy, závratě, deprese centrálního nervového systému, letargii, dočasnou slepotu, záchvaty a kóma. Expozice může také způsobit poškození orgánů jater, ledvin a centrálního nervového systému. Hydrazin je dokumentován jako silný senzibilizátor kůže s potenciálem pro křížovou senzibilizaci na deriváty hydrazinu po počáteční expozici. Kromě výše uvedených profesních použití je expozice hydrazinu možná také v malých množstvích z tabákového kouře.
Oficiální pokyny USA k hydrazinu jako karcinogenu jsou smíšené, ale obecně existují potenciální účinky způsobující rakovinu. Národní institut pro bezpečnost a ochranu zdraví (NIOSH) uvádí jako „potenciální profesní karcinogen“. Národní toxikologický program (NTP) shledává, že se „důvodně předpokládá, že je lidským karcinogenem“. Americká konference vládních průmyslových hygieniků (ACGIH) stupně hydrazin jako „A3-potvrzený karcinogen na zvířatech s neznámou relevancí pro člověka“. Americká agentura pro ochranu životního prostředí (EPA) jej klasifikuje jako „B2 - pravděpodobný lidský karcinogen na základě důkazů ze studií na zvířatech“.
Mezinárodní agentura pro výzkum rakoviny (IARC) hodnotí hydrazin jako „2A - pravděpodobně karcinogenní pro člověka“ s pozitivní asociací pozorovanou mezi expozicí hydrazinu a rakovinou plic. Na základě kohortních a průřezových studií expozice hydrazinu z povolání dospěl výbor z Národních akademií věd , inženýrství a lékařství k závěru, že existují sugestivní důkazy o souvislosti mezi expozicí hydrazinu a rakovinou plic, s nedostatečným důkazem asociace s rakovinou u jiných stránky. Evropská komise je Vědecký výbor pro limity expozice při práci (SCOEL) umístí hydrazinu ve karcinogen ‚skupina B-genotoxický karcinogen‘. Genotoxický mechanismus, který výbor citoval, se týká reakce hydrazinu s endogenním formaldehydem a tvorbou DNA-methylačního činidla.
V případě mimořádné situace související s expozicí hydrazinu NIOSH doporučuje okamžitě odstranit kontaminovaný oděv, umýt kůži mýdlem a vodou a pro expozici očí odstranit kontaktní čočky a vyplachovat oči vodou po dobu nejméně 15 minut. NIOSH také doporučuje každému, kdo má potenciální expozici hydrazinu, aby co nejdříve vyhledal lékařskou pomoc. Neexistují žádná specifická doporučení pro laboratorní nebo lékařské zobrazování po expozici a lékařské vyšetření může záviset na typu a závažnosti symptomů. Světová zdravotnická organizace (WHO) doporučuje potenciální expozice lze léčit symptomaticky se zvláštním zřetelem k potenciálním plic a poškození jater. Dřívější případy expozice hydrazinu dokumentují úspěch léčby pyridoxinem (vitamín B6) .
Mezní hodnoty expozice na pracovišti
- Doporučený expoziční limit NIOSH (REL): 0,03 ppm (0,04 mg/m 3 ) 2hodinový strop
- Přípustný expoziční limit OSHA (PEL): 1 ppm (1,3 mg/m 3 ) 8hodinový časově vážený průměr
- Mezní hodnota ACGIH (TLV): 0,01 ppm (0,013 mg/m 3 ) 8hodinový časově vážený průměr
Prahová hodnota zápachu pro hydrazin je 3,7 ppm, takže pokud je pracovník schopen cítit zápach podobný amoniaku, pravděpodobně překračuje expoziční limit. Tato prahová hodnota zápachu se však velmi liší a neměla by být používána ke stanovení potenciálně nebezpečných expozic.
Pro letecký a kosmický personál USAF používá pokyny pro nouzové ozáření, vyvinuté Výborem pro toxikologii Národní akademie věd , které se používají pro nerutinní expozice široké veřejnosti a nazývají se pokyny pro krátkodobé veřejné nouzové expozice (SPEGL). SPEGL, který se nevztahuje na pracovní expozice, je definován jako přijatelná maximální koncentrace pro nepředvídatelné, jednorázové, krátkodobé nouzové expozice široké veřejnosti a představuje vzácné expozice za celý život pracovníka. U hydrazinu je 1hodinový SPEGL 2 ppm, s 24hodinovým SPEGL 0,08 ppm.
Manipulace a lékařský dohled
Kompletní sledovací program pro hydrazin by měl zahrnovat systematickou analýzu biologického monitorování, lékařský screening a informace o morbiditě/mortalitě. CDC doporučuje souhrny dozoru a vzdělávání být pro orgány dohledu a pracovníků. Před umístěním a periodický lékařský screening by měl být prováděn se zvláštním zaměřením na potenciální účinky hydrazinu na fungování očí, kůže, jater, ledvin, krvetvorného, nervového a dýchacího systému.
Mezi běžné ovládací prvky používané pro hydrazin patří procesní kryt, místní odsávací ventilace a osobní ochranné prostředky (OOP). Pokyny pro hydrazinový OOP zahrnují nepropustné rukavice a oděv, brýle odolné proti stříkající vodě, obličejový štít a v některých případech i respirátor. Použití respirátorů pro manipulaci s hydrazinem by mělo být krajním řešením jako metoda kontroly expozice pracovníků. V případech, kdy jsou zapotřebí respirátory, by měl být zaveden správný výběr respirátoru a kompletní program ochrany dýchacích cest v souladu se směrnicemi OSHA .
Pokud jde o personál USAF , standard 48-8 pro bezpečnost a ochranu zdraví letectva (AFOSH), standard 48-8, dodatek 8 hodnotí úvahy o pracovním vystavení hydrazinu v systémech raket, letadel a kosmických lodí. Specifické pokyny pro reakci na expozici zahrnují povinné nouzové sprchové a výplachové stanice a postup pro dekontaminaci ochranného oděvu. Pokyny také stanoví povinnosti a požadavky na řádné OOPP, školení zaměstnanců, lékařský dohled a reakci na mimořádné události. Základny USAF vyžadující použití hydrazinu mají obecně specifické základní předpisy upravující místní požadavky na bezpečné používání hydrazinu a reakci na mimořádné události.
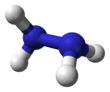
Molekulární struktura
Každá podjednotka H 2 N - N je pyramidová. Vzdálenost jednoduché vazby N -N je 1,45 Á (145 pm ) a molekula přijímá Gauchovu konformaci . Rotační bariéra je dvakrát větší než ethan . Tyto strukturní vlastnosti připomínají vlastnosti plynného peroxidu vodíku , který přijímá „šikmou“ antiklinální konformaci a také zažívá silnou rotační bariéru.
Syntéza a výroba
Byly vyvinuty rozmanité trasy. Klíčovým krokem je vytvoření jednoduché vazby dusík -dusík. Mnoho cest lze rozdělit na ty, které používají oxidační činidla na bázi chloru (a vytvářejí sůl) a ty, které je nepoužívají.
Oxidace amoniaku prostřednictvím oxaziridinů z peroxidu
Hydrazin lze syntetizovat z amoniaku a peroxidu vodíku pomocí ketonového katalyzátoru v postupu zvaném Peroxidový proces (někdy nazývaný Pechiney-Ugine-Kuhlmannův proces, cyklus Atofina-PCUK nebo ketazinový proces). Následuje čistá reakce:
Při této cestě keton a amoniak nejprve kondenzují za vzniku iminu , který je oxidován peroxidem vodíku na oxaziridin , tříčlenný kruh obsahující uhlík, kyslík a dusík. Dále oxaziridinu poskytuje hydrazon o působením amoniaku , přičemž tento způsob vytváří dusík-dusík jednoduchou vazbu. Tento hydrazon kondenzuje s dalším ekvivalentem ketonu.
Výsledný azin se hydrolyzuje za vzniku hydrazinu a regeneruje keton, methylethylketon :
Na rozdíl od většiny ostatních procesů tento přístup neprodukuje sůl jako vedlejší produkt.
Oxidace na bázi chloru
Proces Olin Raschig , poprvé oznámený v roce 1907, produkuje hydrazin z chlornanu sodného (aktivní složka mnoha bělidel ) a amoniaku bez použití ketonového katalyzátoru. Tato metoda se opírá o reakci monochloraminu s amoniakem za vzniku jednoduché vazby dusík -dusík a vedlejšího produktu chlorovodíku :
V souvislosti s Raschigovým procesem lze močovinu oxidovat místo amoniaku. Jako oxidant opět slouží chlornan sodný. Zobrazí se čistá reakce:
Tento proces generuje významné vedlejší produkty a je praktikován hlavně v Asii.
Bayer Ketazine proces je předchůdce pro proces peroxidu. Místo peroxidu vodíku používá jako okysličovadlo chlornan sodný. Jako všechny cesty na bázi chlornanu, tato metoda produkuje ekvivalent soli pro každý ekvivalent hydrazinu.
Reakce
Acidobazické chování
Hydrazin tvoří monohydrát , který má větší hustotu (1,032 g / cm 3 ), než je bezvodého materiálu. Hydrazin má základní ( alkalické ) chemické vlastnosti srovnatelné s vlastnostmi amoniaku :
(pro čpavek )
Je obtížné diprotonovat:
Redoxní reakce
Spalné teplo hydrazinu v kyslíku (vzduchu) je 1,941 x 10 7 J / kg (8345 BTU / lb).
Hydrazin je vhodný redukční prostředek, protože vedlejšími produkty jsou obvykle plynný dusík a voda. Používá se tedy jako antioxidant , pohlcovač kyslíku a inhibitor koroze ve vodních kotlích a topných systémech. Také se používá ke snížení kovové soli a oxidy na čisté kovy v electroless niklu pokovování a plutonia extrakce z odpadu jaderných reaktorů . Některé barevné fotografické postupy také používají slabý roztok hydrazinu jako stabilizační promývací prostředek, protože zachycuje vazebnou látku barviva a nezreagované halogenidy stříbra. Hydrazin je nejběžnějším a nejúčinnějším redukčním činidlem používaným k převodu oxidu grafenu (GO) na redukovaný oxid grafenu (rGO) prostřednictvím hydrotermálního zpracování.
Hydraziniové soli
Hydrazin lze mono -protonovat za vzniku různých pevných solí hydraziniového kationtu (N 2 H 5 + ) zpracováním s minerálními kyselinami. Běžnou solí je hydrazinium sulfát , [N 2 H 5 ] HSO 4 , také nazývaný hydrazin sulfát. Hydrazin sulfát byl zkoumán jako léčba kachexie vyvolané rakovinou , ale ukázal se jako neúčinný.
Double protonace dává hydrazinium dication (H 3 NNH 3 2+ ), které jsou známy různé soli.
Organická chemie
Hydraziny jsou součástí mnoha organických syntéz , často těch, které mají praktický význam ve farmaceutikách (viz část aplikace), jakož i v barvách na textil a ve fotografii.
Hydrazin se používá při Wolff-Kishnerově redukci , reakci, která transformuje karbonylovou skupinu ketonu na methylenový můstek (nebo aldehyd na methylovou skupinu ) prostřednictvím meziproduktu hydrazonu . Reakci napomáhá produkce vysoce stabilního dinitrogenu z hydrazinového derivátu.
Bifunkční se dvěma aminy je hydrazin klíčovým stavebním kamenem pro přípravu mnoha heterocyklických sloučenin kondenzací s řadou difunkčních elektrofilů . S 2,4-pentandionem kondenzuje za vzniku 3,5-dimethylpyrazolu . V Einhornově-Brunnerově reakci hydraziny reagují s imidy za vzniku triazolů .
Být dobrým nukleofilem, N 2 H 4 může napadat sulfonylhalogenidy a acylhalogenidy. Tosylhydrazine také tvoří hydrazonů po zpracování karbonylů.
Hydrazin se používá k štěpení N -alkylovaných derivátů ftalimidu. Tato štěpná reakce umožňuje použití ftalimidového aniontu jako prekurzoru aminu v Gabrielově syntéze .
Tvorba hydrazonu
Příkladem kondenzace hydrazinu s jednoduchým karbonylem je jeho reakce s propanonem za vzniku diisopropylidenhydrazinu (acetonazin). Ten reaguje dále s hydrazinem za vzniku hydrazonu:
Propanon azin je meziprodukt v procesu Atofina- PCUK . Přímá alkylace hydrazinů alkylhalogenidy v přítomnosti báze poskytuje alkyl-substituované hydraziny, ale reakce je obvykle neúčinná kvůli špatné kontrole úrovně substituce (stejné jako u běžných aminů ). Redukce hydrazonů na hydraziny představuje čistý způsob výroby 1,1-dialkylovaných hydrazinů.
V podobné reakci reagují 2-kyanopyridiny s hydrazinem za vzniku amidových hydrazidů, které lze pomocí 1,2-diketonů převést na triaziny .
Biochemie
Hydrazin je meziprodukt v procesu anaerobní oxidace amoniaku ( anammox ). Produkují ji některé kvasinky a otevřená oceánská bakterie anammox ( Brocadia anammoxidans ). Falešné Morel vytváří jed gyromitrin , kterou je organická derivát hydrazinu, který se převede na monomethylhydrazinu metabolickými procesy. I nejoblíbenější jedlá „houba“ z houby Agaricus bisporus produkuje organické deriváty hydrazinu, včetně agaritinu , hydrazinového derivátu aminokyseliny a gyromitrinu .
Dějiny
Název „hydrazin“ vytvořil Emil Fischer v roce 1875; zkoušel vyrábět organické sloučeniny, které sestávaly z monosubstituovaného hydrazinu. V roce 1887 vyrobil Theodor Curtius hydrazin sulfát zpracováním organických diazidů zředěnou kyselinou sírovou; přes opakované úsilí však nebyl schopen získat čistý hydrazin. Čistý bezvodý hydrazin poprvé připravil nizozemský chemik Lobry de Bruyn v roce 1895.
Viz také
- Diazene
- Hydrazin sulfát
- Seznam Stoffů
- Palivová směs z oxidu dusného - třída kapalných raketových pohonných hmot
- USA 193












![{\ displaystyle {\ ce {N2H4 + H2O -> [N2H5]^ + + OH-}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/ef02d7cc8519ded31bae36408d7f1461c64195b7)


![{\ displaystyle {\ ce {[N2H5] + + H2O -> [N2H6]^2 + + OH-}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/58d05df88d00c82f17bb6b59cf2a7d07696dc980)

![{\ displaystyle {\ ce {2 (CH3) 2CO + N2H4 -> 2 H2O + [(CH3) 2C = N] 2}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/8036d601adcf4a13ee6b912eb05bc55994ab952a)
![{\ displaystyle {\ ce {[(CH3) 2C = N] 2 + N2H4 -> 2 (CH3) 2C = NNH2}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/183b956f5ae1e22d5ada6e751b42ace50f85e25d)