Uhlovodík - Hydrocarbon
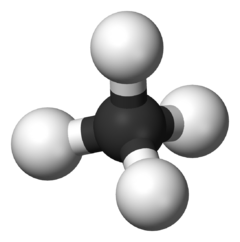
V organické chemii , je uhlovodík je organická sloučenina se skládá výhradně z vodíku a uhlíku . Uhlovodíky jsou příklady hydridů skupiny 14 . Uhlovodíky jsou obecně bezbarvé a hydrofobní se slabým zápachem. Vzhledem k jejich různorodým molekulárním strukturám je obtížné dále generalizovat. Většina antropogenních emisí uhlovodíků pochází ze spalování fosilních paliv, včetně výroby paliva a spalování. Přírodní zdroje uhlovodíků, jako je ethylen, isopren a monoterpeny, pocházejí z emisí vegetace.
Typy
Jak je definováno v nomenklatuře organické chemie IUPAC , klasifikace uhlovodíků jsou:
- Nasycené uhlovodíky jsou z uhlovodíkových druhů nejjednodušší. Skládají se výhradně z jednoduchých vazeb a jsou nasyceny vodíkem. Vzorec pro acyklické nasycené uhlovodíky (tj. Alkany ) je C n H 2 n +2 . Nejobecnější formou nasycených uhlovodíků je C n H 2 n +2 (1- r ) , kde r je počet kruhů. Ti s přesně jedním prstencem jsou cykloalkany . Nasycené uhlovodíky jsou základem ropných paliv a vyskytují se buď jako lineární nebo rozvětvené druhy. Substituční reakce je jejich charakteristickou vlastností (jako chlorační reakce za vzniku chloroformu ). Uhlovodíky se stejným molekulárním vzorcem, ale různými strukturními vzorci, se nazývají strukturní izomery . Jak je uvedeno v příkladu 3-methylhexanu a jeho vyšších homologů , rozvětvené uhlovodíky mohou být chirální . Chirální nasycené uhlovodíky tvoří postranní řetězce biomolekul, jako je chlorofyl a tokoferol .
- Nenasycené uhlovodíky mají jednu nebo více dvojných nebo trojných vazeb mezi atomy uhlíku. Ti s dvojnou vazbou se nazývají alkeny . Ti s jednou dvojnou vazbou mají vzorec C n H 2 n (za předpokladu necyklických struktur). Ty, které obsahují trojné vazby, se nazývají alkiny . Ti s jednou trojnou vazbou mají vzorec C n H 2 n −2 .
- Aromatické uhlovodíky , také známé jako areny , jsou uhlovodíky, které mají alespoň jeden aromatický kruh . 10% celkových emisí organického uhlíku bez methanu tvoří aromatické uhlovodíky z výfuků vozidel poháněných benzínem.
Uhlovodíky mohou být plyny (např. Metan a propan ), kapaliny (např. Hexan a benzen ), vosky nebo pevné látky s nízkou teplotou tání (např. Parafinový vosk a naftalen ) nebo polymery (např. Polyethylen , polypropylen a polystyren ).
Pojem „alifatický“ označuje nearomatické uhlovodíky. Nasycené alifatické uhlovodíky jsou někdy označovány jako „parafiny“. Alifatické uhlovodíky obsahující dvojnou vazbu mezi atomy uhlíku se někdy označují jako „olefiny“.
Jednoduché uhlovodíky a jejich variace
| Počet atomů uhlíku |
Alkane (jednoduchá vazba) | Alken (dvojná vazba) | Alkyne (trojná vazba) | Cykloalkan | Alkadien |
|---|---|---|---|---|---|
| 1 | Metan | - | - | - | - |
| 2 | Etan | Ethen (ethylen) | Ethyne (acetylen) | - | - |
| 3 | Propan | Propen (propylen) | Propyne (methylacetylen) | Cyklopropan | Propadien (allen) |
| 4 | Butan | Buten (butylen) | Butyne | Cyklobutan | Butadien |
| 5 | Pentan | Pentene | Pentyne | Cyklopentan | Pentadien (piperylen) |
| 6 | Hexan | Hexen | Hexyne | Cyklohexan | Hexadien |
| 7 | Heptan | Hepten | Heptyne | Cykloheptan | Heptadien |
| 8 | Oktan | Octene | Octyne | Cyklooktan | Oktadien |
| 9 | Nonane | Nonene | Nonyne | Cyklononan | Nonadien |
| 10 | Dekan | Decene | Decyne | Cyklodekan | Dekadien |
| 11 | Undecane | Undecene | Undecyne | Cycloundecane | Undecadiene |
| 12 | Dodekan | Dodecene | Dodecyne | Cyklododekan | Dodekadienu |
Používání

Převládající využití uhlovodíků je jako zdroj hořlavého paliva . Metan je převládající složkou zemního plynu. C 6 až C 10 alkanů, alkenů a izomerních cykloalkanů jsou hlavní složky benzínu , nafty , tryskového paliva a odborných průmyslových směsí rozpouštědel. S postupným přidáváním uhlíkových jednotek mají jednoduché nekruhové strukturované uhlovodíky vyšší viskozity , mazací indexy, teploty varu, teploty tuhnutí a hlubší barvu. V opačném extrému od metanu leží těžké dehty, které zůstávají jako nejnižší frakce v retortě rafinace ropy . Jsou shromažďovány a široce používány jako střešní krytiny, složení vozovek ( bitumen ), prostředky na ochranu dřeva ( řada kreosotů ) a jako kapaliny extrémně vysoké viskozity odolné proti smyku.
Některé rozsáhlé nepalivové aplikace uhlovodíků začínají etanem a propanem, které se získávají z ropy a zemního plynu. Tyto dva plyny se přeměňují buď na syngas, nebo na ethylen a propylen . Tyto dva alkeny jsou prekurzory polymerů, včetně polyethylenu , polystyrenu, akrylátů, polypropylenu atd. Další třídou speciálních uhlovodíků je BTX , směs benzenu , toluenu a tří xylenových izomerů . Globální spotřeba benzenu, odhadovaná na více než 40 000 000 tun (2009).
Uhlovodíky jsou také v přírodě převládající. Někteří eusociální členovci, jako například brazilská včela bez žihadla, Schwarziana quadripunctata , používají k určení příbuzenstva od příbuzenstva jedinečné uhlovodíkové „vůně“. Chemické složení uhlovodíků se liší podle věku, pohlaví, polohy hnízda a hierarchické polohy.
Existuje také potenciál pro těžbu uhlovodíků z rostlin, jako je Euphorbia lathyri a Euphorbia tirucalli, jako alternativní a obnovitelný zdroj energie pro vozidla využívající naftu. Kromě toho byly endofytické bakterie z rostlin, které přirozeně produkují uhlovodíky, použity při degradaci uhlovodíků ve snaze snížit koncentraci uhlovodíků ve znečištěných půdách.
Reakce
Pozoruhodnou vlastností uhlovodíků je jejich inertnost, zejména u nasycených členů. Jinak lze identifikovat tři hlavní typy reakcí:
Reakce volných radikálů
Substituční reakce se vyskytují pouze u nasycených uhlovodíků (jednoduché vazby uhlík -uhlík). Takové reakce vyžadují vysoce reaktivní činidla, jako je chlor a fluor . V případě chlorace jeden z atomů chloru nahrazuje atom vodíku. Reakce probíhají volnými radikály .
- CH 4 + Cl 2 → CH 3 Cl + HCl
- CH 3 Cl + Cl 2 → CH 2 Cl 2 + HCl
až do CCl 4 ( chlorid uhličitý )
- C 2 H 6 + Cl 2 → C 2 H 5 Cl + HCl
- C 2 H 4 Cl 2 + Cl 2 → C 2 H 3 Cl 3 + HCl
až do C 2 Cl 6 ( hexachloretan )
Střídání
Ze tříd uhlovodíků procházejí aromatické sloučeniny jedinečně (nebo téměř) substitučními reakcemi. Chemický postup praktikovaný v největším měřítku je příkladem: reakce benzenu a ethylenu za vzniku ethylbenzenu .
Adiční reakce
Adiční reakce platí pro alkeny a alkiny. V této reakci přidává řada činidel „přes“ pi-vazbu (y). Chlór, chlorovodík, voda a vodík jsou ilustrativními činidly. Alkeny a některé alkiny také procházejí polymerací , metenezí alkenu a metatezí alkinu .
Oxidace
Uhlovodíky jsou v současné době hlavním zdrojem světové elektrické energie a tepelných zdrojů (například vytápění domácností), protože energie vyrobená při jejich spalování je. Tato energie se často používá přímo jako teplo, například v domácích topidlech, která používají buď ropu, nebo zemní plyn . Uhlovodík se spálí a teplo se použije k ohřevu vody, která pak cirkuluje. Podobný princip se používá k výrobě elektrické energie v elektrárnách .
Společnými vlastnostmi uhlovodíků jsou skutečnosti, že při spalování produkují páru, oxid uhličitý a teplo a že ke spalování je zapotřebí kyslík . Nejjednodušší uhlovodík, metan , hoří následovně:
- CH 4 + 2 O 2 → 2 H 2 O + CO 2 + energie
Při nedostatečném přívodu vzduchu vzniká plynný oxid uhelnatý a vodní pára :
- 2 CH 4 + 3 O 2 → 2 CO + 4 H 2 O
Dalším příkladem je spalování propanu :
- C 3 H 8 + 5 O 2 → 4 H 2 O + 3 CO 2 + energie
A konečně, pro jakýkoli lineární alkan s n atomy uhlíku,
- C n H 2 n +2 + 3 n + 1/2 O 2 → ( n + 1) H 2 O + n CO 2 + energie.
Částečná oxidace charakterizuje reakce alkenů a kyslíku. Tento proces je základem žluknutí a sušení barvy .
Původ
Převážná většina uhlovodíků nacházejících se na Zemi se vyskytuje v ropě , ropě , uhlí a zemním plynu. Ropa (doslova „ropa“ - zkráceně benzín) a uhlí jsou obecně považovány za produkty rozkladu organické hmoty. Uhlí je na rozdíl od ropy bohatší na uhlík a chudší na vodík. Zemní plyn je produktem methanogeneze .
Zdánlivě neomezená řada sloučenin obsahuje ropu, a proto je nezbytná rafinerie. Tyto uhlovodíky se skládají z nasycených uhlovodíků, aromatických uhlovodíků nebo jejich kombinací. V ropě chybí alkeny a alkiny. Jejich výroba vyžaduje rafinerie. Uhlovodíky pocházející z ropy se spotřebovávají hlavně jako palivo, ale jsou také zdrojem prakticky všech syntetických organických sloučenin, včetně plastů a léčiv. Zemní plyn se spotřebovává téměř výhradně jako palivo. Uhlí se používá jako palivo a jako redukční činidlo v metalurgii .
Abiologické uhlovodíky
Malá část uhlovodíků nalezená na Zemi je považována za abiologickou .
Některé uhlovodíky jsou také rozšířené a hojné ve sluneční soustavě . Jezera tekutého metanu a ethanu byla nalezena na Titanu , největším Saturnově měsíci, potvrzeno misí Cassini-Huygens . Uhlovodíky jsou také bohaté na mlhoviny vytvářející polycyklické aromatické uhlovodíkové sloučeniny (PAH).
Bioremediace
Bioremediace uhlovodíků z půdy nebo vody kontaminované je impozantní výzvou kvůli chemické inertnosti, která charakterizuje uhlovodíky (proto přežily miliony let ve zdrojové hornině). Přesto bylo navrženo mnoho strategií, přičemž prominentní je bioremediace. Základním problémem bioremediace je nedostatek enzymů, které na ně působí. Přesto se této oblasti věnuje pravidelná pozornost. Bakterie v gabroické vrstvě oceánské kůry mohou degradovat uhlovodíky; ale extrémní prostředí ztěžuje výzkum. Jiné bakterie, jako je Lutibacterium anuloederans, mohou také degradovat uhlovodíky. Je možná mykoremediace nebo štěpení uhlovodíků myceliem a houbami .
Bezpečnost
Uhlovodíky mají obecně nízkou toxicitu, a proto je rozšířené používání benzínu a souvisejících těkavých produktů. Aromatické sloučeniny, jako je benzen, jsou narkotické a chronické toxiny a jsou karcinogenní . Některé vzácné polycyklické aromatické sloučeniny jsou karcinogenní. Uhlovodíky jsou vysoce hořlavé .
Zásah do životního prostředí
Spalování uhlovodíků jako paliva, které produkuje oxid uhličitý a vodu , je hlavním přispěvatelem k antropogennímu globálnímu oteplování . Uhlovodíky se zavádějí do životního prostředí jejich rozsáhlým používáním jako paliva a chemikálií, jakož i úniky nebo náhodným únikem během průzkumu, výroby, rafinace nebo přepravy fosilních paliv. Antropogenní kontaminace půdy uhlovodíky je vážným globálním problémem kvůli přetrvávání kontaminantů a negativnímu dopadu na lidské zdraví.
Pokud je půda kontaminována uhlovodíky, může to mít významný dopad na její mikrobiologické, chemické a fyzikální vlastnosti. To může sloužit k prevenci, zpomalení nebo dokonce zrychlení růstu vegetace v závislosti na přesných změnách, ke kterým dochází. Ropa a zemní plyn jsou dva největší zdroje uhlovodíkové kontaminace půdy.
Viz také
Reference
externí odkazy


