Lithiumaluminiumhydrid - Lithium aluminium hydride
|
|
|||

|
|||
| Jména | |||
|---|---|---|---|
|
Preferovaný název IUPAC
Lithium tetrahydridoaluminate (III) |
|||
|
Systematický název IUPAC
Lithium alumanuide |
|||
| Ostatní jména
Lithiumaluminiumhydrid
Lithal |
|||
| Identifikátory | |||
|
3D model ( JSmol )
|
|||
| Zkratky | LAH | ||
| ChEBI | |||
| ChemSpider | |||
| Informační karta ECHA |
100.037.146 |
||
| Číslo ES | |||
| 13167 | |||
|
PubChem CID
|
|||
| Číslo RTECS | |||
| UNII | |||
|
Řídicí panel CompTox ( EPA )
|
|||
|
|||
|
|||
| Vlastnosti | |||
| LiAlH 4 | |||
| Molární hmotnost | 37,95 g / mol | ||
| Vzhled | bílé krystaly (čisté vzorky), šedý prášek (komerční materiál), hygroskopický |
||
| Zápach | bez zápachu | ||
| Hustota | 0,917 g / cm 3 , pevný | ||
| Bod tání | 150 ° C (302 ° F; 423 K) (rozkládá se) | ||
| Reaguje | |||
| Rozpustnost v tetrahydrofuranu | 112,332 g / l | ||
| Rozpustnost v diethyletheru | 39,5 g / 100 ml | ||
| Struktura | |||
| monoklinický | |||
| P 2 1 / c | |||
| Termochemie | |||
|
Tepelná kapacita ( C )
|
86,4 J / mol K. | ||
|
Standardní molární
entropie ( S |
87,9 J / mol K. | ||
|
Std entalpie
formace (Δ f H ⦵ 298 ) |
-117 kJ / mol | ||
|
Gibbsova volná energie (Δ f G ˚)
|
-48,4 kJ / mol | ||
| Nebezpečí | |||
| Bezpečnostní list | Lithiumaluminiumhydrid | ||
| Piktogramy GHS |
 
|
||
| Signální slovo GHS | Nebezpečí | ||
| H260 , H314 | |||
| P223 , P231 + 232 , P280 , P305 + 351 + 338 , P370 + 378 , P422 | |||
| NFPA 704 (ohnivý diamant) | |||
| Bod vzplanutí | 125 ° C (257 ° F; 398 K) | ||
| Související sloučeniny | |||
|
Příbuzný hydrid
|
hydrid hlinitý borohydrid sodný hydrid sodný hydrid hlinitý sodný |
||
|
Pokud není uvedeno jinak, jsou uvedeny údaje pro materiály v jejich standardním stavu (při 25 ° C [77 ° F], 100 kPa). |
|||
|
|
|||
| Reference Infoboxu | |||
Lithiumaluminiumhydrid , obyčejně zkrátil na LAH , je anorganická sloučenina s chemickým vzorcem Li Al H 4 . Je to šedá pevná látka. Objevili jej Finholt, Bond a Schlesinger v roce 1947. Tato sloučenina se používá jako redukční činidlo v organické syntéze , zejména pro redukci esterů , karboxylových kyselin a amidů . Pevná látka se nebezpečně reaktivní vůči vodě, uvolňovat plynný vodík (H 2 ). Některé související deriváty byly diskutovány pro skladování vodíku .
Vlastnosti, struktura, příprava

LAH je bezbarvá pevná látka, ale komerční vzorky jsou kvůli kontaminaci obvykle šedé. Tento materiál může být čištěn rekrystalizací z diethyletheru . Velké čištění využívá Soxhletův extraktor . Obvykle se při syntéze používá nečistý šedý materiál, protože nečistoty jsou neškodné a lze je snadno oddělit od organických produktů. Čistý práškový materiál je pyroforický , ale ne jeho velké krystaly. Některé komerční materiály obsahují minerální olej, který inhibuje reakce se vzdušnou vlhkostí, ale častěji je balen v plastových pytlích odolných proti vlhkosti.
LAH prudce reaguje s vodou, včetně atmosférické vlhkosti, aby uvolnil plynný vodík. Reakce probíhá podle následující idealizované rovnice:
- LiAlH 4 + 4 H 2 O → LiOH + Al (OH) 3 + 4 H 2
Tato reakce poskytuje užitečnou metodu pro generování vodíku v laboratoři. Stárnoucí vzorky vystavené vzduchu často vypadají bílé, protože absorbovaly dostatek vlhkosti, aby vytvořily směs bílých sloučenin hydroxidu lithného a hydroxidu hlinitého .
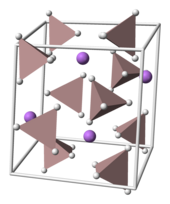
Struktura
LAH krystalizuje v monoklinické prostorové skupině P 2 1 / c . Jednotková buňka má rozměry: s = 4,82, b = 7,81, a c = 7,92 A, α = γ = 90 ° a β = 112 °. Ve struktuře jsou centra Li + obklopena pěti AlH -
4 čtyřstěn . Centra Li + jsou navázána na jeden atom vodíku z každého z okolních čtyřstěnů a vytvářejí tak bipyramidové uspořádání. Při vysokých tlacích (> 2,2 GPa) může dojít k fázovému přechodu, čímž se získá β-LAH.
Příprava
LiAlH 4 se nejprve připraví reakcí mezi lithiumaluminiumhydrid (LiH) a chlorid hlinitý :
- 4 LiH + AlCl 3 → LiAlH 4 + 3 LiCl
Kromě této metody zahrnuje průmyslová syntéza počáteční přípravu hydridu hlinito-sodného z prvků za vysokého tlaku a teploty:
- Na + AI + 2 H 2 → NaAlH 4
LiAlH 4 se pak připraví sůl metatéze podle:
- NaAlH 4 + LiCl → LiAlH 4 + chlorid sodný
který probíhá ve vysokém výnosu. LiCl se odstraní filtrací z etherického roztoku LAH, s následným vysrážením LiAlH 4 , čímž se získá produkt, který obsahuje přibližně 1% w / w LiCl.
Alternativní příprava vychází z LiH, a kovový AI namísto AlCl 3 . Katalyzována malého množství TiCl 3 (0,2%), reakce se provádí za použití dobře dimethylether jako rozpouštědla. Tato metoda zabraňuje kogeneraci soli.
Údaje o rozpustnosti
| Solventní | Teplota (° C) | ||||
|---|---|---|---|---|---|
| 0 | 25 | 50 | 75 | 100 | |
| Diethylether | - | 5,92 | - | - | - |
| THF | - | 2,96 | - | - | - |
| Monoglym | 1.29 | 1,80 | 2.57 | 3.09 | 3.34 |
| Diglyme | 0,26 | 1.29 | 1.54 | 2.06 | 2.06 |
| Triglyme | 0,56 | 0,77 | 1.29 | 1,80 | 2.06 |
| Tetraglym | 0,77 | 1.54 | 2.06 | 2.06 | 1.54 |
| Dioxan | - | 0,03 | - | - | - |
| Dibutylether | - | 0,56 | - | - | - |
LAH je rozpustný v mnoha éterických roztocích. Může se však spontánně rozložit v důsledku přítomnosti katalytických nečistot, i když se zdá být stabilnější v tetrahydrofuranu (THF). THF je tedy výhodný před např. Diethyletherem , a to navzdory nižší rozpustnosti.
Termodynamické údaje
Tabulka shrnuje termodynamická data pro LAH a reakce zahrnující LAH ve formě standardní změny entalpie , entropie a Gibbsovy volné energie .
| Reakce | ΔH ° (kJ / mol) |
ΔS ° (J / (mol · K)) |
ΔG ° (kJ / mol) |
Komentář |
|---|---|---|---|---|
| Li (s) + Al (s) + 2 H 2 (g) → LiAlH 4 (s) | -116,3 | -240,1 | -44,7 | Standardní tvorba z prvků. |
| LiH (y) + Al (s) + 3 / 2 H 2 (g) → LiAlH 4 (s) | -95,6 | -180,2 | 237.6 | Při použití ΔH ° f (LiH) = -90,579865, ΔS ° f (LiH) = -679,9 a ΔG ° f (LiH) = -67,31235744. |
| LiAlH 4 (s) → LiAlH 4 (l) | 22 | - | - | Teplo fúze. Hodnota může být nespolehlivá. |
| LiAlH 4 (l) → 1 / 3 Li 3 AlH 6 (s) + 2 / 3 AI (y) + H 2 (g) | 3.46 | 104,5 | -27,68 | ΔS ° vypočítané z hlášených hodnot ΔH ° a ΔG °. |
Tepelný rozklad
LAH je metastabilní při pokojové teplotě. Při delším skladování se pomalu rozkládá na Li 3 AlH 6 a LiH. Tento proces lze urychlit přítomností katalytických prvků, jako je titan , železo nebo vanad .

Při zahřátí se LAH rozkládá ve tříkrokovém reakčním mechanismu :
-
3 LiAlH 4 → Li 3 AlH 6 + 2 Al + 3 H 2
( R1 )
-
2 Li 3 AlH 6 → 6 LiH + 2 Al + 3 H 2
( R2 )
-
2 LiH + 2 Al → 2 LiAl + H 2
( R3 )
R1 je obvykle iniciován tavením LAH v teplotním rozmezí 150–170 ° C, bezprostředně následovaným rozkladem na pevný Li 3 AlH 6 , i když je známo , že R1 postupuje i pod bodem tání LiAlH 4 . Při asi 200 ° C se Li 3 AlH 6 rozkládá na LiH ( R2 ) a Al, které se následně převádějí na LiAl nad 400 ° C ( R3 ). Reakce R1 je skutečně nevratná. R3 je reverzibilní s rovnovážným tlakem asi 0,25 bar při 500 ° C. R1 a R2 mohou nastat při teplotě místnosti s vhodnými katalyzátory.
Aplikace
Použití v organické chemii
Lithiumaluminiumhydrid (LiAlH4) je široce používán v organické chemii jako redukční činidlo . Je silnější než příbuzné činidlo borohydrid sodný díky slabší vazbě Al-H ve srovnání s vazbou BH. Často jako roztok v diethyletheru a následný zpracováním kyselinou převede estery , karboxylové kyseliny , acylchloridy , aldehydy a ketony na odpovídající alkoholy (viz redukce karbonylu ). Podobně převádí amidové , nitro , nitrilové , iminové , oximové a azidové sloučeniny na aminy (viz: redukce amidu ). Redukuje kvartérní amoniové kationty na odpovídající terciární aminy. Reaktivitu lze doladit nahrazením hydridových skupin alkoxyskupinami . Vzhledem ke své samozápalné povaze, nestabilitě, toxicitě, nízké skladovatelnosti a problémům s manipulací spojenými s jeho reaktivitou byl v posledním desetiletí nahrazen, a to jak v malém průmyslovém měřítku, tak pro redukce ve velkém měřítku vhodnějším souvisejícím činidlem sodným bis (2-methoxyethoxy) aluminiumhydrid , který vykazuje podobnou reaktivitu, ale s vyšší bezpečností, snadnější manipulací a lepší ekonomikou.
LAH se nejčastěji používá k redukci esterů a karboxylových kyselin na primární alkoholy; před příchodem LiAlH 4 se jedná o těžké konverze zahrnující sodný kovu ve vroucím ethanolu (dále redukce Bouveault-Blanc ). Aldehydy a ketony mohou být také snížena na alkoholů LAH, ale to se obvykle provádí za použití mírnějších reakčních činidel, jako je například NaBH 4 ; a, β-nenasycené ketony se redukují na allylalkoholy. Když jsou epoxidy redukovány pomocí LAH, reagují činidla na méně bráněný konec epoxidu, obvykle za vzniku sekundárního nebo terciárního alkoholu. Epoxycyklohexany se redukují, aby se přednostně získaly axiální alkoholy.
Částečná redukce chloridů kyselin za vzniku odpovídajícího aldehydového produktu nemůže pokračovat přes LAH, protože ten redukuje až k primárnímu alkoholu. Místo toho musí být použit mírnější lithiumaluminium tri (t-butoxy) hydrid , který reaguje podstatně rychleji s chloridem kyseliny než s aldehydem. Například když se na kyselinu isovalerovou působí thionylchloridem za vzniku isovaleroylchloridu, lze ji potom redukovat pomocí lithiumaluminium tri (t-butoxy) hydridu za vzniku isovaleraldehydu v 65% výtěžku.

Lithiumaluminiumhydrid také redukuje alkylhalogenidy na alkany . Nejrychleji reagují alkyljodidy, následované alkylbromidy a poté alkylchloridy. Nejaktivnější jsou primární halogenidy, po nichž následují sekundární halogenidy. Terciární halogenidy reagují pouze v určitých případech.
Lithiumaluminiumhydrid nesnižuje jednoduché alkeny nebo areny . Alkyny jsou redukovány pouze v případě, že je poblíž alkoholová skupina. Bylo pozorováno, že LiAlH4 redukuje dvojnou vazbu v N-allylamidech.
Anorganická chemie
LAH se široce používá k přípravě hydridů hlavních skupin a přechodných kovů z odpovídajících halogenidů kovů . Například hydrid sodný (NaH) lze připravit z chloridu sodného (NaCl) následující reakcí:
- LiAlH 4 + 4 NaCl → 4 NaH + LiCl + AlCl 3
LAH také reaguje s mnoha anorganickými ligandy za vzniku koordinovaných komplexů oxidu hlinitého spojených s ionty lithia.
- LiAlH 4 + 4NH 3 → Li [Al (NH 2 ) 4 ] + 4H 2
Skladování vodíku

LiAlH 4 obsahuje 10,6% hmotn vodíku, čímž LAH potenciální skladování vodíku médium pro budoucí palivového článku silové vozidla . Vysoký obsah vodíku, jakož i objev reverzibilní skladování vodíku v Ti-dopovaný NaAlH 4 , vyvolaly obnovený výzkumu LiAlH 4 v posledním desetiletí. Podstatné výzkumné úsilí bylo věnováno urychlení kinetiky rozkladu katalytickým dopingem a kulovým mletím . Aby se využila výhoda celkové kapacity vodíku, musí být rovněž odstraněna meziprodukt LiH . Vzhledem ke své vysoké termodynamické stabilitě to vyžaduje teploty přesahující 400 ° C, což se pro účely přepravy nepovažuje za proveditelné. Přijímáním LiH + Al jako konečného produktu se kapacita skladování vodíku sníží na 7,96% hmotn. Další problém souvisí s skladování vodíku je recyklování zpět do LiAlH 4 , které vzhledem ke své relativně nízké stability, vyžaduje extrémně vysoký tlak vodíku vyšší než 10000 bar. Jízda na kole jedinou reakcí R2 -, která je při použití Li 3 ALH 6 jako výchozí materiál, - se ukládala 5,6 hmotnostních% vodíku v jednom kroku (vs dvou krocích NaAlH 4, který ukládá přibližně stejné množství vodíku). Pokusy o tento proces však dosud nebyly úspěšné.
Ostatní tetrahydridohlinitany
Je známa řada solí analogických s LAH. NaH lze použít efektivní přípravu hlinitý hydrid sodný (NaAlH 4 ) od výměnnou reakcí v THF:
- LiAlH 4 + NaH → NaAlH 4 + LiH
Draselný aluminium hydrid (KAlH 4 ) mohou být vyrobeny podobně jako v diglymu jako rozpouštědlo:
- LiAlH 4 + KH → KAlH 4 + LiH
Opačné, tj. Produkce LAH buď z hydridu hlinito-sodného nebo z hydridu hlinito-draselného lze dosáhnout reakcí s LiCl nebo hydridem lithným v diethyletheru nebo THF :
- NaAlH 4 + LiCl → LiAlH 4 + chlorid sodný
- KAlH 4 + LiCl → LiAlH 4 + KCl
"Alanate Hořčík" (Mg (AlH 4 ) 2 ) vzniká podobně za použití MgBr 2 :
- 2 LiAlH 4 + MgBr 2 → Mg (AlH 4 ) 2 + 2 LiBr
Red-Al (nebo SMEAH, NaAlH 2 (OC 2 H 4 OCH 3 ) 2 ), se syntetizuje reakcí sodnohlinitý tetrahydride (NaAlH 4 ) a 2-methoxyethanol :
Viz také
Reference
Další čtení
- Wiberg, E .; Amberger, E. (1971). Hydridy prvků hlavních skupin I-IV . Elsevier. ISBN 0-444-40807-X .
- Hajos, A. (1979). Složité hydridy a související redukční činidla v organické syntéze . Elsevier. ISBN 0-444-99791-1 .
- Lide, DR, vyd. (1997). Příručka chemie a fyziky . CRC Press. ISBN 0-8493-0478-4 .
- Carey, FA (2002). Organická chemie s online výukovým centrem a výukou podle modelu na CD-ROM . McGraw-Hill. ISBN 0-07-252170-8 .
- Andreasen, A. (2005). „Kapitola 5: Složité hydridy“ (PDF) . Materiály pro skladování vodíku se zaměřením na prvky hlavní skupiny I-II . Risø National Laboratory. ISBN 87-550-3498-5 . Archivovány z původního (PDF) 19. 8. 2012.
externí odkazy
- "Využití LiAlH 4 " . Organické syntézy.
- „Lithium tetrahydridoaluminate - Compound Summary (CID 28112)“ . PubChem.
- "Tetrahydridoaluminát lithný" . Webová kniha . NIST.
- "Bezpečnostní list materiálů" . Cornell University. Archivovány od originálu 8. března 2006.
- "Hydridové informační centrum" . Sandia National Laboratory. Archivovány od originálu 7. května 2005.
- „Redukční reakce“ (PDF) . Učební zdroje - 4. ročník . University of Birmingham. Archivovány z původního (PDF) 23. května 2016.