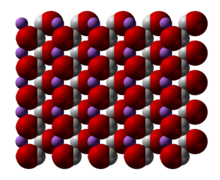
Hydroxid lithný - Lithium hydroxide
|
|
|
|
|
 |
|

|
|
| Jména | |
|---|---|
|
Název IUPAC
Hydroxid lithný
|
|
| Identifikátory | |
|
3D model ( JSmol )
|
|
| ČEBI | |
| ChemSpider | |
| Informační karta ECHA |
100,013,804 |
| 68415 | |
|
PubChem CID
|
|
| Číslo RTECS | |
| UNII | |
| UN číslo | 2680 |
|
CompTox Dashboard ( EPA )
|
|
|
|
|
|
| Vlastnosti | |
| LiOH | |
| Molární hmotnost | |
| Vzhled | |
| Zápach | žádný |
| Hustota | |
| Bod tání | 462 ° C (864 ° F; 735 K) |
| Bod varu | 924 ° C (1695 ° F; 1197 K) se rozkládá |
| Rozpustnost v methanolu | |
| Rozpustnost v ethanolu | |
| Rozpustnost v isopropanolu | |
| Bazicita (p K b ) | -0,04 |
| Konjugovaná základna | Anionty oxidu lithného |
| −12,3 · 10 −6 cm 3 /mol | |
|
Index lomu ( n D )
|
|
| Termochemie | |
|
Tepelná kapacita ( C )
|
2,071 J/g⋅K |
|
Standardní entalpie
tvorby (Δ f H ⦵ 298 ) |
−20,36 kJ/g |
| Nebezpečí | |
| Hlavní nebezpečí | Korozívní |
| Bezpečnostní list |
„ICSC 0913“ . „ICSC 0914“ . (monohydrát) |
| NFPA 704 (ohnivý diamant) | |
| Bod vzplanutí | Nehořlavé |
| Smrtelná dávka nebo koncentrace (LD, LC): | |
|
LD 50 ( střední dávka )
|
210 mg/kg (orální, krysa) |
| Související sloučeniny | |
|
Jiné anionty
|
Amid lithný |
|
Jiné kationty
|
Hydroxid sodný Hydroxid draselný Hydroxid rubidia Hydroxid česný |
|
Související sloučeniny
|
Oxid lithný |
|
Pokud není uvedeno jinak, jsou údaje uvedeny pro materiály ve standardním stavu (při 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Reference na infobox | |
Hydroxid lithný je anorganická sloučenina se vzorcem LiOH . (H 2 O) n . Bezvodá i hydratovaná forma jsou bílé hygroskopické pevné látky. Jsou rozpustné ve vodě a mírně rozpustné v ethanolu . Oba jsou komerčně dostupné. I když je hydroxid lithný klasifikován jako silná báze , je nejslabším známým hydroxidem alkalického kovu.
Výroba
Preferovanou surovinou je spodumen z tvrdých hornin , kde je obsah lithia vyjádřen jako % oxidu lithného .
Trasa uhličitanu lithného
Hydroxid lithný se často průmyslově vyrábí z uhličitanu lithného v metateze s hydroxidem vápenatým :
- Li 2 CO 3 + Ca (OH) 2 → 2 LiOH + CaCO 3
Původně vyrobený hydrát se dehydratuje zahříváním ve vakuu až na 180 ° C.
Cesta síranem lithným
Alternativní cesta zahrnuje meziprodukt síranu lithného :
- α-spodumen → β-spodumen
- β-spodumen + CaO → Li 2 O + ...
- Li 2 O + H 2 SO 4 → Li 2 SO 4 + H 2 O
- Li 2 SO 4 + 2 NaOH → Na 2 SO 4 + 2 LiOH.
Hlavními vedlejšími produkty jsou sádra a síran sodný, které mají určitou tržní hodnotu.
Komerční nastavení
Podle agentury Bloomberg byly největšími producenty v roce 2020 společnosti Ganfeng Lithium Co. Ltd. (GFL nebo Ganfeng) a Albemarle s přibližně 25 kt/rok, dále Livent Corporation (FMC) a SQM . Plánuje se významná nová kapacita, která bude držet krok s poptávkou poháněnou elektrifikací vozidel. Společnost Ganfeng rozšíří chemickou kapacitu lithia na 85 000 tun a přidáním kapacity pronajaté od společnosti Jiangte se Ganfeng v roce 2021 stane největším globálním výrobcem hydroxidu lithného.
Závod Albemarle v Kemertonu WA, původně plánovaný na dodávku 100 kt/rok, byl snížen na 50 kt/rok.
v roce 2023 AVZ Minerals, australská společnost, plánuje vyrábět vysoce čistý primární lithium sulfát lithný (PLS) s obsahem baterie obsahující více než 80% lithia. PLS je lithiová chemikálie, která je na trhu novinkou ve výrobě hydroxidu lithného (předchůdce lithium-iontové baterie).
V roce 2020 je největším výrobcem Tianqi Lithium's , závod v Kwinaně v západní Austrálii s kapacitou 48 kt/rok.
Aplikace
Lithium -iontové baterie
Hydroxid lithný se spotřebovává hlavně při výrobě katodových materiálů pro lithium -iontové baterie , jako je oxid lithný kobaltu (LiCoO 2 ) a fosforečnan lithno -železitý . Je upřednostňován před uhličitanem lithným jako prekurzor pro oxidy kobaltu lithného niklu a manganu .
Tuk
Oblíbeným zahušťovadlem lithného tuku je lithium-12-hydroxystearát , který vyrábí univerzální mazací tuk díky své vysoké odolnosti vůči vodě a použitelnosti při různých teplotách.
Čištění oxidu uhličitého
Hydroxid lithný se používá v systémech čištění dýchacích plynů pro kosmické lodě , ponorky a rebreathers k odstraňování oxidu uhličitého z vydechovaného plynu produkcí uhličitanu lithného a vody:
- 2 LiOH • H 2 O + CO 2 → Li 2 CO 3 + 3 H 2 O
nebo
- 2 LiOH + CO 2 → Li 2 CO 3 + H 2 O
Posledně jmenovaný, bezvodý hydroxid, je výhodný pro svou nižší hmotnost a menší produkci vody pro respirační systémy v kosmických lodích. Jeden gram bezvodého hydroxidu lithného může odstranit 450 cm 3 z plynného oxidu uhličitého. Monohydrát ztrácí vodu při 100–110 ° C.
Předchůdce
Hydroxid lithný je spolu s uhličitanem lithným klíčovými meziprodukty používanými pro výrobu dalších sloučenin lithia, což dokládá jeho použití při výrobě fluoridu lithného :
- LiOH + HF → LiF + H 2 O.
Jiné použití
Používá se také v keramice a některých formulacích portlandského cementu . Hydroxid lithný ( isotopově obohacených v lithium-7 ) se používá k alkalizovat chladicí kapaliny reaktoru, ve tlakovodní reaktory pro potlačení koroze. Je to dobrá radiační ochrana proti volným neutronům.
Cena
V roce 2012 byla cena hydroxidu lithného asi 5-6 $/kg.
V prosinci 2020 se zvýšil na 9 $/kg
Dne 18. března 2021 se cena zvýšila na 11,50 USD/kg
Viz také
Reference
externí odkazy
- Mezinárodní karta chemické bezpečnosti 0913 (bezvodá)
- Mezinárodní karta chemické bezpečnosti 0914 (monohydrát)

