Mycoplasma pneumoniae -Mycoplasma pneumoniae
| Mycoplasma pneumoniae | |
|---|---|
| Vědecká klasifikace | |
| Doména: | |
| Kmen: | |
| Třída: | |
| Objednat: | |
| Rodina: | |
| Rod: | |
| Druh: |
M. pneumoniae
|
| Binomické jméno | |
|
Mycoplasma pneumoniae Somerson a kol., 1963
|
|
Mycoplasma pneumoniae je velmi malá bakterie ze třídy Mollicutes . Jedná se o lidský patogen, který způsobuje onemocnění mykoplazmatickou pneumonií , což je forma atypické bakteriální pneumonie související s chladným aglutininovým onemocněním . M. pneumoniae je charakterizována nepřítomností buněčné stěny peptidoglykanu a výslednou odolností vůči mnoha antibakteriálním činidlům . Perzistenceinfekcí M. pneumoniae i po léčbě je spojena s její schopností napodobitsložení povrchu hostitelské buňky .
Objev a historie
V roce 1898, Nocard a Roux izolován agent Předpokládá se, že příčinou skotu pneumonie a pojmenoval jej mikrob de la peripneumonie Mikroorganismy z jiných zdrojů, které mají podobné vlastnosti jako na plicní organismu (PPO) skotu, brzy přišel být známý jako pleuropneumonia- jako organismy (PPLO), ale jejich skutečná podstata zůstala neznámá. Později bylo prokázáno, že mnoho PPLO je příčinou pneumonií a artritidy u několika nižších zvířat.
V roce 1944 použila Monroe Eaton embryonovaná kuřecí vejce k kultivaci agenta, který je považován za příčinu primární lidské atypické pneumonie (PAP), běžně známé jako „chodící pneumonie“. Tento neznámý organismus se stal známým jako „agent Eaton“. V té době společnost Eaton používala embryonovaná vajíčka, která se poté používala pro kultivaci virů, podporu myšlenky, že agent Eaton je virus. Přesto bylo známo, že PAP lze léčit širokospektrálními antibiotiky , což vyvolává podezření na virovou etiologii.
Robert Chanock , výzkumník virů agentů společnosti Eaton z NIH , navštívil v roce 1961 Wistar Institute ve Philadelphii, aby získal buněčnou kulturu normálního kmene lidských buněk vyvinutou Leonardem Hayflickem . Bylo známo, že tento buněčný kmen je mimořádně citlivý na izolaci a růst lidských virů. Chanock řekl Hayflickovi o svém výzkumu agenta Eaton a o svém přesvědčení, že jeho virová povaha je diskutabilní. Ačkoli Hayflick věděl málo o současném výzkumu tohoto agenta, jeho doktorská práce byla provedena o chorobách zvířat způsobených PPLO. Hayflick věděl, že mnoho nižších zvířat trpí pneumoniemi způsobenými PPLO (později nazývanými mykoplazmy ). Hayflick usoudil, že agent Eaton může být mykoplazma a ne virus. Chanock nikdy neslyšel o mykoplazmách a na Hayflickovu žádost mu poslal vaječný žloutek obsahující agenta Eatona.
Hayflick pomocí nového přípravku z agaru a tekutého média, který navrhl, izoloval z vaječného žloutku unikátní mykoplazmu. To bylo brzy prokázáno Chanockem a Hayflickem jako původce PAP. Když se tento objev stal známým předním světovým odborníkem na tyto organismy, doktorkou Emmy Klieneberger-Nobel z Listerského institutu v Londýně, navrhla, aby se tento organismus jmenoval Mycoplasma hayflickiae . Hayflick namítl ve prospěch Mycoplasma pneumoniae .
Tento nejmenší volně žijící mikroorganismus byl první izolován a bylo prokázáno, že je příčinou lidské nemoci. Za svůj objev obdržel Hayflick Prezidentskou cenu Mezinárodní organizace pro mykoplazmologii. Invertovaný mikroskop, pod kterým Hayflick objevil Mycoplasma pneumoniae, byl zpřístupněn Smithsonian Institution .
Taxonomie a klasifikace
Termín Mycoplasma ( mykes což znamená, houby, a plazmy , což znamená vytvořený) je odvozen z houbového -jako růstu některých druhů mykoplazmat. Mykoplazmy byly v roce 1960 klasifikovány jako Mollicutes („mollis“, což znamená měkké a „cutis“, což znamená kůže) kvůli jejich malé velikosti a genomu , nedostatku buněčné stěny , nízkému obsahu G+C a neobvyklým nutričním potřebám. M. pneumoniae bylo označeno jako arginin non kvasných druhů. Mykoplazmy jsou dále klasifikovány podle sekvenčního složení 16s rRNA . Všechna mykoplazmata ze skupiny pneumoniae mají podobné 16s variace rRNA jedinečné pro tuto skupinu, z nichž M. pneumoniae má 6,3% variace v konzervovaných oblastech , což naznačuje, že mykoplazmy vzniklé degenerativní evolucí z grampozitivní eubakteriální skupiny, která zahrnuje bacily , streptokoky a laktobacily . M. pneumoniae je členem čeledi Mycoplasmataceae a řád Mycoplasmatales .
Buněčná biologie
Mykoplazmy, které patří mezi nejmenší samoreplikující se organismy, jsou parazitické druhy, kterým chybí buněčná stěna a periplazmatický prostor , mají snížené genomy a omezenou metabolickou aktivitu. Buňky Mycoplasma pneumoniae mají prodloužený tvar, který je přibližně 0,1–0,2 µm (100–200 nm ) na šířku a 1–2 µm (1 000–2 000 nm) na délku. Extrémně malá velikost buněk znamená, že je nelze vyšetřit světelnou mikroskopií ; stereomikroskop je pro zobrazení požadované morfologie a M. pneumoniae kolonií , které jsou obvykle menší než 100 um na délku. Neschopnost syntetizovat buněčnou stěnu peptidoglykanu je způsobena absencí genů kódujících její tvorbu a vede ke zvýšenému významu při udržování osmotické stability, aby se zabránilo vysychání . Nedostatek buněčné stěny také vyžaduje zvýšenou podporu buněčné membrány (vyztužené steroly), která zahrnuje tuhý cytoskelet složený ze složité proteinové sítě a potenciálně extracelulární kapsle usnadňující adherenci k hostitelské buňce . M. pneumoniae jsou jediné bakteriální buňky, které mají ve své buněčné membráně cholesterol (získaný z hostitele) a mají více genů, které kódují variace membránových lipoproteinů, než jiné mykoplazmy, o nichž se předpokládá, že jsou spojeny s jeho parazitickým životním stylem. Buňky M. pneumoniae mají také připevňovací organelu , která se používá při klouzavé pohyblivosti organismu neznámým mechanismem.
Genomika a metabolická rekonstrukce
Sekvenování na pneumoniae M. genomu v roce 1996 odhalila, že je 816394 pb. Genom obsahuje 687 genů, které kódují proteiny, z nichž asi 56,6% kóduje esenciální metabolické enzymy ; zejména těch, které se podílejí na glykolýze a fermentaci organickými kyselinami . M. pneumoniae je v důsledku toho velmi citlivé na ztrátu enzymatické funkce pomocí genových mutací , jako jediný pufrovací systémy proti funkční ztrátu bodovými mutacemi jsou pro údržbu pentózofosfátové cesty a nukleotidů metabolismu. Ztráta funkce v jiných drahách se navrhuje kompenzovat metabolizmem hostitelských buněk. Kromě potenciálu pro ztrátu funkce dráhy redukovanému genomu M. pneumoniae přímo chybí řada cest, včetně cyklu TCA , transportního řetězce respiračních elektronů a cest biosyntézy pro aminokyseliny , mastné kyseliny , cholesterol a puriny a pyrimidiny . Tato omezení činí M. pneumoniae závislým na dovozních systémech, které získávají základní stavební kameny ze svého hostitele nebo prostředí, které nelze získat glykolytickými cestami . Spolu s energetickou nákladné proteinů a RNA výroby, velká část energetického metabolismu působí pro udržení protonových přechody (až 80%), vzhledem k vysoké poměr plochy povrchu k objemu z pneumoniae M. buněk. Pouze 12 - 29% energetického metabolismu je zaměřeno na růst buněk , což je u bakteriálních buněk neobvykle málo a je považováno za adaptaci jeho parazitického životního stylu. Na rozdíl od jiných bakterií používá M. pneumoniae kodon UGA ke kódování tryptofanu, a nikoli jako stop kodon.
Hostitel a reprodukce
Mycoplasma pneumoniae roste výhradně parazitováním na savcích. Reprodukce tedy závisí na připojení k hostitelské buňce. Podle Waiteho a Talkingtona dochází ke specializované reprodukci „ binárním štěpením , dočasně spojeným s duplikací její připojené organely, která migruje do opačného pólu buňky během replikace a před separací nukleoidů “. Mutace, které ovlivňují tvorbu připojovací organely, nejen brání motilitě a dělení buněk , ale také snižují schopnost buněk M. pneumoniae adherovat k hostitelské buňce.
Patogenita
Mycoplasma pneumoniae parazituje na epitelu dýchacích cest člověka. Dodržování respiračních epiteliálních buňkách se předpokládá, že dochází prostřednictvím připevňovacího organely, následuje vyhýbání se hostitelský imunitní systém podle intracelulární lokalizaci a nastavení buněčné membrány kompozice napodobovat membránu hostitelské buňky.
Cytoadherence
Přilnutí M. pneumoniae k hostitelské buňce (obvykle buňce dýchacího traktu , ale příležitostně buňce erytrocytů nebo urogenitální výstelky ) je iniciační událostí pro pneumonické onemocnění a související symptomy. Specializovaná připojovací organela je polární , elektronově hustá a prodloužená buněčná extenze, která usnadňuje pohyblivost a adherenci k hostitelským buňkám. Skládá se z centrálního vlákna obklopeného intracytoplazmatickým prostorem spolu s řadou adhezinů a strukturálních a pomocných proteinů lokalizovaných na špičce organely. Je známo, že k tvorbě a funkčnosti připevňovací organely přispívá řada proteinů, včetně pomocných proteinů HMW1 – HMW5, P30, P56 a P90, které poskytují strukturu a podporu adhezinu, a P1, P30 a P116, které jsou přímo zapojeny do příloha. Tato síť proteinů se podílí nejen na zahájení tvorby a adheze organel přichycení, ale také na pohyblivosti . P1 adhesin (trypsin citlivé protein) je 120 kDa protein vysoce seskupeny na povrchu špičky připevnění organel v virulentní mykoplazmat. Pro připojení M. pneumoniae k hostitelské buňce je nutná jak přítomnost P1, tak jeho koncentrace na povrchu buňky. Buňky M. pneumoniae ošetřené monoklonálními protilátkami specifickými pro imunogenní C-konec P1 adhezinu byly inhibovány ve své schopnosti připojit se k povrchu hostitelské buňky přibližně o 75%, což naznačuje, že P1 je hlavní složkou adherence. Tyto protilátky také snížily schopnost buňky rychle klouzat , což může přispět ke snížení adherence k hostiteli tím, že brání jejich schopnosti lokalizovat hostitelskou buňku. Kromě toho mutace v P1 nebo degradace působením trypsinu poskytují avirulentní buňky M. pneumoniae . Ztráta proteinů v cytoskeletu zapojená do lokalizace P1 ve struktuře hrotu, jako je HMW1 – HMW3, také způsobuje avirulenci kvůli nedostatku shlukování adhezinu . Dalším proteinem, který hraje důležitou roli v adherenci, je P30, protože buňky M. pneumoniae s mutacemi v tomto proteinu nebo s protilátkami vytvořenými proti P30 nejsou schopné adherovat k hostitelským buňkám. P30 není zapojen do lokalizace P1 ve špičkové struktuře, protože P1 je transportován do připojovací organely v mutantech P30, ale spíše může fungovat jako doplňkový adhezin vázající receptor . Mutanti P30 také vykazují odlišné morfologické znaky, jako je více laloků a zaoblený tvar, na rozdíl od prodloužených, což naznačuje, že P30 může interagovat s cytoskeletem během tvorby připojovací organely. Řada složek povrchu eukaryotických buněk se podílí na adherenci buněk M. pneumoniae k epitelu respiračního traktu . Mezi nimi jsou sialoglykokonjugáty , sulfátované glykolipidy , glykoproteiny , fibronektin a receptory neuraminové kyseliny . Lektiny na povrchu bakteriálních buněk jsou schopné vázat oligosacharidové řetězce na glykolipidech a glykoproteinech, aby usnadnily navázání, navíc k proteinům TU a pyruvátdehydrogenáze E1 p , které se vážou na fibronektin.
Intracelulární lokalizace
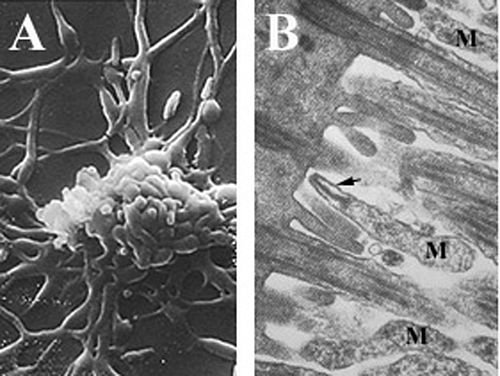
O Mycoplasma pneumoniae je známo, že se vyhýbá detekci imunitního systému hostitele , odolává léčbě antibiotiky a překračuje slizniční bariéry, což může být způsobeno jeho schopností fúzovat s hostitelskými buňkami a přežít intracelulárně . Kromě těsné fyzické blízkosti M. pneumoniae a hostitelských buněk může fúzi usnadnit nedostatek buněčné stěny a zvláštních složek buněčné membrány , jako je cholesterol (1). Interní lokalizace může způsobit chronické nebo latentní infekce, protože M. pneumoniae je schopna přetrvávat , syntetizovat DNA a replikovat se v hostitelské buňce i po léčbě antibiotiky. Přesný mechanismus intracelulární lokalizace není znám, nicméně potenciál pro cytoplazmatickou sekvestraci v hostiteli vysvětluje obtížnost úplného odstranění infekcí M. pneumoniae u postižených jedinců.
Imunitní odpověď
Kromě vyhýbání se imunitnímu systému hostitele intracelulární lokalizací může M. pneumoniae změnit složení své buněčné membrány, aby napodobil membránu hostitelské buňky a vyhnul se detekci buňkami imunitního systému . Buňky M. pneumoniae mají řadu proteinových a glykolipidových antigenů, které vyvolávají imunitní reakce , ale variace těchto povrchových antigenů by umožnila infekci přetrvávat dostatečně dlouho, aby se buňky M. pneumoniae spojily s hostitelskými buňkami a unikly detekci. Podobnost mezi kompozicemi M. pneumoniae a membránami lidských buněk může také vést k autoimunitním reakcím v několika orgánech a tkáních.
Cytotoxicita a účinky na organismus
Hlavním cytotoxickým účinkem M. pneumoniae je lokální narušení tkáňové a buněčné struktury podél epitelu dýchacího traktu v důsledku jeho těsné blízkosti hostitelských buněk. Připojení bakterií k hostitelským buňkám může mít za následek ztrátu řasinek , snížení metabolismu , biosyntézu a import makromolekul a nakonec mohou být infikované buňky odstraněny z epiteliální výstelky. M. pneumoniae produkuje jedinečný faktor virulence známý jako toxin komunitního syndromu respirační tísně (CARDS). Toxin CARDS s největší pravděpodobností pomáhá při kolonizaci a patogenních cestách M. pneumoniae, což vede k zánětu a dysfunkci dýchacích cest. Kromě toho je tvorba peroxidu vodíku klíčovým faktorem virulence u infekcí M. pneumoniae . Uchycení M. pneumoniae na erytrocyty umožňuje difuzi peroxidu vodíku z bakterií do hostitelské buňky bez detoxifikace od kataláza nebo peroxidáza , která může zranit hostitelské buňky tím, že sníží glutathion , poškození lipidové membrány a způsobuje denaturaci bílkovin . Místní poškození může být také důsledkem získání laktoferinu a následné tvorby hydroxylových radikálů , superoxidového aniontu a peroxidu . Cytotoxické účinky infekcí M. pneumoniae se projevují běžnými příznaky, jako je kašel a podráždění plic, které mohou přetrvávat měsíce po odeznění infekce. Místní zánět a hyperreaktivita produkcí cytokinů indukovanou infekcí byla spojena s chronickými stavy, jako je bronchiální astma, a byla také spojena s progresí symptomů u jedinců s cystickou fibrózou a CHOPN .
Epidemiologie
Zdá se, že výskyt nemocí nesouvisí s ročním obdobím nebo geografií; infekce se však vyskytuje častěji v letních a podzimních měsících, kdy jsou jiné respirační patogeny méně rozšířené. Předpokládá se, že reinfekce a cyklování epidemie jsou důsledkem variace podtypu adhezinu P1. Přibližně 40% získané komunitní pneumonie je způsobena pneumoniae M. infekcí u dětí a starších osob bytí nejvíce náchylné , ale ne osobní rizikové faktory pro získání M. pneumoniae vyvolané pneumonie byly stanoveny. Přenos z M. pneumoniae může dojít pouze prostřednictvím těsném kontaktu a výměny aerosolů podle kašle v důsledku zvýšené citlivosti na buněčné stěny -lacking organismu vysychání . Ohnisek z pneumoniae M. infekcí se obvykle vyskytují ve skupinách lidí v těsné blízkosti a dlouhotrvající, včetně škol, institucí, vojenských základen, a domácností .
Příznaky infekce
O M. pneumoniae je známo, že způsobuje řadu symptomů, jako je primární atypická pneumonie , tracheobronchitida a onemocnění horních cest dýchacích . Primární atypická pneumonie je jedním z nejzávažnějších typů projevů, přičemž nejčastějším příznakem je tracheobronchitida a dalších 15% případů, obvykle dospělých, zůstává asymptomatických. Symptomatické infekce se obvykle vyvíjejí po dobu několika dnů a projevy pneumonie mohou být zaměněny s řadou dalších bakteriálních patogenů a stavů, které způsobují zápal plic. Tracheobronchitida je nejčastější u dětí kvůli snížené kapacitě imunitního systému a až 18% infikovaných dětí vyžaduje hospitalizaci . Mezi běžné mírné příznaky patří bolest v krku , sípání a kašel , horečka , bolest hlavy , rýma , myalgie a pocity neklidu , přičemž intenzitu a trvání symptomů lze omezit včasnou léčbou antibiotiky . Vzácně má pneumonie M. pneumoniae za následek smrt v důsledku lézí a ulcerace výstelky epitelu, plicního edému a obliteranů bronchiolitidy . Extrapulmonální příznaky, jako jsou autoimunitní reakce, komplikace centrálního nervového systému a dermatologické poruchy, byly spojeny s infekcí M. pneumoniae až v 25% případů.
Diagnóza
Diagnóza z pneumoniae Mycoplasma infekcí komplikuje zpožděný nástup příznaků a podobnost příznaků na jiné plicní onemocnění. Infekce M. pneumoniae jsou často diagnostikovány jako jiné stavy a příležitostně jsou nepatogenní mykoplazmy přítomné v respiračním traktu zaměněny za M. pneumoniae . Historicky byla diagnóza infekcí M. pneumoniae stanovena na základě přítomnosti studených aglutininů a schopnosti infikovaného materiálu redukovat tetrazolium . Kauzální diagnostika závisí na laboratorních testech, nicméně tyto metody jsou praktičtější v epidemiologických studiích než v diagnostice pacientů. Kultivační testy se jen zřídka používají jako diagnostické nástroje; k diagnostice a charakterizaci bakteriálních pneumonických infekcí se používá spíše imunoblotování , imunofluorescenční barvení, hemadsorpční testy, redukce tetrazolia, testy metabolické inhibice, sérologické testy a polymerázová řetězová reakce (PCR) . PCR je nejrychlejší a nejúčinnější způsob stanovení přítomnosti M. pneumoniae , tento postup však nenaznačuje aktivitu ani životaschopnost přítomných buněk. Sérologické testy enzymatické imunoanalýzy (EIA) jsou nejběžnější metodou detekce M. pneumoniae používanou v diagnostice pacientů kvůli nízkým nákladům a relativně krátké době testování. Jednou nevýhodou sérologie je, že jsou nutné životaschopné organismy, které mohou nadhodnocovat závažnost infekce. Žádná z těchto metod, spolu s jinými, nebyla lékařským odborníkům k dispozici v rychlé, účinné a dostatečně levné formě, aby mohla být použita při rutinní diagnostice, což vedlo ke snížení schopnosti lékařů diagnostikovat infekce M. pneumoniae .
Léčba a prevence
Většina antibiotik používaných k léčbě infekcí M. pneumoniae je zaměřena na bakteriální rRNA v ribozomálních komplexech, včetně makrolidů , tetracyklinu , ketolidů a fluorochinolonů , z nichž mnohé lze podávat orálně. Makrolidy jsou schopné snížit hyperreaktivitu a chránit epiteliální výstelku před oxidačním a strukturálním poškozením, jsou však schopné pouze inhibovat bakterie ( bakteriostatické ) a nejsou schopny způsobit smrt bakteriálních buněk. Nejběžnějšími makrolidy používanými při léčbě infikovaných dětí v Japonsku jsou erythromycin a klarithromycin , které inhibují syntézu bakteriálních proteinů vazbou 23S rRNA . Bylo prokázáno, že podávání antibiotik snižuje životnost a intenzitu infekcí M. pneumoniae ve srovnání s případy neléčenými. Navíc některé terapie vysokými dávkami steroidů prokázaly zvrácení neurologických účinků u dětí s komplikovanými infekcemi.
Obtížnost vymýcení infekcí způsobených bakterií Mycoplasma pneumoniae je dána schopností bakterie přetrvávat uvnitř jedince, jakož i nedostatkem buněčné stěny u M. pneumoniae , což činí více antibiotik namířených proti bakteriální buněčné stěně při léčbě infekcí neúčinnými. M. pneumoniae proto vykazuje odolnost vůči antimikrobiálním látkám, jako jsou beta-laktamy , glykopeptidy , sulfonamidy , trimethoprim , polymixiny , kyselina nalidixová a rifampin . Míra antimikrobiální lékové rezistence pro Mycoplasma pneumoniae byla stanovena v klinických vzorcích a izolátech získaných v letech 2011–2012 v kanadském Ontariu. Z 91 vzorků M. pneumoniae rezistentních na léčivo mělo 11 (12,1%) nukleotidové mutace spojené s rezistencí na makrolidy v genu 23S rRNA . Žádný ze vzorků M. pneumoniae nebyl odolný vůči fluorochinolonům nebo tetracyklinům .
Doxycyklin lze použít k léčbě pneumonie Mycoplasma , která se obvykle projevuje přetrvávajícím neustálým kašlem, který trvá několik týdnů a vykazuje intersticiální plicní infiltráty na rentgenu hrudníku.
Design vakcíny pro M. pneumoniae byl zaměřen především na prevenci přichycení hostitelské buňky, která by zabránila zahájení cytotoxicity a následných symptomů. K dnešnímu dni vakcíny cílené na adhezin P1 neprokázaly žádné snížení nástupu infekce a některé pokusy s vakcínami vedly ke zhoršení symptomů v důsledku senzibilizace imunitního systému . Nedávné experimenty na myších modelech spojily tento jev se senzibilizací imunitního systému lipidovými skupinami lipoproteinů M. pneumoniae . Zavedení peptidů, které blokují receptory adheze na povrch hostitelské buňky, může být také schopné zabránit připojení M. pneumoniae .
Přenos infekcí Mycoplasma pneumoniae je obtížné omezit kvůli několikadennímu období infekce, než se objeví příznaky. Nedostatek vhodných diagnostických nástrojů a účinné léčby bakterií také přispívá k vypuknutí infekce. Pomocí teorie sítí Meyers et al. analyzovala přenos infekcí M. pneumoniae a na základě vytvořeného modelu vyvinula kontrolní strategie. Zjistili, že kohortování pacientů je méně účinné kvůli dlouhé inkubační době , a tak je nejlepší metodou prevence omezit interakce pečující s pacientem a omezit pohyb pečujících osob na více oddělení .
Viz také
| Externí video | |
|---|---|
|
|
Reference
Tento článek včlení text veřejné domény z citovaného CDC.
Další čtení
- Baseman JB, Reddy SP, Dallo SF (říjen 1996). „Souhra mezi povrchovými proteiny mykoplazmy, buňkami dýchacích cest a proteanskými projevy lidských infekcí zprostředkovaných mykoplazmou“. American Journal of Respiratory and Critical Care Medicine . 154 (4 Pt 2): S137-44. doi : 10,1146/ajrccm/154,4_Pt_2.S137 . PMID 8876532 .
- Razin S, Yogev D, Naot Y (prosinec 1998). „Molekulární biologie a patogenita mykoplazmat“ . Recenze mikrobiologie a molekulární biologie . 62 (4): 1094–156. doi : 10,1128/MMBR.62.4.1094-1156.1998 . PMC 98941 . PMID 9841667 .
- Kashyap S, Sarkar M (duben 2010). „Mycoplasma pneumonia: Klinické rysy a léčba“ . Plicní Indie . 27 (2): 75–85. doi : 10.4103/0970-2113.63611 . PMC 2893430 . PMID 20616940 .
- Narita M (září 2009). „Patogeneze neurologických projevů infekce Mycoplasma pneumoniae“. Dětská neurologie . 41 (3): 159–66. doi : 10,1016/j.pediatrneurol.2009.04.012 . PMID 19664529 .
- Ferwerda A, Moll HA, de Groot R (srpen 2001). „Infekce dýchacích cest Mycoplasma pneumoniae u dětí: přehled diagnostických a terapeutických opatření“. European Journal of Pediatrics . 160 (8): 483–91. doi : 10,1007/s004310100775 . PMID 11548186 . S2CID 9131256 .
- Esposito S, Droghetti R, Bosis S, Claut L, Marchisio P, Principi N (srpen 2002). „Sekrece cytokinů u dětí s akutní infekcí a sípáním Mycoplasma pneumoniae“. Dětská pneumologie . 34 (2): 122–7. doi : 10,1002/ppul.10139 . PMID 12112778 . S2CID 1386332 .
- Ríos AM, Mejías A, Chávez-Bueno S, Fonseca-Aten M, Katz K, Hatfield J, et al. (Srpen 2004). „Dopad terapie cethromycinem (ABT-773) na mikrobiologické, histologické, imunologické a respirační indexy na myším modelu infekce dolních cest dýchacích Mycoplasma pneumoniae“ . Antimikrobiální látky a chemoterapie . 48 (8): 2897–904. doi : 10.1128/AAC.48.8.2897-2904.2004 . PMC 478543 . PMID 15273098 .
- Viz také Hayflickovy komentáře ke knize Meredith Wadmanovy „The Vaccine Race: Science, Politics and the Human Costs of Defease Disease“, 2017 Chyby v knize „The Vaccine Race“