Nitrace - Nitration
V organické chemii je nitrace obecnou třídou chemických procesů pro zavedení nitroskupiny do organické sloučeniny . Termín je také aplikován nesprávně na jiný proces formování dusičnanů esterů mezi alkoholy a kyseliny dusičné (jako je tomu v syntéze z nitroglycerinu ). Rozdíl mezi výslednými molekulárními strukturami nitrosloučenin a dusičnanů spočívá v tom, že atom dusíku v nitrosloučeninách je přímo vázánna non kyslíku atomu (obvykle uhlíku nebo jiný atom dusíku), zatímco na estery dusičnanů (nazývané také organické nitráty), dusík je vázán k atomu kyslíku, který je zase obvykle je vázán na atom uhlíku (nitrito skupina).
Existuje mnoho hlavních průmyslových aplikací nitrace v přísném smyslu; objemově nejdůležitější jsou pro výrobu nitroaromatických sloučenin, jako je nitrobenzen . Nitrační reakce se používají zejména pro výrobu výbušnin, například pro konverzi guanidinu na nitroguanidin a konverzi toluenu na trinitrotoluen (TNT). Mají však velký význam jako chemické meziprodukty a prekurzory . Ročně se vyrobí miliony tun nitroaromatiky.
Aromatická nitrace
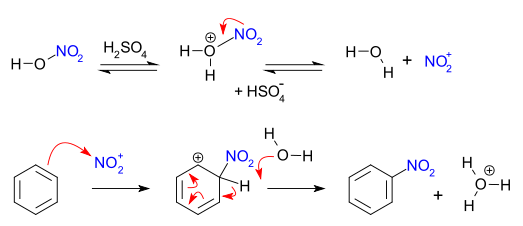
Typické nitrační syntézy používají takzvanou „směsnou kyselinu“, směs koncentrované kyseliny dusičné a kyselin sírové . Tato směs produkuje nitroniový iont (NO 2 + ), což je aktivní látka v aromatické nitraci . Tato aktivní složka, kterou lze izolovat v případě tetrafluoroboritanu nitroničitého , také působí nitraci bez potřeby smíšené kyseliny. Při syntézách směsných kyselin se kyselina sírová nespotřebovává, a proto působí jako katalyzátor i jako absorbent vody. V případě nitrace benzenu se reakce provádí za teplé teploty nepřesahující 50 ° C. Tento proces je jedním příkladem elektrofilní aromatické substituce , která zahrnuje útok benzenovým kruhem bohatým na elektrony :
Byly také navrženy alternativní mechanismy, včetně jednoho zahrnujícího přenos jednoho elektronu (SET).
Rozsah
Selektivita může být výzvou při nitracích, protože zpravidla může vzniknout více než jedna sloučenina, ale je požadována pouze jedna, takže alternativní produkty působí jako kontaminující látky nebo se jednoduše plýtvají. V souladu s tím je žádoucí navrhnout syntézy s vhodnou selektivitou; například kontrolou reakčních podmínek lze fluorenon selektivně trinitrovat nebo tetranitrovat.
Substituenty na aromatických kruzích ovlivňují rychlost této elektrofilní aromatické substituce . Deaktivační skupiny, jako jsou jiné nitroskupiny, mají účinek odebírající elektrony. Takové skupiny deaktivují (zpomalují) reakci a směřují elektrofilní nitroniový iont k útoku na aromatickou meta pozici . Deaktivující metadměrující substituenty zahrnují sulfonyl , kyanoskupiny , keto , estery a karboxyláty . Nitraci lze urychlit aktivací skupin, jako jsou aminoskupiny , hydroxylové a methylové skupiny, také amidů a etherů, což vede k para a orto izomerům.
Přímá nitrace anilinu s kyselinou dusičnou a kyselinou sírovou , podle jednoho zdroje, výsledky v 50/50 směsi para - a meta -nitroanilinu izomerů. V této reakci existuje rychle reagující a aktivující anilin (ArNH 2 ) v rovnováze s hojnějším, ale méně reaktivním (deaktivovaným) aniliniovým iontem (ArNH 3 + ), což může vysvětlit distribuci tohoto reakčního produktu. Podle jiného zdroje začíná kontrolovanější nitrace anilinu tvorbou acetanilidu reakcí s anhydridem kyseliny octové, po níž následuje skutečná nitrace. Protože amid je pravidelná aktivační skupina, tvoří se produkty para a orto izomery. Zahřívání reakční směsi je dostatečné k hydrolyzaci amidu zpět na nitrovaný anilin.
V reakci Wolffenstein-Böters , benzen reaguje s kyselinou dusičnou a dusičnan rtuti (II) za vzniku kyseliny pikrové .
Ipso nitrace
S arylchloridy , trifláty a nonafláty může substituce ipso probíhat také v takzvané nitraci ipso . Fráze byl poprvé použit Perrin a Skinner v roce 1971 ve vyšetřování chloranisol nitraci V jednom protokolu, 4-chlor- N -butylbenzene se nechá reagovat s dusitanu sodného v t -butanolu v přítomnosti 0,5 mol% Pd 2 (dba) 3 biarylfosfinový ligand a katalyzátor fázového přenosu na 4-nitro- n -butylbenzen.