Enantiomer - Enantiomer
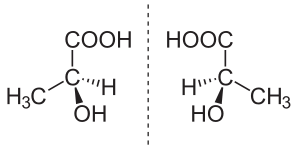
V chemii , An enantiomer ( / ɪ n æ n t i ə m ər , ɛ -, - t i oʊ - / ə- NAN -tee-ə-mər , z řeckého ἐνάντιος (enántios) 'naproti' a μέρος ( méros) „část“) (také nazývaný optický izomer , antipod nebo optický antipod) je jedním ze dvou stereoizomerů, které jsou navzájem zrcadlovými obrazy, které nelze překrývat (nejsou identické), stejně jako zrcadlové obrazy levé a pravé ruky navzájem, které nemohou vypadat identicky jednoduše přeorientováním. Jediný chirální atom nebo podobný strukturní znak ve sloučenině způsobuje, že tato sloučenina má dvě možné struktury, které nelze překrývat, přičemž každá je zrcadlovým obrazem druhé. Každý člen dvojice se nazývá enantiomorf ( enantio = opak; morph = forma); strukturální vlastnost se nazývá enantiomerismus. Přítomnost více chirálních znaků v dané sloučenině zvyšuje počet možných geometrických forem, i když stále mohou existovat nějaké páry dokonalých zrcadlových obrazů.
Vzorek chemikálie je považován za enantiomerní (také nazývaný enantiomerně čistý), pokud má v mezích detekce molekuly pouze jedné chirality .
Pokud jsou přítomny v symetrické prostředí, enantiomery mají stejné chemické a fyzikální vlastnosti kromě pro jejich schopnost otáčet rovinu - polarizovaného světla (+/-) stejným dílem, ale v opačných směrech (i když polarizované světlo může být považována za asymetrický médium). Takové sloučeniny jsou proto popsány jako opticky aktivní , se specifickými termíny pro každý enantiomer na základě směru: pravotočivá sloučenina otáčí světlo ve směru hodinových ručiček (+), zatímco levotočivá sloučenina otáčí světlo proti směru hodinových ručiček (-). Směs stejného počtu obou enantiomerů se nazývá racemická směs nebo racemát . V racemické směsi je množství pozitivní rotace přesně vyváženo stejným množstvím negativní rotace, takže čistá rotace je nulová (směs není opticky aktivní).
Členy enantiomerů mají často různé chemické reakce s jinými enantiomerními látkami. Protože mnoho biologických molekul jsou enantiomery, někdy existuje výrazný rozdíl v účincích dvou enantiomerů na biologické organismy. V drogách je například často pouze jeden z enantiomerů léčiva zodpovědný za požadované fyziologické účinky (označovaný jako eutomer), zatímco druhý enantiomer je méně aktivní, neaktivní nebo někdy dokonce produkuje nežádoucí účinky (označovaný jako distomer). . Díky tomuto objevu lze vyvinout léky složené pouze z jednoho enantiomeru („enantiopure“), aby lék lépe fungoval a někdy odstranil některé vedlejší účinky. Příkladem je eszopiklon (Lunesta), což je pouze jeden enantiomer staršího racemického léku zvaného zopiclon . Toto je typický příklad chirálního přepínače . Jeden enantiomer je zodpovědný za všechny požadované efekty, zatímco druhý enantiomer se zdá být neaktivní, takže dávka eszopiklonu je poloviční oproti zopiclonu.
Při chemické syntéze enantiomerních látek neenantiomerní prekurzory nevyhnutelně produkují racemické směsi. Při absenci účinného enantiomerního prostředí ( prekurzor , chirální katalyzátor nebo kinetické rozlišení ) není rozdělení racemické směsi na její enantiomerní složky možné, přestože některé racemické směsi spontánně krystalizují ve formě racemického konglomerátu , v němž krystaly enantiomery jsou fyzicky odděleny a mohou být separovány mechanicky (např. enantiomery kyseliny vinné, jejichž krystalizované enantiomery byly odděleny pinzetou od Pasteura ). Většina racemátů však bude krystalizovat v krystalech obsahujících oba enantiomery v poměru 1: 1, uspořádaných v pravidelné mřížce.
Konvence pojmenování
Systém R/S je důležitý nomenklaturní systém používaný k označení odlišných enantiomerů. Jiný systém pojmenování používá předpony (+)- a (-)- k označení optické aktivity enantiomeru. (Předpony d - a l - jsou zastaralá synonyma pro (+) - a ( -) -). Latinská slova pro levici jsou laevus a zlověstná a slovo pro pravé je dexter (nebo rectus ve smyslu správného nebo ctnostného). Anglické slovo doprava je příbuzný z rectus . Toto je původ zápisů L/D a S/R a použití předpon levo- a dextro- v běžných jménech .
Předpona ent- na chemický název může být použit k označení chemické látky, která je enantiomer jeden název napovídá.
Chirality centra

Molekula je chirální, a proto má enantiomer, pokud nemá symetrii odrazu a žádnou nesprávnou rotaci (rotoreflexní) symetrii. Společnou charakteristikou chirality je přítomnost asymetrického atomu uhlíku , který má vazby na čtyři různé atomy nebo skupiny, takže tyto skupiny mohou být uspořádány dvěma různými způsoby, které nejsou superposable. Mít enantiomer na základě asymetrického atomu uhlíku (nebo asymetricky vázaného atomu jakéhokoli prvku) představuje běžný typ chirality, nazývaný bodová chiralita nebo centrální chiralita . Asymetrický atom se nazývá centrum chirality , typ stereocentra . Sloučeniny, které obsahují přesně jeden (nebo libovolný lichý počet) asymetrických atomů, jsou vždy chirální. Sloučeninám, které obsahují sudý počet asymetrických atomů, však někdy chybí chiralita, protože jsou uspořádány v zrcadlově symetrických párech a jsou známé jako meso sloučeniny . Například kyselina meso vinná (zobrazená vpravo) má dva asymetrické atomy uhlíku, ale nevykazuje enantiomerismus, protože existuje zrcadlová symetrická rovina. Naopak existují formy chirality, které nevyžadují asymetrické atomy, jako je axiální , planární a šroubovicová chiralita.
Přestože chirální molekule chybí symetrie odrazu (C s ) a rotačního odrazu (S 2 n ), může mít i jiné molekulární symetrie a její symetrie je popsána jednou ze skupin chirálních bodů : C n , D n , T, O, nebo I. Například peroxid vodíku je chirální a má C 2 (dvojnásobně rotační) symetrii. Běžným chirálním případem je bodová skupina C 1 , což znamená žádné symetrie, což platí pro kyselinu mléčnou.
Příklady
Příkladem takového enantiomeru je sedativní thalidomid , který se prodával v řadě zemí po celém světě od roku 1957 do roku 1961. Byl stažen z trhu, když se zjistilo, že způsobuje vrozené vady. Jeden enantiomer způsobil žádoucí sedativní účinky, zatímco druhý, nevyhnutelně přítomný ve stejném množství, způsobil vrozené vady.
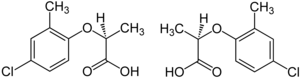
Herbicid mecoprop je racemická směs, s ( R ) - (+) - enantiomer ( "Mecoprop-P", "Duplosan KV") majících herbicidní účinnost.
Dalším příkladem jsou antidepresiva escitalopram a citalopram . Citalopram je racemát [1: 1 směs ( S ) -citalopramu a ( R ) -citalopramu]; escitalopram [( S ) -citalopram] je čistý enantiomer. Dávky escitalopramu jsou typicky 1/2 dávky citalopramu. Zde (S) -citalopram se nazývá chirální spínač Citalopramu.
Enantioselektivní přípravky
Pro přípravu enantiočistých sloučenin existují dvě hlavní strategie. První je známý jako chirální rozlišení. Tento způsob zahrnuje přípravu sloučeniny v racemické formě a její rozdělení na její izomery. Ve své průkopnické práci dokázal Louis Pasteur izolovat izomery kyseliny vinné, protože krystalizují z roztoku jako krystaly, každý s jinou symetrií. Méně obvyklou metodou je enantiomerová autodepporace .
Druhou strategií je asymetrická syntéza: použití různých technik k přípravě požadované sloučeniny ve vysokém enantiomerním přebytku . Zahrnuté techniky zahrnují použití chirálních výchozích materiálů ( syntéza chirálního poolu ), použití chirálních pomocných látek a chirálních katalyzátorů a aplikace asymetrické indukce . Požadovanou sloučeninu může také připravit použití enzymů ( biokatalýza ).
Třetí strategií je enantiokonvergentní syntéza , syntéza jednoho enantiomeru z racemického prekurzoru, využívající oba enantiomery. Použitím chirálního katalyzátoru vedou oba enantiomery reakčního činidla k jednomu enantiomeru produktu.
Enantiomery nemusí být izolovatelné, pokud existuje dostupná cesta pro racemizaci (interkonverze mezi enantiomorfy za vzniku racemické směsi) při dané teplotě a časovém měřítku. Například aminy se třemi odlišnými substituenty jsou chirální, ale až na několik výjimek (např. Substituované N -chloraziridiny) rychle procházejí " deštníkovou inverzí " při pokojové teplotě, což vede k racemizaci. Pokud je racemizace dostatečně rychlá, lze s molekulou často zacházet jako s achirální průměrovanou strukturou.
Enantiočisté léky
Pokroky v průmyslových chemických procesech učinily ekonomickými pro farmaceutické výrobce brát léky, které byly původně uváděny na trh jako racemická směs, a uvádět na trh jednotlivé enantiomery. Tato strategie prodeje chirálně specifického léčiva z již schváleného a existujícího racemického léčiva se obvykle provádí pro lepší terapeutickou účinnost. Tento druh přechodu z racemického léčiva na léčivo enantiomerní se nazývá chirální spínač a tento proces se nazývá chirální přepínání. V některých případech mají enantiomery skutečně odlišné účinky. Zajímavým případem je propoxyfen. Enantiomerní pár propoxyfenu prodává samostatně společnost Eli Lilly a společnost. Jedním z partnerů je dextropropoxyfen, analgetikum (Darvon) a druhý se nazývá levopropoxyfen, účinné antitusikum (Novrad). Je zajímavé poznamenat, že obchodní názvy drog, DARVON a NOVRAD, také odrážejí vztah chemického zrcadlového obrazu. V ostatních případech nemusí být pro pacienta žádný klinický přínos. V některých jurisdikcích jsou léky s jedním enantiomerem patentovatelné odděleně od racemické směsi. Je možné, že je aktivní pouze jeden z enantiomerů. Nebo je možné, že jsou aktivní obě, v takovém případě nemá oddělení směsi žádné objektivní výhody, ale prodlužuje patentovatelnost léčiva.
Porušení parity
Pro všechny záměry a účely má každý enantiomer v páru stejnou energii. Nicméně, teoretická fyzika předpovídá, že kvůli parity porušení této slabé jaderné síly (jediná síla v přírodě, které mohou „Řekni doleva zprava“), tam je vlastně minutu rozdíl v energii mezi enantiomery (v řádu 10 -12 eV nebo 10 −10 kJ/mol nebo méně) v důsledku mechanismu slabého neutrálního proudu . Tento rozdíl v energii je mnohem menší než energetické změny způsobené i malými změnami molekulární konformace a příliš malý na to, aby je bylo možné měřit současnou technologií, a je proto chemicky bezvýznamný. Ve smyslu, který používají částicoví fyzici, je „pravý“ enantiomer molekuly, který má přesně stejný obsah hmotnostní energie jako původní molekula, zrcadlovým obrazem, který je také postaven z antihmoty (antiprotony, antineutrony a pozitrony) . V celém tomto článku je „enantiomer“ používán pouze v chemickém smyslu pro sloučeniny běžné hmoty, které nelze na jejich zrcadlovém obrazu překrýt.
kvazi -enantiomerů
Kvazi -enantiomery jsou molekulární druhy, které nejsou striktně enantiomery, ale chovají se, jako by byly. Kvazi enantiomerů mají použití v paralelním kinetického štěpení .
Viz také
Reference
externí odkazy
-
 Média související s enantiomery na Wikimedia Commons
Média související s enantiomery na Wikimedia Commons - chemwiki: stereoizomerismus

