Fenyllithium - Phenyllithium
|
|
| Jména | |
|---|---|
|
Systematický název IUPAC
Fenyllithium |
|
| Ostatní jména
Lithiobenzen
|
|
| Identifikátory | |
|
3D model ( JSmol )
|
|
| Zkratky | LiPh, PhLi |
| 506502 | |
| ČEBI | |
| ChemSpider | |
| Informační karta ECHA |
100,008,838 |
| Číslo ES | |
| 2849 | |
| Pletivo | fenyllithium |
|
PubChem CID
|
|
|
CompTox Dashboard ( EPA )
|
|
|
|
|
|
| Vlastnosti | |
|
LiC 6H 5 |
|
| Molární hmotnost | 84,045 g mol −1 |
| Vzhled | Bezbarvé krystaly |
| Hustota | 828 mg cm −3 |
| Bod varu | 140 až 143 ° C (284 až 289 ° F; 413 až 416 K) |
| Reaguje | |
| Termochemie | |
|
Standardní entalpie
tvorby (Δ f H ⦵ 298 ) |
48,3-52,5 kJ mol −1 |
| Nebezpečí | |
| Bezpečnostní list | Externí bezpečnostní list |
| R-věty (zastaralé) | R14 , R17 , R23/24/25 , R48 |
| S-věty (zastaralé) | (S1/2) , S8 , S9 , S16 , S26 , S30 , S46 , S36/37/39 , S45 |
| Související sloučeniny | |
|
Související sloučeniny
|
fenyl měď , fenylsod , fenylcobalt |
|
Pokud není uvedeno jinak, jsou údaje uvedeny pro materiály ve standardním stavu (při 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Reference na infobox | |
Fenyllithium nebo lithobenzen je organokovové činidlo s empirickým vzorcem C 6 H 5 Li. Nejčastěji se používá jako metalizační činidlo v organických syntézách a jako náhrada za Grignardova činidla pro zavádění fenylových skupin do organických syntéz. Krystalické fenyllithium je bezbarvé; roztoky fenyllithia však mají různé odstíny hnědé nebo červené v závislosti na použitém rozpouštědle a nečistotách přítomných v rozpuštěné látce.
Příprava
Fenyllithium byl nejprve vyroben reakcí kovového lithia s diphenylmercury :
- (C 6 Η 5 ) 2 Ηg + 2Li → 2C 6 Η 5 Li + Ηg
Reakcí fenylhalogenidu s kovem lithia vzniká fenyllithium:
- X-Ph + 2Li → Ph-Li + LiX
Fenyllithium lze také syntetizovat výměnou kov-halogen:
- n-BuLi + X-Ph → n-BuX + Ph-Li
Převládající metodou výroby fenyllithia jsou dnes dvě poslední syntézy.
Reakce
Primárním použitím PhLi je usnadnit tvorbu vazeb uhlík-uhlík pomocí nukleofilních adičních a substitučních reakcí:
- PhLi + R 2 C = O → PhR 2 COLi
2-Fenylpyridin se připravuje reakcí fenyllithia s pyridinem, což je proces, který zahrnuje cestu adiční eliminace:
- C 6 H 5 Li + C 5 H 5 N → C 6 H 5 -C 5 H 4 N + LiH
Struktura a vlastnosti
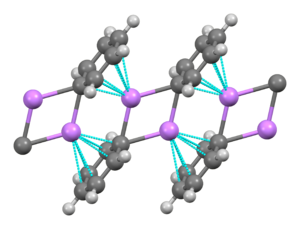
Fenyllithium je organolithná sloučenina, která tvoří monoklinické krystaly. Pevné fenyllithium lze popsat jako sestávající z dimerních Li 2 Ph 2 podjednotek. Atomy Li a ipso uhlíky fenylových kruhů tvoří planární čtyřčlenný kruh. Rovina fenylových skupin je kolmá na rovinu tohoto kruhu Li 2 C 2 . Mezi těmito fenyllithiovými dimery a n-elektrony fenylových skupin v sousedních dimerech dochází k další silné intermolekulární vazbě, což má za následek nekonečnou polymerní strukturu žebříku.
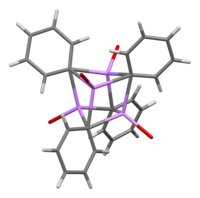
V roztoku je zapotřebí různých struktur závislých na organickém rozpouštědle. V tetrahydrofuranu ekvilibruje mezi monomerními a dimerními stavy. V etheru, jak se běžně prodává, existuje fenyllithium jako tetramer. Čtyři atomy Li a čtyři centra uhlíku ipso zaujímají střídající se vrcholy zkreslené krychle. Ph
Délky vazby C – Li jsou v průměru 2,33 Å. Molekula etheru se váže na každé z míst Li prostřednictvím svého kyslíkového atomu. V přítomnosti LiBr, vedlejší produkt přímo reakci lithia s fenylovým halogenidem, v [(Phli • Et 2 O) 4 ] komplex namísto stane [(Phli • Et 2 O) 3 • LiBr). Atom Li LiBr zaujímá jedno z lithiových míst v klastru kubánského typu a atom Br sedí v sousedním uhlíkovém místě.