Polyedrická teorie párových elektronových párů - Polyhedral skeletal electron pair theory
V chemii mnohostěnný kosterní teorie dvojice elektronů (PSEPT) poskytuje počítání elektronového pravidla užitečné pro předpovídání struktury klastrů , jako je boran a carborane klastrů. Pravidla pro počítání elektronů původně formuloval Kenneth Wade a dále je rozvíjel Michael Mingos a další; oni jsou někdy známé jako pravidla Wade nebo pravidel Wade-Mingos . Pravidla jsou založena na molekulárním orbitálním ošetření vazby. Tato pravidla byla rozšířena a sjednoceny v podobě Jemmis MNO pravidel .
Predikce struktur klastrových sloučenin
V závislosti na počtu elektronů na vrchol jsou vyvolána různá pravidla (4 n , 5 n nebo 6 n ).
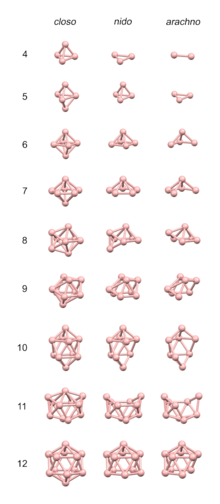
Pravidla 4 n jsou přiměřeně přesná při předpovídání struktur klastrů, které mají asi 4 elektrony na vrchol, jako je tomu v případě mnoha boranů a karboranů . U takovýchto klastrů jsou struktury založeny na deltahedře , což jsou mnohostěny, ve kterých je každá plocha trojúhelníková. 4 n klastry jsou klasifikovány jako closo- , nido- , arachno- nebo hypho- podle toho, zda představují úplný ( closo- ) deltahedron nebo deltahedron, kterému chybí jeden ( nido- ), dva ( arachno- ) nebo tři ( hypho- ) vrcholy.
Hypho klastry jsou však relativně neobvyklé kvůli tomu, že počet elektronů je dostatečně vysoký na to, aby začal zaplňovat sousedící orbitaly a destabilizovat 4 n strukturu. Pokud se počet elektronů blíží 5 elektronům na vrchol, struktura se často změní na strukturu, která se řídí pravidly 5n, která jsou založena na 3-připojené mnohostěně.
Jak se počet elektronů dále zvyšuje, struktury klastrů s počtem elektronů 5n jsou nestabilní, takže lze implementovat 6 n pravidel. Klastry 6 n mají struktury založené na prstencích.
K racionalizaci vazby klastrových sloučenin typů 4 n , 5 n a 6 n lze použít molekulární orbitální ošetření .
4 n pravidla
Následující mnohostěn je closo mnohostěn a je základem pro pravidla 4 n ; každý z nich má trojúhelníkové tváře. Počet vrcholů v klastru určuje, na jakém mnohostěnu je struktura založena.
| Počet vrcholů | Mnohostěn |
|---|---|
| 4 | Čtyřstěn |
| 5 | Trigonální bipyramid |
| 6 | Osmistěn |
| 7 | Pentagonální bipyramid |
| 8 | D 2d (trigonální) dodecahedron ( urážlivý disphenoid ) |
| 9 | Zúžený trigonální hranol |
| 10 | Bezbariérový čtvercový antiprism |
| 11 | Edge-contracted icosahedron (octadecahedron) |
| 12 | Dvacetistěn (bicapped pětiúhelníkové antiprism) |
Pomocí počtu elektronů lze najít predikovanou strukturu. n je počet vrcholů v klastru. 4 n pravidla jsou vyjmenována v následující tabulce.
| Počet elektronů | název | Předvídaná struktura |
|---|---|---|
| 4 n - 2 | Postižené closo | n - 2 vrcholový klonovaný mnohostěn se 2 uzavřenými ( zvětšenými ) plochami |
| 4 n | Capped closo | n - 1 vrcholový mnohostranný mnohostěn s 1 čelem zakončeným |
| 4 n + 2 | closo | closo mnohostěn s n vrcholy |
| 4 n + 4 | nido | n + 1 mnohostěn vrcholového klonu s 1 chybějícím vrcholem |
| 4n + 6 | arachno | n + 2 mnohostěn vrcholového klosu se 2 chybějícími vrcholy |
| 4n + 8 | hypho | n + 3 vrcholový closo mnohostěn se 3 chybějícími vrcholy |
| 4n + 10 | klado | n + 4 vrcholový closo mnohostěn se 4 chybějícími vrcholy |
Při počítání elektronů pro každý klastr je uveden počet valenčních elektronů . Pro každý přítomný přechodový kov se odečte 10 elektronů od celkového počtu elektronů. Například v Rh 6 (CO) 16 by celkový počet elektronů byl 6 × 9 + 16 × 2 - 6 × 10 = 86 - 60 = 26. Proto je klastr klozovým polyhedronem, protože n = 6 , se 4 n + 2 = 26 .
Při předpovídání struktury klastrů lze vzít v úvahu i jiná pravidla:
- U klastrů sestávajících převážně z přechodných kovů jsou všechny přítomné prvky hlavní skupiny často nejlépe počítány jako ligandy nebo intersticiální atomy, nikoli jako vrcholy.
- Větší a elektropozitivní atomy mají tendenci zabírat vrcholy s vysokou konektivitou a menší elektronegativnější atomy mají tendenci zabírat vrcholy s nízkou konektivitou.
- Ve zvláštním případě klastrů hydridu bóru má každý atom boru spojený se 3 nebo více vrcholy jeden koncový hydrid, zatímco atom boru spojený se dvěma dalšími vrcholy má dva koncové atomy vodíku. Pokud je přítomno více atomů vodíku, jsou umístěny do otevřených čelních poloh, aby se vyrovnal koordinační počet vrcholů.
- Pro zvláštní případ klastrů přechodných kovů se do kovových center přidávají ligandy, aby kovy získaly přiměřená koordinační čísla, a pokud jsou přítomny nějaké atomy vodíku , jsou umístěny do přemosťovacích poloh, aby se koordinační čísla vrcholů vyrovnala.
Obecně platí, že struktury klona s n vrcholy jsou n -vrcholná mnohostěn.
Pro předpověď strukturu Nido clusteru closo clusteru s n + 1 vrcholů je použit jako výchozí bod; pokud je klastr složen z malých atomů, je odstraněn vrchol s vysokou konektivitou, zatímco pokud je klastr složen z velkých atomů, je odstraněn vrchol s nízkou konektivitou.
Pro předpověď strukturu Arachno clusteru closo mnohostěn s n + 2 vrcholy se používá jako výchozí bod, a n + 1 vrchol nido komplex je generován po pravidlo výše; druhý vrchol sousedící s prvním je odstraněn, pokud je shluk složen převážně z malých atomů, druhý vrchol nesousedící s prvním je odstraněn, pokud je shluk složen převážně z velkých atomů.
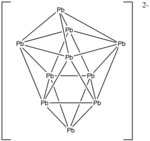
Příklad: Pb2-
10
- Počet elektronů: 10 × Pb + 2 (pro záporný náboj) = 10 × 4 + 2 = 42 elektronů.
- Vzhledem k tomu, že n = 10, 4 n + 2 = 42, je klastr closo bicapped square antiprism.
Příklad: S.2+
4
- Počet elektronů: 4 × S - 2 (pro kladný náboj) = 4 × 6 - 2 = 22 elektronů.
- Protože n = 4, 4 n + 6 = 22, je kupa arachno .
- Počínaje osmistěnem je odstraněn vrchol vysoké konektivity a poté je odstraněn nesousedící vrchol.
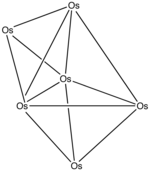
Příklad: Os 6 (CO) 18
- Počet elektronů: 6 × Os + 18 × CO - 60 (pro 6 atomů osmiia) = 6 × 8 + 18 × 2-60 = 24
- Protože n = 6, 4 n = 24, je klastr uzavřen closo .
- Počínaje trigonálním bipyramidem je obličej uzavřen. Karbonyly byly pro přehlednost vynechány.
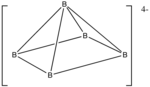
Příklad: B
5H4-
5
- Počet elektronů: 5 × B + 5 × H + 4 (pro záporný náboj) = 5 × 3 + 5 × 1 + 4 = 24
- Protože n = 5, 4 n + 4 = 24, tak klastr je nido.
- Počínaje osmistěnem je jeden z vrcholů odstraněn.
Pravidla jsou užitečná také při předpovídání struktury karboranů . Příklad: C 2 B 7 H 13
- Počet elektronů = 2 × C + 7 × B + 13 × H = 2 × 4 + 3 × 7 + 13 × 1 = 42
- Protože n v tomto případě je 9, 4 n + 6 = 42, shluk je arachno .
Účetnictví deltahedrických klastrů se někdy provádí počítáním kosterních elektronů místo celkového počtu elektronů. Kosterní orbitální (elektronový pár) a kosterní elektronové počty pro čtyři typy deltahedrických shluků jsou:
- n -vrcholové closo : n + 1 kosterních orbitálů, 2 n + 2 kosterních elektronů
- n -vertex nido : n + 2 kosterní orbitaly, 2 n + 4 kosterní elektrony
- n -vertex Arachno : n + 3 kosterní orbitaly, 2 n + 6 kosterní elektronů
- n -hyptex vrcholu : n + 4 kosterní orbitaly, 2 n + 8 kosterních elektronů
Počty kosterních elektronů jsou určeny součtem následujícího počtu elektronů:
- 2 z každé jednotky BH
- 3 z každé jednotky ÚT
- 1 z každého dalšího atomu vodíku (nad a nad atomy na jednotkách BH a CH)
- elektrony s aniontovým nábojem
5 n pravidel
Jak bylo diskutováno dříve, pravidlo 4 n se zabývá hlavně klastry s počty elektronů 4 n + k , ve kterých jsou na každém vrcholu přibližně 4 elektrony . Jak se přidává více elektronů na vrchol, počet elektronů na vrchol se blíží 5. Spíše než k přijímání struktur založených na deltahedře mají klastry typu 5n struktury založené na jiné sérii mnohostěnů známých jako 3-připojené mnohostěny , ve kterých každý vrchol je spojen se 3 dalšími vrcholy. Tyto 3-připojené mnohostěn jsou duals z deltahedra. Níže jsou uvedeny běžné typy 3-spojených mnohostěnů.
| Počet vrcholů | Typ 3-připojeného mnohostěnu |
|---|---|
| 4 | Čtyřstěn |
| 6 | Trigonální hranol |
| 8 | Krychle |
| 10 | Pentagonální hranol |
| 12 | D 2d pseudo-octahedron (dual of snub disphenoid) |
| 14 | Duál trojúhelníkového trojúhelníkového hranolu (K 5 asociatedron ) |
| 16 | Čtvercový komolý lichoběžník |
| 18 | Duál ikosahedronu s kontrahováním hran |
| 20 | Dodecahedron |
Pravidla 5 n jsou následující.
| Celkový počet elektronů | Předvídaná struktura |
|---|---|
| 5 n | n -vrchol 3 -spojený mnohostěn |
| 5 n + 1 | n -1 vrchol 3-spojený mnohostěn s jedním vrcholem vloženým do hrany |
| 5 n + 2 | n -2 vrchol 3-spojený mnohostěn se dvěma vrcholy vloženými do hran |
| 5 n + k | n - k vrchol 3-spojený mnohostěn s k vrcholy vloženými do hran |
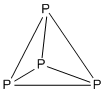
Příklad: P 4
- Počet elektronů: 4 × P = 4 × 5 = 20
- Jedná se o 5 n strukturu s n = 4, je tedy čtyřboká
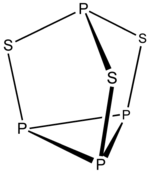
Příklad: P 4 S 3
- Počet elektronů 4 × P + 3 × S = 4 × 5 + 3 × 6 = 38
- Jedná se o strukturu 5 n + 3 s n = 7. Do okrajů jsou vloženy tři vrcholy
Příklad: P 4 O 6
- Počet elektronů 4 × P + 6 × O = 4 × 5 + 6 × 6 = 56
- Jedná se o strukturu 5 n + 6 s n = 10. Do hran je vloženo šest vrcholů
6 n pravidel
Jak se do 5 n shluku přidává více elektronů , počet elektronů na vrchol se blíží 6. Místo přijetí struktur založených na 4 n nebo 5 n pravidlech mají klastry obvykle struktury řízené pravidly 6 n , které jsou založeny na prsteny. Pravidla pro 6 n struktur jsou následující.
| Celkový počet elektronů | Předvídaná struktura |
|---|---|
| 6 n - k | n -členěný prsten s k ⁄ 2 transanulárních vazeb |
| 6 n - 4 | n -členěný prsten se 2 transanulárními vazbami |
| 6 n - 2 | n -členěný prsten s 1 transanulární vazbou |
| 6 n | n -členěný prsten |
| 6 n + 2 | n -členěný řetěz ( n -členěný prsten s 1 přerušeným svazkem) |
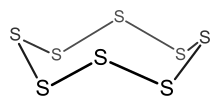
Příklad: S 8
- Počet elektronů = 8 × S = 8 × 6 = 48 elektronů.
- Protože n = 8, 6 n = 48, je tedy klastr 8členným prstencem.
Hexan (C 6 H 14 )
- Počet elektronů = 6 × C + 14 × H = 6 × 4 + 14 × 1 = 38
- Protože n = 6, 6 n = 36 a 6 n + 2 = 38, je klastr šestičlenný řetězec.
Isolobální vrcholové jednotky
Za předpokladu, že jednotka vrcholu je isolobální s BH, pak může být v zásadě alespoň nahrazena jednotkou BH, i když BH a CH nejsou izoelektronické. Jednotka CH + je izolobální, proto se pravidla vztahují na karborany. To lze vysvětlit díky hraniční orbitální léčbě. Kromě toho existují izolobální jednotky přechodových kovů. Například Fe (CO) 3 poskytuje 2 elektrony. Odvození je stručně následující:
- Fe má 8 valenčních elektronů.
- Každá karbonylová skupina je čistým donorem 2 elektronů poté, co se při vytváření 14 elektronů vezme v úvahu vnitřní vazba σ - a π .
- 3 páry jsou považovány za zapojené do Fe – CO σ -vazeb a 3 páry jsou zapojeny do π -zpětného spojení z Fe na CO, což snižuje 14 na 2.
Lepení v klastrových sloučeninách
-
closo - B
6H2-
6
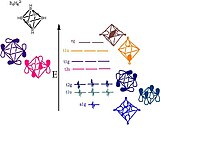
- Atomy boru leží na každém vrcholu osmistěnu a jsou sp hybridizovány. Jeden sp-hybrid vyzařuje ze struktury tvořící vazbu s atomem vodíku. Druhý sp-hybrid vyzařuje do středu struktury a tvoří ve středu klastru velký vazebný molekulární orbitál. Zbývající dva nehybridizované orbitaly leží podél tangenty struktury podobné kouli a vytvářejí více spojovacích a nevázaných orbitálů mezi bórovými vrcholy. Orbitální diagram se rozpadá následovně:
- 18 rámcových molekulárních orbitálů (MO), odvozených od 18 atomů orbitalu boru, jsou:
- 1 spojovací MO ve středu klastru a 5 antibondických MO ze 6 sp-radiálních hybridních orbitálů
- 6 spojovacích MO a 6 antibondických MO z 12 tangenciálních p-orbitálů.
- 18 rámcových molekulárních orbitálů (MO), odvozených od 18 atomů orbitalu boru, jsou:
- Celkový počet orbitálů kosterních vazeb je tedy 7, tj. N + 1 .
Přechodové kovové klastry
Klastry přechodových kovů používají k spojování d orbitaly . Mají tedy až devět spojovacích orbitálů, namísto pouze čtyř přítomných v klastrech bóru a hlavní skupiny.
Shluky s intersticiálními atomy
Vzhledem ke svým velkým poloměrům tvoří přechodové kovy obvykle shluky, které jsou větší než prvky hlavní skupiny. Jedním z důsledků jejich zvýšené velikosti jsou, že tyto klastry často obsahují ve svých centrech atomy. Významným příkladem je [Fe 6 C (CO) 16 ] 2- . V takových případech pravidla počítání elektronů předpokládají, že intersticiální atom přispívá všemi valenčními elektrony ke klastrové vazbě. Tímto způsobem je [Fe 6 C (CO) 16 ] 2- ekvivalentní [Fe 6 (CO) 16 ] 6- nebo [Fe 6 (CO) 18 ] 2- .
Reference
Obecné reference
- Greenwood, Norman N .; Earnshaw, Alan (1997). Chemistry of the Elements (2. vyd.). Butterworth-Heinemann . ISBN 978-0-08-037941-8.
- Cotton, F. Albert ; Wilkinson, Geoffrey ; Murillo, Carlos A .; Bochmann, Manfred (1999), Advanced Anorganic Chemistry (6. ed.), New York: Wiley-Interscience, ISBN 0-471-19957-5