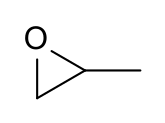
Propylenoxid - Propylene oxide
|
|

|
|
| Jména | |
|---|---|
|
Preferovaný název IUPAC
(2R) -2-methyloxiran (2S) -2-methyloxiran |
|
| Ostatní jména
Propylenoxid
epoxypropan Propylen epoxidu 1,2-propylenoxid methyl oxiranu 1,2-epoxypropan propenu oxid methyl ethylenoxidu oxid methylethylenovou |
|
| Identifikátory | |
|
3D model ( JSmol )
|
|
| ChEBI | |
| ChemSpider | |
| Informační karta ECHA |
100 000 800 |
| Číslo ES | |
| KEGG | |
|
PubChem CID
|
|
| UNII | |
|
Řídicí panel CompTox ( EPA )
|
|
|
|
|
|
| Vlastnosti | |
| C 3 H 6 O | |
| Molární hmotnost | 58,080 g · mol -1 |
| Vzhled | Bezbarvá kapalina |
| Zápach | jako benzen |
| Hustota | 0,859 g / cm 3 |
| Bod tání | -111,9 ° C (-169,4 ° F; 161,2 K) |
| Bod varu | 35 ° C (95 ° F; 308 K) |
| 41% (20 ° C) | |
| Tlak páry | 445 mmHg (20 ° C) |
| −4,25 × 10 −5 cm 3 / mol | |
|
Index lomu ( n D )
|
1,3660 |
| Termochemie | |
|
Tepelná kapacita ( C )
|
120,4 J · (K · mol) -1 |
|
Standardní molární
entropie ( S |
196,5 J · (K · mol) -1 |
|
Std entalpie
formace (Δ f H ⦵ 298 ) |
−123,0 kJ · mol −1 |
| Nebezpečí | |
| Hlavní rizika | Extrémně hořlavý |
| Piktogramy GHS |
  
|
| Signální slovo GHS | Nebezpečí |
| NFPA 704 (ohnivý diamant) | |
| Bod vzplanutí | -37 ° C (-35 ° F; 236 K) |
| 747 ° C (1377 ° F; 1020 K) | |
| Výbušné limity | 2,3–36% |
| Smrtelná dávka nebo koncentrace (LD, LC): | |
|
LD 50 ( střední dávka )
|
660 mg / kg (morče, orální) 380 mg / kg (krysa, orální) 440 mg / kg (myš, orální) 1140 mg / kg (krysa, orální) 690 mg / kg (morče, orální) |
|
LC 50 ( střední koncentrace )
|
1740 ppm (myš, 4 h) 4000 ppm (krysa, 4 h) |
|
LC Lo ( zveřejněno nejnižší )
|
2005 ppm (pes, 4 h) 4000 ppm (morče, 4 h) |
| NIOSH (limity expozice USA pro zdraví): | |
|
PEL (přípustné)
|
PEL 100 ppm (240 mg / m 3 ) |
|
REL (doporučeno)
|
Ca. |
|
IDLH (okamžité nebezpečí)
|
Ca [400 ppm] |
|
Pokud není uvedeno jinak, jsou uvedeny údaje o materiálech v jejich standardním stavu (při 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Reference Infoboxu | |
Propylenoxid je organická sloučenina s molekulárním vzorcem CH 3 CH 2 O. Tento bezbarvé těkavé kapaliny s zápach připomínající etheru, se vyrábí ve velkém měřítku průmyslově. Jeho hlavní aplikací je jeho použití pro výrobu polyetherpolyolů pro použití při výrobě polyuretanových plastů. Je to chirální epoxid , i když se běžně používá jako racemická směs .
Tato sloučenina se někdy nazývá 1,2-propylenoxid, aby se odlišila od svého izomeru 1,3-propylenoxidu, lépe známého jako oxetan .
Výroba
Průmyslová výroba propylenoxidu začíná z propylenu . Používají se dva obecné přístupy, jeden zahrnující hydrochlorizaci a druhý zahrnující oxidaci. V roce 2005 se přibližně polovina světové produkce vyráběla technologií chlorohydrinu a polovina oxidačními cestami. Druhý přístup nabývá na významu.
Způsob hydrochlorace
Tradiční cesta probíhá konverzí propenu na propylenchlorhydrin podle následujícího zjednodušeného schématu:
Směs 1-chlor-2-propanolu a 2-chlor-1-propanolu se poté dehydrochloruje. Například:
K absorpci HCl se často používá vápno ( hydroxid vápenatý ) .
Oxidace propylenu
Další obecná cesta k propylenoxidu zahrnuje oxidaci propylenu organickým peroxidem. Reakce sleduje tuto stechiometrii:
- CH 3 CH = CH 2 + RO 2 H → CH 3 CH 2 O + ROH
Proces se praktikuje se čtyřmi hydroperoxidy :
- V Halconově procesu se terc -butylhydroperoxid získává okysličením isobutanu , čímž se získá terc- butanol . Tento koprodukt lze dehydratovat na isobuten, převést na MTBE , přísadu pro benzín .
- Ethylbenzenhydroperoxid odvozený od okysličování ethylbenzenu , který poskytuje 1-fenyletanol. Tento koprodukt lze dehydratovat, čímž se získá styren , užitečný monomer.
- Kumenhydroperoxid odvozený od okysličování kumenu (isopropylbenzenu), který poskytuje kumylalkohol. Pomocí dehydratace a hydrogenace lze tento koprodukt recyklovat zpět na kumen. Tuto technologii komercializovala společnost Sumitomo Chemical.
- Peroxid vodíku je oxidační činidlo v procesu peroxid vodíku na propylenoxid (HPPO), katalyzované titanem dopovaným silikalitem :
- C 3 H 6 + H 2 O 2 → C 3 H 6 O + H 2 O
V zásadě tento proces produkuje pouze vodu, která byla vedlejším produktem. V praxi se generují některé deriváty PO s otevřeným kruhem.
Reakce
Stejně jako ostatní epoxidy, i PO prochází reakcemi otevření kruhu. S vodou se vyrábí propylenglykol. U alkoholů dochází k reakcím, které se nazývají hydroxylpropylace , analogicky k ethoxylaci . Grignardova činidla se přidávají k propylenoxidu za vzniku sekundárních alkoholů.
Některé další reakce propylenoxidu zahrnují:
- Reakce s oxidem hlinitým při 250–260 ° C vede k propionaldehydu a malému množství acetonu .
- Reakce s oxidem stříbrným vede k kyselině octové .
- Reakce s amalgámem sodíku a rtuti a vodou vede k isopropanolu .
Použití
Mezi 60 a 70% veškerého propylenoxidu se převádí na polyetherpolyoly procesem nazývaným alkoxylace . Tyto polyoly jsou stavebními kameny při výrobě polyuretanových plastů. Asi 20% propylenoxidu se hydrolyzuje na propylenglykol procesem, který se urychluje kyselou nebo zásaditou katalýzou . Dalšími hlavními produkty jsou polypropylenglykol , propylenglykolethery a propylenkarbonát .
Niche používá
Fumigant
Úřad pro kontrolu potravin a léčiv USA schválil použití propylenoxidu k pasterizaci surových mandlí počínaje 1. zářím 2007, v reakci na dva případy kontaminace salmonelou v komerčních sadech, k jednomu došlo v Kanadě a jednomu ve Spojených státech. Pistáciové oříšky mohou být také podrobeny propylenoxidu ke kontrole salmonely .
Mikroskopie
Propylenoxid se běžně používá při přípravě biologických vzorků pro elektronovou mikroskopii k odstranění zbytkového ethanolu dříve používaného k dehydrataci. Při typickém postupu se vzorek nejprve ponoří do směsi stejných objemů ethanolu a propylenoxidu na 5 minut a poté čtyřikrát do čistého oxidu, vždy po 10 minutách.
Bezpečnost
Je to potenciální lidský karcinogen a je zařazen do seznamu karcinogenů skupiny IARC skupiny 2B .
Přirozený výskyt
V roce 2016 bylo oznámeno, že propylenoxid byl detekován ve Sagittarius B2 , oblaku plynu v Mléčné dráze o hmotnosti tří milionů slunečních hmot . Je to první chirální molekula, která byla detekována ve vesmíru, i když bez enantiomerního přebytku.
Reference
Citované zdroje
- Haynes, William M., ed. (2011). CRC Handbook of Chemistry and Physics (92. vydání). Boca Raton, FL: Press CRC . ISBN 1439855110.

