Proteinogenní aminokyselina - Proteinogenic amino acid
Proteinogenní aminokyseliny jsou aminokyseliny, které jsou během translace biosynteticky začleněny do proteinů . Slovo „proteinogenní“ znamená „vytvářející bílkoviny“. Během známého života existuje 22 geneticky kódovaných (proteinogenních) aminokyselin, 20 ve standardním genetickém kódu a další 2, které mohou být začleněny speciálními translačními mechanismy.
Naproti tomu neproteinogenní aminokyseliny jsou aminokyseliny, které buď nejsou začleněny do proteinů (jako GABA , L -DOPA nebo trijodthyronin ), jsou chybně začleněny místo geneticky kódované aminokyseliny, nebo nejsou produkovány přímo a izolovaně standardními buněčnými stroje (jako hydroxyprolin ). Ta často vyplývá z posttranslační modifikace proteinů. Některé neproteinogenní aminokyseliny jsou začleněny do nerribozomálních peptidů, které jsou syntetizovány neribozomálními peptidovými syntetázami.
Jak eukaryoty, tak prokaryota mohou do svých proteinů včlenit selenocystein prostřednictvím nukleotidové sekvence známé jako prvek SECIS , která nasměruje buňku k translaci blízkého kodonu UGA jako selenocysteinu (UGA je normálně stop kodon ). U některých methanogenních prokaryot může být kodon UAG (normálně stop kodon) také převeden na pyrrolysin .
V eukaryotech je pouze 21 proteinogenních aminokyselin, 20 standardního genetického kódu, plus selenocystein . Lidé mohou syntetizovat 12 z nich navzájem nebo z jiných molekul intermediárního metabolismu. Zbývajících devět musí být spotřebováno (obvykle jako jejich proteinové deriváty), a proto se jim říká esenciální aminokyseliny . Esenciálními aminokyselinami jsou histidin , isoleucin , leucin , lysin , methionin , fenylalanin , threonin , tryptofan a valin (tj. H, I, L, K, M, F, T, W, V).
Bylo zjištěno, že proteinogenní aminokyseliny souvisejí se souborem aminokyselin, které lze rozeznat pomocí ribozymových autoaminoacylačních systémů. Neproteinogenní aminokyseliny by tedy byly vyloučeny podmíněným evolučním úspěchem forem života na bázi nukleotidů. Byly nabídnuty další důvody k vysvětlení, proč určité specifické neproteinogenní aminokyseliny nejsou obecně začleněny do proteinů; například ornithin a homoserin cyklují proti peptidové páteři a fragmentují protein s relativně krátkými poločasy , zatímco jiné jsou toxické, protože mohou být omylem začleněny do proteinů, jako je například argininový analog kanavanin .
Struktury
Následující text ilustruje struktury a zkratky 21 aminokyselin, které jsou přímo kódovány pro syntézu proteinů genetickým kódem eukaryot. Níže uvedené struktury jsou standardní chemické struktury, nikoli typické formy obojetných iontů, které existují ve vodných roztocích.
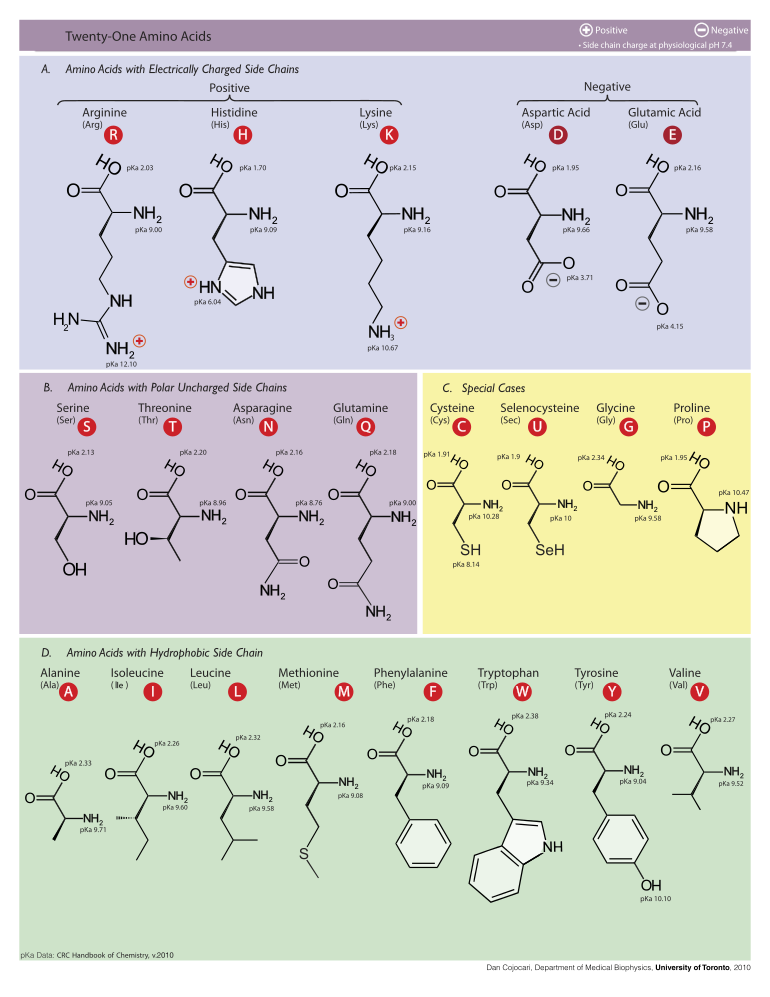
L -alanin
(Ala / A)L -Arginin
(Arg / R)L -Asparagin
(Asn / N)Kyselina L -asparagová
(Asp / D)L -cystein
(Cys / C)Kyselina L -glutamová
(Glu / E)L -glutamin
(Gln / Q)Glycin
(Gly / G)L -histidin
(His / H)L -izoleucin
(Ile / I)L -leucin
(Leu / L)L -lysin
(Lys / K)L -metionin
(met / M)L -fenylalanin
(Phe / F)L -Prolín
(Pro / P)L -Serine
(Ser / S)L -threonin
(Thr / T)L -tryptofan
(Trp / W)L -tyrosin
(Tyr / Y)L -Valine
(Val / V)
IUPAC / IUBMB nyní také doporučuje standardní zkratky pro následující dvě aminokyseliny:
L -Selenocystein
(Sec / U)L -pyrrolysin
(Pyl / O)
Chemické vlastnosti
Následuje tabulka se seznamem jednopísmenných symbolů, třípísmenných symbolů a chemických vlastností postranních řetězců standardních aminokyselin. Uvedené hmotnosti jsou založeny na vážených průměrech elementárních izotopů v jejich přirozeném množství . Vytvoření peptidové vazby vede k eliminaci molekuly vody . Hmotnost proteinu se tedy rovná hmotnosti aminokyselin, z nichž je protein složen z minus 18,01524 Da na peptidovou vazbu.
Obecné chemické vlastnosti
| Aminokyselina | Krátký | Zkratka. | Prům. hmotnost ( Da ) | pI |
pK 1 (α-COOH) |
pK 2 (α- + NH 3 ) |
|---|---|---|---|---|---|---|
| Alanine | A | Ala | 89,09404 | 6.01 | 2.35 | 9,87 |
| Cystein | C | Cys | 121,15404 | 5,05 | 1,92 | 10,70 |
| Kyselina asparagová | D | Asp | 133,10384 | 2,85 | 1,99 | 9,90 |
| Kyselina glutamová | E | Glu | 147,13074 | 3.15 | 2.10 | 9,47 |
| Fenylalanin | F | Phe | 165,19184 | 5,49 | 2.20 | 9,31 |
| Glycin | G | Gly | 75,06714 | 6.06 | 2.35 | 9,78 |
| Histidin | H | Jeho | 155,15634 | 7,60 | 1,80 | 9,33 |
| Isoleucin | Já | Ile | 131,17464 | 6.05 | 2.32 | 9,76 |
| Lysin | K | Lys | 146,18934 | 9,60 | 2.16 | 9.06 |
| Leucin | L | Leu | 131,17464 | 6.01 | 2.33 | 9,74 |
| Methionin | M | Se setkal | 149,20784 | 5,74 | 2.13 | 9.28 |
| Asparagin | N. | Asn | 132,11904 | 5,41 | 2.14 | 8,72 |
| Pyrrolysin | Ó | Pyl | 255,31 | ? | ? | ? |
| Prolin | P | Pro | 115,13194 | 6.30 | 1,95 | 10,64 |
| Glutamin | Otázka | Gln | 146,14594 | 5,65 | 2.17 | 9.13 |
| Arginin | R. | Arg | 174,20274 | 10,76 | 1,82 | 8,99 |
| Serine | S | Ser | 105,09344 | 5,68 | 2.19 | 9.21 |
| Threonin | T | Thr | 119,12034 | 5,60 | 2,09 | 9.10 |
| Selenocystein | U | Sek | 168,053 | 5,47 | 1,91 | 10 |
| Valine | PROTI | Val | 117,14784 | 6,00 | 2.39 | 9,74 |
| Tryptofan | W | Trp | 204,22844 | 5,89 | 2,46 | 9,41 |
| Tyrosin | Y | Tyr | 181,19124 | 5,64 | 2.20 | 9.21 |
Vlastnosti postranního řetězce
| Aminokyselina | Krátký | Zkratka. | Boční řetěz |
hydro- panický |
pKa § | Polární | pH | Malý | Drobný |
Aromatické nebo alifatické |
objem van der Waals (Å 3 ) |
|---|---|---|---|---|---|---|---|---|---|---|---|
| Alanine | A | Ala | -CH 3 |
|
- |
|
- |
|
|
Alifatický | 67 |
| Cystein | C | Cys | -CH 2 SH |
|
8,55 |
|
kyselý |
|
|
- | 86 |
| Kyselina asparagová | D | Asp | -CH 2 COOH |
|
3,67 |
|
kyselý |
|
|
- | 91 |
| Kyselina glutamová | E | Glu | -CH 2 CH 2 COOH |
|
4.25 |
|
kyselý |
|
|
- | 109 |
| Fenylalanin | F | Phe | -CH 2 C 6 H 5 |
|
- |
|
- |
|
|
Aromatický | 135 |
| Glycin | G | Gly | -H |
|
- |
|
- |
|
|
- | 48 |
| Histidin | H | Jeho | -CH 2 - C 3 H 3 N 2 |
|
6,54 |
|
slabý základ |
|
|
Aromatický | 118 |
| Isoleucin | Já | Ile | -CH (CH 3 ) CH 2 CH 3 |
|
- |
|
- |
|
|
Alifatický | 124 |
| Lysin | K | Lys | -(CH 2 ) 4 NH 2 |
|
10,40 |
|
základní |
|
|
- | 135 |
| Leucin | L | Leu | -CH 2 -CH (CH 3 ) 2 |
|
- |
|
- |
|
|
Alifatický | 124 |
| Methionin | M | Se setkal | -CH 2 CH 2 S CH 3 |
|
- |
|
- |
|
|
Alifatický | 124 |
| Asparagin | N. | Asn | -CH 2 CONH 2 |
|
- |
|
- |
|
|
- | 96 |
| Pyrrolysin | Ó | Pyl | -(CH 2 ) 4 NHCO C 4 H 5 N CH 3 |
|
ND |
|
slabý základ |
|
|
- | ? |
| Prolin | P | Pro | -CH 2 CH 2 CH 2 - |
|
- |
|
- |
|
|
- | 90 |
| Glutamin | Otázka | Gln | -CH 2 CH 2 CONH 2 |
|
- |
|
- |
|
|
- | 114 |
| Arginin | R. | Arg | -(CH 2 ) 3 NH-C (NH) NH 2 |
|
12.3 |
|
silně základní |
|
|
- | 148 |
| Serine | S | Ser | -CH 2 OH |
|
- |
|
- |
|
|
- | 73 |
| Threonin | T | Thr | -CH (OH) CH 3 |
|
- |
|
- |
|
|
- | 93 |
| Selenocystein | U | Sek | -CH 2 SeH |
|
5.43 |
|
kyselý |
|
|
- | ? |
| Valine | PROTI | Val | -CH (CH 3 ) 2 |
|
- |
|
- |
|
|
Alifatický | 105 |
| Tryptofan | W | Trp | -CH 2 C 8 H 6 N |
|
- |
|
- |
|
|
Aromatický | 163 |
| Tyrosin | Y | Tyr | -CH 2 -C 6 H 4 OH |
|
9,84 |
|
slabě kyselý |
|
|
Aromatický | 141 |
§: Hodnoty pro Asp, Cys, Glu, His, Lys a Tyr byly stanoveny pomocí zbytku aminokyseliny umístěného centrálně v alanin pentapeptidu. Hodnota pro Arg je od Pace a kol. (2009). Hodnota pro Sec pochází z Byun & Kang (2011).
ND: Hodnota pKa pyrrolysinu nebyla hlášena.
Poznámka: Hodnota pKa aminokyselinového zbytku v malém peptidu je typicky mírně odlišná, pokud je uvnitř proteinu. Výpočty proteinů pKa se někdy používají k výpočtu změny hodnoty pKa zbytku aminokyseliny v této situaci.
Genová exprese a biochemie
| Aminokyselina | Krátký | Zkratka. | Codon (y) | Výskyt | Nezbytné ‡ u lidí | |||
|---|---|---|---|---|---|---|---|---|
| v archaských bílkovinách (%) & |
v bakteriálních bílkovinách (%) & |
v eukaryotických bílkovinách (%) & |
Výskyt v lidských bílkovinách (%) & |
|||||
| Alanine | A | Ala | GCU, GCC, GCA, GCG | 8.2 | 10.06 | 7,63 | 7.01 | Ne |
| Cystein | C | Cys | UGU, UGC | 0,98 | 0,94 | 1,76 | 2.3 | Podmíněně |
| Kyselina asparagová | D | Asp | GAU, GAC | 6.21 | 5,59 | 5.4 | 4,73 | Ne |
| Kyselina glutamová | E | Glu | GAA, GAG | 7,69 | 6.15 | 6,42 | 7.09 | Podmíněně |
| Fenylalanin | F | Phe | UUU, UUC | 3,86 | 3,89 | 3,87 | 3,65 | Ano |
| Glycin | G | Gly | GGU, GGC, GGA, GGG | 7,58 | 7,76 | 6,33 | 6,58 | Podmíněně |
| Histidin | H | Jeho | CAU, CAC | 1,77 | 2,06 | 2,44 | 2,63 | Ano |
| Isoleucin | Já | Ile | AUU, AUC, AUA | 7.03 | 5,89 | 5.1 | 4.33 | Ano |
| Lysin | K | Lys | AAA, AAG | 5.27 | 4,68 | 5,64 | 5,72 | Ano |
| Leucin | L | Leu | UUA, UUG, CUU, CUC, CUA, CUG | 9,31 | 10.09 | 9.29 | 9,97 | Ano |
| Methionin | M | Se setkal | SRPEN | 2.35 | 2.38 | 2.25 | 2.13 | Ano |
| Asparagin | N. | Asn | AAU, AAC | 3,68 | 3,58 | 4.28 | 3,58 | Ne |
| Pyrrolysin | Ó | Pyl | UAG * | 0 | 0 | 0 | 0 | Ne |
| Prolin | P | Pro | CCU, CCC, CCA, CCG | 4.26 | 4,61 | 5,41 | 6.31 | Ne |
| Glutamin | Otázka | Gln | CAA, CAG | 2.38 | 3,58 | 4.21 | 4,77 | Ne |
| Arginin | R. | Arg | CGU, CGC, CGA, CGG, AGA, AGG | 5,51 | 5,88 | 5,71 | 5,64 | Podmíněně |
| Serine | S | Ser | UCU, UCC, UCA, UCG, AGU, AGC | 6.17 | 5,85 | 8,34 | 8,33 | Ne |
| Threonin | T | Thr | ACU, ACC, ACA, ACG | 5,44 | 5,52 | 5,56 | 5,36 | Ano |
| Selenocystein | U | Sek | UGA ** | 0 | 0 | 0 | > 0 | Ne |
| Valine | PROTI | Val | GUU, GUC, GUA, GUG | 7.8 | 7.27 | 6.2 | 5,96 | Ano |
| Tryptofan | W | Trp | UGG | 1,03 | 1,27 | 1.24 | 1.22 | Ano |
| Tyrosin | Y | Tyr | UAU, UAC | 3,35 | 2,94 | 2,87 | 2,66 | Podmíněně |
| Zastavit kodon † | - | Období | UAA, UAG, UGA †⇨ | ? | ? | ? | N/A | N/A |
* UAG je normálně jantarový stop kodon , ale v organismech obsahujících biologický aparát kódovaný shlukem genů pylTSBCD bude začleněna aminokyselina pyrrolysin.
** UGA je normálně opálový (nebo umber) stop kodon, ale kóduje selenocystein, pokud je přítomen prvek SECIS .
† stop kodon není aminokyselina, ale je zahrnut pro úplnost.
†Atics UAG a UGA nepůsobí vždy jako stop kodony (viz výše).
‡ Esenciální aminokyselinu nelze syntetizovat u lidí, a proto musí být dodávána ve stravě. Podmíněně esenciální aminokyseliny nejsou ve stravě běžně vyžadovány, ale musí být dodávány exogenně specifickým populacím, které je nesyntetizují v odpovídajícím množství.
& Výskyt aminokyselin je založen na 135 Archaea, 3775 Bacteria, 614 Eukaryota proteomech a lidském proteomu (21 006 proteinů).
Hmotnostní spektrometrie
Při hmotnostní spektrometrii peptidů a proteinů je užitečná znalost hmot zbytků. Hmotnost peptidu nebo proteinu je součtem hmot zbytků plus hmotnosti vody ( monoizotopická hmotnost = 18,01056 Da; průměrná hmotnost = 18,0153 Da). Hmotnosti zbytků se vypočítají z tabulkových chemických vzorců a atomových hmotností. V hmotnostní spektrometrii mohou ionty také zahrnovat jeden nebo více protonů ( monoizotopická hmotnost = 1,00728 Da; průměrná hmotnost* = 1,0074 Da). *Protony nemohou mít průměrnou hmotnost, což je matoucím způsobem odvozeno od Deuteronů jako platného izotopu, ale měly by být jiného druhu (viz Hydron (chemie) )
| Aminokyselina | Krátký | Zkratka. | Vzorec | Po. hmotnost § ( Da ) | Prům. hmotnost ( Da ) |
|---|---|---|---|---|---|
| Alanine | A | Ala | C 3 H 5 Č | 71,03711 | 71,0779 |
| Cystein | C | Cys | C 3 H 5 NOS | 103,00919 | 103,1429 |
| Kyselina asparagová | D | Asp | C 4 H 5 NO 3 | 115,02694 | 115,0874 |
| Kyselina glutamová | E | Glu | C 5 H 7 NO 3 | 129,04259 | 129,1140 |
| Fenylalanin | F | Phe | C 9 H 9 Č | 147,06841 | 147,1739 |
| Glycin | G | Gly | C 2 H 3 Č | 57,02146 | 57,0513 |
| Histidin | H | Jeho | C 6 H 7 N 3 O | 137,05891 | 137,1393 |
| Isoleucin | Já | Ile | C 6 H 11 Č | 113,08406 | 113,1576 |
| Lysin | K | Lys | C 6 H 12 N 2 O | 128,09496 | 128,1723 |
| Leucin | L | Leu | C 6 H 11 Č | 113,08406 | 113,1576 |
| Methionin | M | Se setkal | C 5 H 9 NOS | 131,04049 | 131,1961 |
| Asparagin | N. | Asn | C 4 H 6 N 2 O 2 | 114,04293 | 114,1026 |
| Pyrrolysin | Ó | Pyl | C 12 H 19 N 3 O 2 | 237,14773 | 237,2982 |
| Prolin | P | Pro | C 5 H 7 Č | 97,05276 | 97,1152 |
| Glutamin | Otázka | Gln | C 5 H 8 N 2 O 2 | 128,05858 | 128,1292 |
| Arginin | R. | Arg | C 6 H 12 N 4 O | 156,10111 | 156,1857 |
| Serine | S | Ser | C 3 H 5 NO 2 | 87,03203 | 87,0773 |
| Threonin | T | Thr | C 4 H 7 NO 2 | 101,04768 | 101,1039 |
| Selenocystein | U | Sek | C 3 H 5 NOS | 150,95364 | 150,0489 |
| Valine | PROTI | Val | C 5 H 9 Č | 99,06841 | 99,1311 |
| Tryptofan | W | Trp | C 11 H 10 N 2 O | 186,07931 | 186,2099 |
| Tyrosin | Y | Tyr | C 9 H 9 NO 2 | 163,06333 | 163,1733 |
Stechiometrie a metabolické náklady v buňce
Níže uvedená tabulka uvádí množství aminokyselin v buňkách E.coli a metabolické náklady (ATP) na syntézu aminokyselin. Záporná čísla naznačují, že metabolické procesy jsou energeticky příznivé a nestojí čistý ATP buňky. Množství aminokyselin zahrnuje aminokyseliny ve volné formě a v polymerační formě (proteiny).
| Aminokyselina | Krátký | Zkratka. | Hojnost (počet molekul (× 108 ) na buňku E. coli ) |
Náklady na syntézu ATP | |
|---|---|---|---|---|---|
| Aerobní podmínky |
Anaerobní podmínky |
||||
| Alanine | A | Ala | 2.9 | -1 | 1 |
| Cystein | C | Cys | 0,52 | 11 | 15 |
| Kyselina asparagová | D | Asp | 1.4 | 0 | 2 |
| Kyselina glutamová | E | Glu | 1.5 | -7 | -1 |
| Fenylalanin | F | Phe | 1.1 | -6 | 2 |
| Glycin | G | Gly | 3.5 | -2 | 2 |
| Histidin | H | Jeho | 0,54 | 1 | 7 |
| Isoleucin | Já | Ile | 1.7 | 7 | 11 |
| Lysin | K | Lys | 2.0 | 5 | 9 |
| Leucin | L | Leu | 2.6 | -9 | 1 |
| Methionin | M | Se setkal | 0,88 | 21 | 23 |
| Asparagin | N. | Asn | 1.4 | 3 | 5 |
| Pyrrolysin | Ó | Pyl | - | - | - |
| Prolin | P | Pro | 1.3 | -2 | 4 |
| Glutamin | Otázka | Gln | 1.5 | -6 | 0 |
| Arginin | R. | Arg | 1.7 | 5 | 13 |
| Serine | S | Ser | 1.2 | -2 | 2 |
| Threonin | T | Thr | 1.5 | 6 | 8 |
| Selenocystein | U | Sek | - | - | - |
| Valine | PROTI | Val | 2.4 | -2 | 2 |
| Tryptofan | W | Trp | 0,33 | -7 | 7 |
| Tyrosin | Y | Tyr | 0,79 | -8 | 2 |
Poznámky
| Aminokyselina | Zkratka. | Poznámky | |
|---|---|---|---|
| Alanine | A | Ala | Velmi hojný a velmi univerzální, je tužší než glycin, ale dostatečně malý, aby představoval pouze malé sterické limity pro konformaci proteinu. Chová se poměrně neutrálně a může být umístěn jak v hydrofilních oblastech na vnějším proteinu, tak v hydrofobních oblastech uvnitř. |
| Asparagin nebo kyselina asparagová | B | Asx | Zástupný symbol, když některá aminokyselina může zaujímat pozici |
| Cystein | C | Cys | Atom síry se snadno váže na ionty těžkých kovů . Za oxidačních podmínek se dva cysteiny mohou spojit dohromady v disulfidové vazbě za vzniku aminokyseliny cystinu . Pokud jsou cystiny součástí proteinu, například inzulínu , je terciární struktura stabilizována, což činí protein odolnějším vůči denaturaci ; proto jsou disulfidové vazby běžné u proteinů, které musí fungovat v drsném prostředí, včetně trávicích enzymů (např. pepsin a chymotrypsin ) a strukturálních proteinů (např. keratin ). Disulfidy se také nacházejí v peptidech příliš malých na to, aby samy udržely stabilní tvar (např. Inzulín ). |
| Kyselina asparagová | D | Asp | Asp se chová podobně jako kyselina glutamová a nese hydrofilní kyselou skupinu se silným negativním nábojem. Obvykle se nachází na vnějším povrchu proteinu, takže je rozpustný ve vodě. Váže se na kladně nabité molekuly a ionty a často se používá v enzymech k fixaci kovových iontů. Když jsou umístěny v proteinu, aspartát a glutamát jsou obvykle spárovány s argininem a lysinem. |
| Kyselina glutamová | E | Glu | Glu se chová podobně jako kyselina asparagová a má delší, o něco pružnější postranní řetězec. |
| Fenylalanin | F | Phe | Fenylalanin, tyrosin a tryptofan, esenciální pro člověka, obsahují na postranním řetězci velkou tuhou aromatickou skupinu. To jsou největší aminokyseliny. Stejně jako isoleucin, leucin a valin jsou tyto hydrofobní a mají tendenci se orientovat směrem dovnitř složené molekuly proteinu. Fenylalanin lze převést na tyrosin. |
| Glycin | G | Gly | Vzhledem ke dvěma atomům vodíku na α uhlíku není glycin opticky aktivní . Je to nejmenší aminokyselina, snadno se otáčí a dodává proteinovému řetězci flexibilitu. Je schopen se vejít do nejužších prostor, např. Do trojité šroubovice kolagenu . Protože přílišná flexibilita obvykle není žádoucí, je jako strukturní složka méně častá než alanin. |
| Histidin | H | Jeho | Jeho je pro člověka zásadní. V i mírně kyselých podmínkách dochází k protonaci dusíku, čímž se mění vlastnosti histidinu a polypeptidu jako celku. Mnoho proteinů jej používá jako regulační mechanismus, který mění konformaci a chování polypeptidu v kyselých oblastech, jako je pozdní endosom nebo lysozom , což vynucuje změnu konformace v enzymech. K tomu je však zapotřebí pouze několik histidinů, takže je poměrně vzácný. |
| Isoleucin | Já | Ile | Ile je pro člověka nezbytný. Izoleucin, leucin a valin mají velké alifatické hydrofobní postranní řetězce. Jejich molekuly jsou tuhé a jejich vzájemné hydrofobní interakce jsou důležité pro správné skládání proteinů, protože tyto řetězce se obvykle nacházejí uvnitř molekuly proteinu. |
| Leucin nebo isoleucin | J. | Xle | Zástupný symbol, když některá aminokyselina může zaujímat pozici |
| Lysin | K | Lys | Lys je pro člověka nezbytný a chová se podobně jako arginin. Obsahuje dlouhý, pružný postranní řetěz s kladně nabitým koncem. Flexibilita řetězce činí lysin a arginin vhodné pro vazbu na molekuly s mnoha negativními náboji na jejich povrchu. Například proteiny vážící DNA mají aktivní oblasti bohaté na arginin a lysin. Silný náboj činí tyto dvě aminokyseliny náchylné k umístění na vnějších hydrofilních površích proteinů; když jsou nalezeny uvnitř, jsou obvykle spárovány s odpovídající záporně nabitou aminokyselinou, např. aspartátem nebo glutamátem. |
| Leucin | L | Leu | Leu je pro člověka nezbytný a chová se podobně jako izoleucin a valin. |
| Methionin | M | Se setkal | Met je pro člověka nezbytný. Vždy první aminokyselina, která má být začleněna do proteinu, je někdy odstraněna po translaci. Stejně jako cystein obsahuje síru, ale s methylovou skupinou místo vodíku. Tato methylová skupina může být aktivována a používá se v mnoha reakcích, kde se do jiné molekuly přidává nový atom uhlíku. |
| Asparagin | N. | Asn | Podobně jako kyselina asparagová obsahuje Asn amidovou skupinu, kde Asp má karboxyl . |
| Pyrrolysin | Ó | Pyl | Podobný lysinu , ale má připojený pyrrolinový kruh. |
| Prolin | P | Pro | Pro obsahuje neobvyklý kruh pro N-koncovou aminoskupinu, který nutí sekvenci CO-NH amidu do pevné konformace. Může narušit struktury skládání proteinů, jako je alfa šroubovice nebo β list , což způsobí požadovaný zlom v proteinovém řetězci. Běžné v kolagenu , často prochází posttranslační modifikací na hydroxyprolin . |
| Glutamin | Otázka | Gln | Podobně jako kyselina glutamová obsahuje Gln amidovou skupinu, kde Glu má karboxyl . Používá se v bílkovinách a jako úložiště amoniaku je to nejhojnější aminokyselina v těle. |
| Arginin | R. | Arg | Funkčně podobný lysinu. |
| Serine | S | Ser | Serin a threonin mají krátkou skupinu zakončenou hydroxylovou skupinou. Jeho vodík je snadno odstranitelný, takže serin a threonin často působí jako donory vodíku v enzymech. Oba jsou velmi hydrofilní, takže vnější oblasti rozpustných proteinů s nimi bývají bohaté. |
| Threonin | T | Thr | Thr, který je pro člověka nezbytný, se chová podobně jako serin. |
| Selenocystein | U | Sek | Selenu analog cysteinu, ve které selen nahradí síry atom. |
| Valine | PROTI | Val | Val je pro člověka nezbytný, chová se podobně jako izoleucin a leucin. |
| Tryptofan | W | Trp | Trp, nezbytný pro člověka, se chová podobně jako fenylalanin a tyrosin. Je prekurzorem serotoninu a je přirozeně fluorescenční . |
| Neznámý | X | Xaa | Zástupný symbol, pokud je aminokyselina neznámá nebo nedůležitá. |
| Tyrosin | Y | Tyr | Tyr se chová podobně jako fenylalanin (předchůdce tyrosinu) a tryptofan a je prekurzorem melaninu , epinefrinu a hormonů štítné žlázy . Přirozeně fluorescenční , jeho fluorescence je obvykle potlačena přenosem energie na tryptofany. |
| Kyselina glutamová nebo glutamin | Z | Glx | Zástupný symbol, když některá aminokyselina může zaujímat pozici |
Katabolismus
Aminokyseliny lze klasifikovat podle vlastností jejich hlavních produktů:
- Glukogenní, přičemž výrobky, které mají schopnost tvořit glukózy prostřednictvím glukoneogeneze
- Ketogenní, s produkty, které nemají schopnost vytvářet glukózu: Tyto produkty mohou být stále použity pro ketogenezi nebo syntézu lipidů .
- Aminokyseliny katabolizované na glukogenní i ketogenní produkty
Viz také
Reference
Obecné reference
- Nelson, David L .; Cox, Michael M. (2000). Lehningerovy principy biochemie (3. vyd.). Worth Publishers. ISBN 978-1-57259-153-0.
- Kyte J, Doolittle RF (květen 1982). „Jednoduchá metoda pro zobrazení hydropatického charakteru proteinu“. Journal of Molecular Biology . 157 (1): 105–32. CiteSeerX 10.1.1.458.454 . doi : 10,1016/0022-2836 (82) 90515-0 . PMID 7108955 .
- Meierhenrich, Uwe J. (2008). Aminokyseliny a asymetrie života (1. vyd.). Springer. ISBN 978-3-540-76885-2.
- Biochemie, Harpers (2015). Harpers Illustrated Biochemistry (30. ed.). Lange. ISBN 978-0-07-182534-4.
























