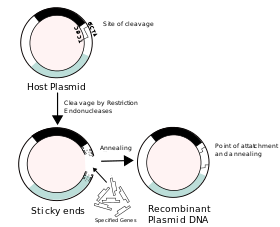
Rekombinantní DNA - Recombinant DNA
| Část série na |
| Genetické inženýrství |
|---|
 |
| Geneticky modifikované organismy |
| Historie a regulace |
| Proces |
| Aplikace |
| Kontroverze |
Molekuly rekombinantní DNA ( rDNA ) jsou molekuly DNA vytvořené laboratorními metodami genetické rekombinace (jako je molekulární klonování ), které spojují genetický materiál z více zdrojů a vytvářejí sekvence, které by se jinak v genomu nenašly .
Rekombinantní DNA je obecný název pro část DNA, která byla vytvořena kombinací alespoň dvou fragmentů ze dvou různých zdrojů. Rekombinantní DNA je možná, protože molekuly DNA ze všech organismů mají stejnou chemickou strukturu a liší se pouze v nukleotidové sekvenci v rámci stejné celkové struktury. Rekombinantní molekuly DNA se někdy nazývají chimérické DNA , protože mohou být vyrobeny z materiálu dvou různých druhů, jako je mytická chiméra . Technologie R-DNA využívá palindromické sekvence a vede k produkci lepkavých a tupých konců .
Sekvence DNA použité při konstrukci molekul rekombinantní DNA mohou pocházet z jakéhokoli druhu . Rostlinná DNA může být například spojena s bakteriální DNA nebo lidská DNA může být spojena s houbovou DNA. Navíc sekvence DNA, které se nevyskytují nikde v přírodě, mohou být vytvořeny chemickou syntézou DNA a začleněny do rekombinantních molekul. Pomocí technologie rekombinantní DNA a syntetické DNA může být vytvořena a zavedena doslova jakákoli sekvence DNA do kteréhokoli z velmi širokého spektra živých organismů.
Proteiny, které mohou být výsledkem exprese rekombinantní DNA v živých buňkách, se nazývají rekombinantní proteiny . Když je rekombinantní DNA kódující protein zaveden do hostitelského organismu, rekombinantní protein není nutně produkován. Exprese cizích proteinů vyžaduje použití specializovaných expresních vektorů a často vyžaduje významnou restrukturalizaci cizími kódujícími sekvencemi.
Rekombinantní DNA se liší od genetické rekombinace v tom, že první je výsledkem umělých metod ve zkumavce, zatímco druhá je normální biologický proces, který vede k remixování existujících sekvencí DNA v podstatě ve všech organismech.
Vytvoření DNA
Molekulární klonování je laboratorní proces používaný k vytvoření rekombinantní DNA. Je to jedna ze dvou nejpoužívanějších metod spolu s polymerázovou řetězovou reakcí (PCR), která se používá k řízení replikace jakékoli konkrétní sekvence DNA zvolené experimentátorem. Mezi metodami existují dva zásadní rozdíly. Jedním z nich je, že molekulární klonování zahrnuje replikaci DNA v živé buňce, zatímco PCR replikuje DNA ve zkumavce bez živých buněk. Dalším rozdílem je, že klonování zahrnuje řezání a vkládání sekvencí DNA, zatímco PCR se zesiluje kopírováním existující sekvence.
Tvorba rekombinantní DNA vyžaduje klonovací vektor , molekulu DNA, která se replikuje v živé buňce. Vektory jsou obecně odvozeny z plazmidů nebo virů a představují relativně malé segmenty DNA, které obsahují nezbytné genetické signály pro replikaci, a také další prvky pro usnadnění vkládání cizí DNA, identifikace buněk, které obsahují rekombinantní DNA, a kde je to vhodné, exprese cizí DNA. Volba vektoru pro molekulární klonování závisí na volbě hostitelského organismu, velikosti klonované DNA a na tom, zda a jak má být cizí DNA exprimována. Segmenty DNA lze kombinovat za použití řady metod, jako je klonování restrikčním enzymem/ligázou nebo Gibsonova sestava .
Ve standardních klonovacích protokolech klonování jakéhokoli fragmentu DNA v zásadě zahrnuje sedm kroků: (1) volba hostitelského organismu a klonovacího vektoru, (2) příprava vektorové DNA, (3) příprava DNA na klonování, (4) vytvoření rekombinantní DNA, (5) Zavedení rekombinantní DNA do hostitelského organismu, (6) Výběr organismů obsahujících rekombinantní DNA a (7) Screening klonů s požadovanými DNA vložkami a biologickými vlastnostmi. Tyto kroky jsou podrobně popsány v souvisejícím článku ( molekulární klonování ).
Exprese DNA
Po transplantaci do hostitelského organismu může, ale nemusí být exprimována cizí DNA obsažená v konstruktu rekombinantní DNA . To znamená, že DNA může být jednoduše replikována bez exprese, nebo může být transkribována a translována a je produkován rekombinantní protein. Obecně řečeno, exprese cizího genu vyžaduje restrukturalizaci genu tak, aby zahrnovala sekvence, které jsou nutné pro produkci molekuly mRNA , která může být použita translačním aparátem hostitele (např. Promotor , translační iniciační signál a terminátor transkripce ). Pro zlepšení exprese mimoděložního genu mohou být provedeny specifické změny v hostitelském organismu. Kromě toho mohou být nutné také změny v kódujících sekvencích, aby se optimalizovala translace, učinil protein rozpustným, nasměroval rekombinantní protein do správného buněčného nebo extracelulárního umístění a stabilizoval protein před degradací.
Vlastnosti organismů obsahujících rekombinantní DNA
Organismy obsahující rekombinantní DNA mají ve většině případů zjevně normální fenotypy . To znamená, že jejich vzhled, chování a metabolismus jsou obvykle nezměněny a jediný způsob, jak prokázat přítomnost rekombinantních sekvencí, je zkoumat samotnou DNA, obvykle pomocí testu polymerázové řetězové reakce (PCR). Významné výjimky existují a jsou diskutovány níže.
Pokud sekvence rDNA kódují gen, který je exprimován, pak lze detekovat přítomnost RNA a/nebo proteinových produktů rekombinantního genu, typicky pomocí RT-PCR nebo metod západní hybridizace . Hrubé fenotypové změny nejsou normou, pokud rekombinantní gen nebyl vybrán a upraven tak, aby generoval biologickou aktivitu v hostitelském organismu. Další fenotypy, se kterými se setkáváme, zahrnují toxicitu pro hostitelský organismus indukovanou produktem rekombinantního genu, zvláště pokud je nadměrně exprimován nebo exprimován v nevhodných buňkách nebo tkáních.
V některých případech může mít rekombinantní DNA škodlivé účinky, i když není exprimována. Jedním mechanismem, kterým se to děje, je inzerční inaktivace , při které se rDNA vloží do genu hostitelské buňky. V některých případech vědci používají tento jev k „ vyřazení “ genů, aby určili jejich biologickou funkci a důležitost. Dalším mechanismem, kterým může inzerce rDNA do chromozomální DNA ovlivnit genovou expresi, je nevhodná aktivace dříve neexprimovaných genů hostitelské buňky. To se může stát například tehdy, když se fragment rekombinantní DNA obsahující aktivní promotor umístí vedle dříve tichého genu hostitelské buňky, nebo když gen hostitelské buňky, který funguje tak, že omezuje genovou expresi, podstoupí inzerční inaktivaci rekombinantní DNA.
Aplikace DNA
Rekombinantní DNA je široce používána v biotechnologiích , medicíně a výzkumu . Rekombinantní proteiny a další produkty, které jsou výsledkem použití technologie DNA, se dnes nacházejí v podstatě v každé západní lékárně, ordinaci lékaře nebo veterináře, lékařské testovací laboratoři a laboratoři biologického výzkumu. Kromě toho se organismy, které byly manipulovány pomocí technologie rekombinantní DNA, stejně jako produkty z nich odvozené, dostaly do mnoha farem, supermarketů , domácích lékárniček a dokonce i do zverimexu, jako jsou ty, které prodávají GloFish a další geneticky upravená zvířata .
Nejběžnější aplikace rekombinantní DNA je v základním výzkumu, ve kterém je technologie důležitá pro většinu současné práce v biologických a biomedicínských vědách. Rekombinantní DNA se používá k identifikaci, mapování a sekvenování genů a ke stanovení jejich funkce. Sondy rDNA se používají k analýze genové exprese v jednotlivých buňkách a v tkáních celých organismů. Rekombinantní proteiny jsou široce používány jako činidla v laboratorních experimentech a ke generování protilátkových sond pro zkoumání syntézy proteinů v buňkách a organismech.
Mnoho dalších praktických aplikací rekombinantní DNA se nachází v průmyslu, výrobě potravin, humánní a veterinární medicíně, zemědělství a bioinženýrství. Některé konkrétní příklady jsou uvedeny níže.
- Rekombinantní chymozin
- Nalezeno v syřidla , chymosinu je enzym, nutných pro výrobu sýra. Byla to první geneticky upravená potravinářská přídatná látka používaná komerčně. Procesory tradičně získávali chymosin ze syřidla, což je přípravek získaný ze čtvrtého žaludku telat krmených mlékem. Vědci vyvinuli nepatogenní kmen (K-12) bakterií E. coli pro rozsáhlou laboratorní produkci enzymu. Tento mikrobiologicky produkovaný rekombinantní enzym, strukturně identický s enzymem získaným z tele, stojí méně a je produkován v hojném množství. Dnes je asi 60% tvrdých sýrů v USA vyrobeno z geneticky upraveného chymozinu. V roce 1990 FDA udělil chymozinu status „ obecně uznávaný jako bezpečný “ (GRAS) na základě údajů prokazujících, že enzym je bezpečný.
- Rekombinantní lidský inzulín
- Téměř úplně nahradil inzulín získávaný ze zvířecích zdrojů (např. Prasat a skotu) pro léčbu diabetu závislého na inzulínu . Široce se používá řada různých rekombinantních inzulínových přípravků. Rekombinantní inzulín se syntetizuje vložením genu pro lidský inzulín do E. coli nebo kvasinek (Saccharomyces cerevisiae), které poté produkují inzulín pro humánní použití.
- Rekombinantní lidský růstový hormon (HGH, somatotropin)
- Podává se pacientům, jejichž hypofýza generuje nedostatečné množství na podporu normálního růstu a vývoje. Předtím, než byl k dispozici rekombinantní HGH, byl HGH pro terapeutické použití získán z hypofýzy mrtvol. Tato nebezpečná praxe vedla u některých pacientů k rozvoji Creutzfeldt – Jakobovy choroby . Rekombinantní HGH tento problém odstranil a nyní se používá terapeuticky. Byl také zneužíván jako droga zvyšující výkonnost sportovci a dalšími. Vstup do DrugBank
- Rekombinantní faktor srážení krve VIII
- Protein srážející krev, který je podáván pacientům s formami hemofilie s poruchou krvácení, kteří nejsou schopni produkovat faktor VIII v množství dostatečném pro podporu normální koagulace krve. Před vývojem rekombinantního faktoru VIII byl protein získán zpracováním velkého množství lidské krve od více dárců, což s sebou neslo velmi vysoké riziko přenosu infekčních nemocí přenášených krví , například HIV a hepatitidy B. Vstup na DrugBank
- Rekombinantní vakcína proti hepatitidě B.
- Infekce hepatitidy B je kontrolována použitím rekombinantní vakcíny proti hepatitidě B, která obsahuje formu povrchového antigenu viru hepatitidy B, který je produkován v kvasinkových buňkách. Vývoj rekombinantní podjednotkové vakcíny byl důležitý a nezbytný vývoj, protože virus hepatitidy B, na rozdíl od jiných běžných virů, jako je virus obrny , nelze pěstovat in vitro . Informace o očkování od Nadace proti hepatitidě B.
- Diagnostika infekce HIV
- Každá ze tří široce používaných metod diagnostiky infekce HIV byla vyvinuta pomocí rekombinantní DNA. Test protilátek ( ELISA nebo Western blot ) používá rekombinantní protein HIV k testování přítomnosti protilátek, které si tělo vytvořilo v reakci na infekci HIV. Test DNA zjišťuje přítomnost genetického materiálu HIV pomocí polymerázové řetězové reakce s reverzní transkripcí (RT-PCR). Vývoj testu RT-PCR byl umožněn molekulárním klonováním a sekvenční analýzou genomů HIV. Stránka testování HIV z amerických center pro kontrolu nemocí (CDC)
- Zlatá rýže
- Rekombinantní odrůda rýže, která byla zkonstruována tak, aby exprimovala enzymy zodpovědné za biosyntézu beta-karotenu . Tato odrůda rýže je významným příslibem snížení výskytu nedostatku vitaminu A ve světové populaci. Zlatá rýže se momentálně nepoužívá, čeká se na vyřešení problémů s regulací a duševním vlastnictvím.
- Plodiny odolné vůči herbicidům
- Byly vyvinuty komerční odrůdy důležitých zemědělských plodin (včetně sóji, kukuřice/kukuřice, čiroku, řepky, vojtěšky a bavlny), které obsahují rekombinantní gen, který vede k rezistenci vůči herbicidu glyfosátu (obchodní název Roundup ) a zjednodušují kontrolu plevele glyfosátem aplikace. Tyto plodiny jsou běžně komerčně využívány v několika zemích.
- Plodiny odolné proti hmyzu
- Bacillus thuringeiensis je bakterie, která přirozeně produkuje protein ( Bt toxin ) s insekticidními vlastnostmi. Bakterie byla aplikována na plodiny jako strategie hubení hmyzu po mnoho let a tato praxe byla široce přijata v zemědělství a zahradnictví. Nedávno byly vyvinuty rostliny, které exprimují rekombinantní formu bakteriálního proteinu, který může účinně kontrolovat některé hmyzí predátory. Environmentální problémy spojené s používáním těchto transgenních plodin nebyly zcela vyřešeny.
Dějiny
Myšlenku rekombinantní DNA poprvé navrhl Peter Lobban, postgraduální student prof. Dale Kaisera z katedry biochemie na Stanfordské univerzitní lékařské škole. První publikace popisující úspěšnou produkci a intracelulární replikaci rekombinantní DNA se objevily v letech 1972 a 1973 od Stanfordu a UCSF . V roce 1980 získal Paul Berg , profesor katedry biochemie na Stanfordu a autor jednoho z prvních článků, Nobelovu cenu za chemii za práci na nukleových kyselinách „se zvláštním ohledem na rekombinantní DNA“. Werner Arber , Hamilton Smith a Daniel Nathans sdíleli Nobelovu cenu za fyziologii nebo medicínu z roku 1978 za objev restrikčních endonukleáz, které zdokonalily techniku technologie rDNA.
Stanfordská univerzita požádala v roce 1974 o americký patent na rekombinantní DNA a uvedla vynálezce jako Herbert W. Boyer (profesor na Kalifornské univerzitě v San Francisku ) a Stanley N. Cohen (profesor na Stanfordské univerzitě ); tento patent byl udělen v roce 1980. První licencovaný lék generovaný pomocí technologie rekombinantní DNA byl lidský inzulín, vyvinutý společností Genentech a licencovaný společností Eli Lilly and Company .
Kontroverze
Vědci související s počátečním vývojem metod rekombinantní DNA uznali, že existuje potenciál, že organismy obsahující rekombinantní DNA mají nežádoucí nebo nebezpečné vlastnosti. Na konferenci Asilomar o rekombinantní DNA v roce 1975 byly tyto obavy projednány a bylo zahájeno dobrovolné moratorium na výzkum rekombinantní DNA pro experimenty, které byly považovány za obzvláště rizikové. Toto moratorium bylo široce pozorováno, dokud národní instituty zdraví (USA) nevyvinuly a nevydaly formální pokyny pro práci rDNA. Rekombinantní molekuly DNA a rekombinantní proteiny dnes obvykle nejsou považovány za nebezpečné. Stále však existují obavy ohledně některých organismů, které exprimují rekombinantní DNA, zvláště když opouštějí laboratoř a jsou zaváděny do životního prostředí nebo do potravinového řetězce. Tyto obavy jsou diskutovány v článcích o geneticky modifikovaných organismech a kontroverzích geneticky modifikovaných potravin . Kromě toho existují obavy z vedlejších produktů v biofarmaceutické výrobě, kde rekombinantní DNA vede ke specifickým proteinovým produktům. Hlavní vedlejší produkt, nazývaný protein hostitelské buňky , pochází z expresního systému hostitele a představuje hrozbu pro zdraví pacienta a celkové životní prostředí.
Viz také
- Asilomarská konference o rekombinantní DNA
- Genetické inženýrství
- Geneticky upravený organismus
- Rekombinantní virus
- Vektorové DNA
- Biomolekulární inženýrství
- Technologie rekombinantní DNA
- Protein hostitelské buňky
- Expresní systém T7
Reference
Další čtení
- Osmý den stvoření: Tvůrci revoluce v biologii . Touchstone Books, ISBN 0-671-22540-5 . 2. vydání: Cold Spring Harbor Laboratory Press, 1996 brožováno: ISBN 0-87969-478-5 .
- Micklasi, Davide. 2003. DNA Science: První kurz . Cold Spring Harbor Press: ISBN 978-0-87969-636-8 .
- Rasmussen, Nicolas , Gene Jockeys: Life Science and the rise of Biotech Enterprise , Johns Hopkins University Press, (Baltimore), 2014 . ISBN 978-1-42141-340-2 .
- Rosenfeld, Izrael. 2010. DNA: Grafický průvodce po molekule, která otřásla světem . Columbia University Press: ISBN 978-0-231-14271-7 .
- Schultz, Mark a Zander Cannon. 2009. Věc života: grafický průvodce genetikou a DNA . Hill and Wang: ISBN 0-8090-8947-5 .
- Watson, Jamesi. 2004. DNA: Tajemství života . Random House: ISBN 978-0-09-945184-6 .
externí odkazy
|
Knihovní zdroje o rekombinantních proteinech |
- Informační list o rekombinantní DNA (z University of New Hampshire)
- Plazmidy v kvasnicích (přehled ze Státní univerzity v San Diegu)
- Animace ilustrující konstrukci rekombinantní DNA a produkce cizích proteinů rekombinantními bakteriemi
- Výzkum rekombinantní DNA na UCSF a komerční aplikace v Genentech Upravený přepis rozhovoru z roku 1994 s Herbertem W. Boyerem, projekt Living history. Orální historie.
- Příručka zásad a metod čištění rekombinantních proteinů
- Massachusetts Institute of Technology, Oral History Program, Oral History Collection on the Recombinant DNA Controversy , MC-0100. Massachusetts Institute of Technology, Department of Distinctive Collections, Cambridge, Massachusetts