Relativistická kvantová chemie - Relativistic quantum chemistry
Relativistická kvantová chemie kombinuje relativistickou mechaniku s kvantovou chemií pro výpočet elementárních vlastností a struktury, zejména u těžších prvků periodické tabulky . Významným příkladem je vysvětlení barvy zlata : kvůli relativistickým efektům není stříbřitý jako většina ostatních kovů.
Termín relativistické efekty byl vyvinut ve světle historie kvantové mechaniky. Zpočátku byla vyvinuta kvantová mechanika bez ohledu na teorii relativity . Relativistické efekty jsou ty nesrovnalosti mezi hodnotami vypočítanými modely, které berou v úvahu relativitu, a těmi, které ji neberou. Relativistické efekty jsou důležité pro těžší prvky s vysokým atomovým číslem . V nejběžnějším rozložení periodické tabulky jsou tyto prvky zobrazeny ve spodní oblasti. Příklady jsou lanthanoidy a aktinidy .
Za relativistické efekty v chemii lze považovat perturbace nebo malé korekce nerelativistické teorie chemie, která je vyvinuta z řešení Schrödingerovy rovnice . Tyto korekce ovlivňují elektrony různě v závislosti na rychlosti elektronů ve srovnání s rychlostí světla . Relativistické efekty jsou výraznější u těžkých prvků, protože pouze v těchto prvcích dosahují elektrony dostatečné rychlosti, aby prvky měly vlastnosti, které se liší od toho, co předpovídá nerelativistická chemie.
Dějiny
Počínaje rokem 1935 popsala Bertha Swirles relativistické zacházení s mnoha elektronovým systémem, a to navzdory tvrzení Paula Diraca z roku 1929, že jediné nedokonalosti zbývající v kvantové mechanice „způsobují potíže pouze tehdy, jsou-li zapojeny vysokorychlostní částice, a jsou proto nemá žádný význam při zvažování atomové a molekulární struktury a běžných chemických reakcí, ve kterých je skutečně dostatečně přesná, pokud člověk zanedbá relativní variabilitu hmotnosti a rychlosti a předpokládá pouze Coulombovy síly mezi různými elektrony a atomovými jádry “.
Teoretičtí chemici z velké části souhlasili s Diracovým sentimentem až do 70. let 20. století, kdy byly v těžkých prvcích pozorovány relativistické efekty. Schrödingerova rovnice byla vyvinuta bez ohledu relativity Schrödinger 1926 článku. Na Schrödingerově rovnici (viz Kleinova -Gordonova rovnice ) byly provedeny relativistické opravy k popisu jemné struktury atomových spekter, ale tento vývoj a další nepronikly okamžitě do chemické komunity. Protože atomové spektrální čáry byly z velké části v říši fyziky a ne v chemii, většina chemiků nebyla obeznámena s relativistickou kvantovou mechanikou a jejich pozornost byla věnována lehčím prvkům typickým pro tehdejší zaměření organické chemie .
Diracov názor na roli, kterou by relativistická kvantová mechanika hrála pro chemické systémy, je špatný ze dvou důvodů. Za prvé, elektrony v atomových orbitalech s a p cestují podstatným zlomkem rychlosti světla. Za druhé, relativistické efekty vedou k nepřímým důsledkům, které jsou zvláště patrné u d a f atomových orbitalů.
Kvalitativní léčba
Jedním z nejdůležitějších a nejznámějších výsledků relativity je, že „ relativistická hmotnost “ elektronu roste s
kde jsou elektronová klidová hmotnost , rychlost elektronu a rychlost světla . Obrázek vpravo ilustruje tento relativistický efekt jako funkci rychlosti.
To má okamžitý dopad na poloměr Bohr ( ), který je dán vztahem
kde je redukovaná Planckova konstanta a α je konstanta jemné struktury (relativistická korekce pro Bohrův model ).
Arnold Sommerfeld vypočítal, že pro 1s orbitální elektron atomu vodíku s poloměrem obíhání 0,0529 nm, α ≈ 1/137. To znamená, že konstanta jemné struktury ukazuje elektron pohybující se rychlostí téměř 1/137 rychlosti světla. Lze to rozšířit na větší prvek s atomovým číslem Z pomocí výrazu v ≈ Zc /137 pro 1s elektron, kde v je jeho radiální rychlost. U zlata se Z = 79, v ≈ 0,58 c , tedy 1s elektron bude procházet 58% rychlosti světla. Když to zapojíme pro v / c v rovnici pro „relativistickou hmotnost“, zjistíme, že m rel = 1,22 m e , a když to zadáme pro Bohrův poloměr nad tím, zjistíme, že se poloměr zmenší o 22%.
Pokud někdo nahradí „relativistickou hmotnost“ do rovnice pro Bohrův poloměr, může být zapsán
Z toho vyplývá, že
Vpravo je výše uvedený poměr relativistických a nerelativistických Bohrových poloměrů vynesen jako funkce rychlosti elektronu. Všimněte si, jak relativistický model ukazuje, že poloměr klesá se zvyšující se rychlostí.
Když je Bohrovo zpracování rozšířeno na vodíkové atomy , stane se Bohrův poloměr
kde je hlavní kvantové číslo a Z je celé číslo pro atomové číslo . V Bohrově modelu je moment hybnosti dán jako . Dosazením do výše uvedené rovnice a řešením pro dává
Od tohoto bodu lze atomové jednotky použít ke zjednodušení výrazu do
Dosazením tohoto výrazu do výše uvedeného Bohrova poměru získáte
V tomto okamžiku je vidět, že nízká hodnota a vysoká hodnota vede k . To odpovídá intuici: elektrony s nižšími hlavními kvantovými čísly budou mít vyšší hustotu pravděpodobnosti, že budou blíže jádru. Jádro s velkým nábojem způsobí, že elektron bude mít vysokou rychlost. Vyšší rychlost elektronů znamená zvýšenou elektronovou relativistickou hmotnost a v důsledku toho se elektrony budou po většinu času blížit jádru a tím smršťovat poloměr pro malá hlavní kvantová čísla.
Odchylky periodické tabulky
Periodická tabulka byla postavena vědci, kteří zaznamenali periodické trendy známých prvků té doby. Vzory v něm nalezené skutečně dávají periodické tabulce její sílu. Mnoho chemických a fyzikálních rozdílů mezi 5. periodou ( Rb - Xe ) a 6. periodou ( Cs - Rn ) vyplývá z větších relativistických efektů pro druhé období. Tyto relativistické efekty jsou obzvláště velké u zlata a jeho sousedů - platiny a rtuti. Důležitým kvantově relativistickým efektem je Van der Waalsova síla .
Rtuť
Rtuť (Hg) je kapalina až do -39 ° C (viz bod tání ). Spojovací síly jsou pro vazby Hg – Hg slabší než pro jeho bezprostřední sousedy, jako je kadmium (t. T. 321 ° C) a zlato (t. T. 1064 ° C). Lanthanoidů kontrakce pouze částečně odpovídá za tuto anomálii. Rtuť v plynné fázi je mezi kovy sama v tom, že se obvykle vyskytuje v monomerní formě jako Hg (g). Také se tvoří Hg 2 2+ (g) a je to stabilní druh díky relativistickému zkrácení vazby.
Hg 2 (g) netvoří, protože 6s 2 okružní smluvně relativistickými účinky a mohou se proto jen slabě účasti při spojování; ve skutečnosti musí být vazba Hg – Hg většinou výsledkem van der Waalsových sil , což vysvětluje, proč je vazba pro Hg – Hg dostatečně slabá, aby umožnila Hg být kapalinou při pokojové teplotě.
Au 2 (g) a Hg (g) jsou analogické, přinejmenším v tom, že stejný charakter rozdílu, H 2, (g) a He (g). Pro relativistickou kontrakci orbitálu 6s 2 lze plynnou rtuť nazvat pseudo vzácným plynem.
Barva zlata a cesia
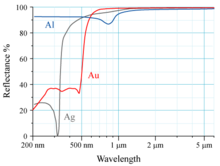
Odrazivost z hliníku (AI), stříbro (Ag) a zlato (Au) je zobrazena v grafu na pravé straně. Lidské oko vidí elektromagnetické záření o vlnové délce blízké 600 nm jako žluté. Zlato vypadá žlutě, protože pohlcuje modré světlo více než jiné viditelné vlnové délky světla; odražené světlo dopadající do oka proto ve srovnání s dopadajícím světlem postrádá modrou barvu. Vzhledem k tomu, že žlutá je komplementární k modré, díky tomu vypadá zlatý kousek pod bílým světlem pro lidské oči žlutý.
Za tuto absorpci je zodpovědný elektronický přechod z orbitálu 5d na 6s. Analogický přechod nastává u stříbra, ale relativistické efekty jsou menší než u zlata. Zatímco 4d orbitál stříbra zažívá určitou relativistickou expanzi a orbitál 5s určitou kontrakci, vzdálenost 4d – 5s ve stříbře je mnohem větší než vzdálenost 5d – 6s ve zlatě. Relativistické efekty zvyšují vzdálenost orbitálu 5d od jádra atomu a snižují vzdálenost orbitalu 6s.
Cesium, nejtěžší z alkalických kovů, které lze shromáždit v množství dostatečném pro prohlížení, má zlatý odstín, zatímco ostatní alkalické kovy jsou stříbro-bílé. Relativistické efekty však nejsou příliš významné při Z = 55 pro cesium (nedaleko od Z = 47 pro stříbro). Zlatá barva cesia pochází z klesající frekvence světla potřebného k excitaci elektronů alkalických kovů při sestupu skupiny. U lithia přes rubidium je tato frekvence v ultrafialovém záření, ale u cesia dosahuje modrofialového konce viditelného spektra; jinými slovy, plazmonická frekvence alkalických kovů se snižuje z lithia na cesium. Cesium tedy přednostně přenáší a částečně absorbuje fialové světlo, zatímco jiné barvy (s nižší frekvencí) se odrážejí; proto vypadá nažloutle.
Olověná baterie
Bez relativity by se olovo dalo chovat podobně jako cín, takže cínové baterie by měly fungovat stejně dobře jako olovo -kyselinové baterie běžně používané v automobilech. Výpočty však ukazují, že asi 10 V ze 12 V produkovaných 6článkovou olověnou baterií pochází čistě z relativistických efektů, což vysvětluje, proč cínové baterie nefungují.
Inertní párový efekt
V TI (I) ( thalia ), Pb (II) ( olovo ), a Bi (III) ( bismut ) komplexy 6s 2 dvojice elektronů existuje. Efekt inertního páru je tendence tohoto páru elektronů odolávat oxidaci v důsledku relativistické kontrakce orbitalu 6s.
Jiné efekty
Dalšími jevy běžně způsobenými relativistickými efekty jsou následující:
- Metalofilní interakce
- Stabilita zlatého aniontu, Au - , ve sloučeninách, jako je CsAu
- Krystalová struktura olova , která je místo diamantu podobná krychlovému kubickému
- Úžasná podobnost mezi zirkoniem a hafniem
- Stabilita uranylového kationtu a dalších vysokých oxidačních stavů v raných aktinidech (Pa – Am)
- Malé atomové poloměry francia a radia
- Asi 10% kontrakce lanthanoidů je přičítáno relativistické hmotnosti vysokorychlostních elektronů a menšímu Bohrovu poloměru, který je výsledkem
- V případě zlata je podstatně více než 10% jeho kontrakce způsobeno relativisticky těžkými elektrony a zlato (prvek 79) je téměř dvakrát hustší než olovo (prvek 82)
- Tendence nižších přechodných kovů k tvorbě aniontů , příkladem je platina, která kromě oxidačních stavů (I), (II), (III) a (IV) také tvoří Pt - a Pt 2− .
Viz také
Reference
Další čtení
- PA Christiansen; WC Ermler; KS Pitzer. Relativistické efekty v chemických systémech. Annual Review of Physical Chemistry 1985 , 36 , 407–432. doi : 10,1146/annurev.pc.36.100185.002203