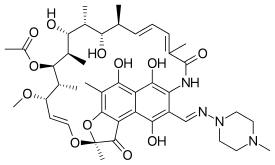
Rifampicin - Rifampicin
 | |
 | |
| Klinické údaje | |
|---|---|
| Výslovnost | / R ɪ f æ m p ə s ɪ n / |
| Obchodní názvy | Rifadin, další |
| Ostatní jména | Rifampin ( USAN USA ) |
| AHFS / Drugs.com | Monografie |
| MedlinePlus | a682403 |
| Licenční údaje | |
Kategorie těhotenství |
|
| Cesty podání |
Ústně , IV |
| ATC kód | |
| Právní status | |
| Právní status | |
| Farmakokinetické údaje | |
| Biologická dostupnost | 90 až 95% (ústy) |
| Vazba na bílkoviny | 80% |
| Metabolismus | Játra a střevní stěna |
| Poločas eliminace | 3–4 hodiny |
| Vylučování | Moč (~ 30%), stolice (60–65%) |
| Identifikátory | |
| |
| Číslo CAS | |
| PubChem CID | |
| IUPHAR/BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ČEBI | |
| CHEMBL | |
| NIAID ChemDB | |
| PDB ligand | |
| CompTox Dashboard ( EPA ) | |
| Informační karta ECHA |
100,032,997 |
| Chemická a fyzikální data | |
| Vzorec | C 43 H 58 N 4 O 12 |
| Molární hmotnost | 822,953 g · mol −1 |
| 3D model ( JSmol ) | |
| Bod tání | 183 až 188 ° C (361 až 370 ° F) |
| Bod varu | 937 ° C (1719 ° F) |
| |
| |
|
| |
Rifampicin , také známý jako rifampin , je antibiotikum používané k léčbě několika typů bakteriálních infekcí , včetně tuberkulózy (TBC), komplexu Mycobacterium avium , malomocenství a legionářské choroby . Používá se téměř vždy společně s jinými antibiotiky se dvěma výraznými výjimkami: pokud je podáván jako „preferovaná léčba, která se důrazně doporučuje“ u latentní infekce TBC; a při použití jako profylaxe po expozici k prevenci Haemophilus influenzae typu b a meningokokového onemocnění u lidí, kteří byli vystaveni těmto bakteriím. Před dlouhodobým ošetřováním člověka se doporučuje změřit jaterní enzymy a krevní obraz. Rifampicin může být podáván buď ústy nebo intravenózně.
Mezi časté nežádoucí účinky patří nevolnost, zvracení, průjem a ztráta chuti k jídlu. Často mění moč, potí se a trhá červenou nebo oranžovou barvu. Mohou se objevit problémy s játry nebo alergické reakce. Je součástí doporučené léčby aktivní tuberkulózy během těhotenství, ačkoli její bezpečnost v těhotenství není známa. Rifampicin patří do skupiny rifamycinových antibiotik. Funguje tak, že snižuje produkci RNA bakteriemi.
Rifampicin byl objeven v roce 1965, uveden na trh v Itálii v roce 1968 a schválen ve Spojených státech v roce 1971. Je na seznamu základních léků Světové zdravotnické organizace . Světová zdravotnická organizace klasifikuje rifampicin jako kriticky důležitý pro humánní medicínu. Je k dispozici jako generický lék . Rifampicin je vyráběn půdní bakterií Amycolatopsis rifamycinica .
Lékařské využití
Mykobakterie
Rifampicin se používá k léčbě tuberkulózy v kombinaci s jinými antibiotiky, jako je pyrazinamid , isoniazid a ethambutol . Pro léčbu tuberkulózy se podává denně po dobu nejméně šesti měsíců. Kombinovaná terapie se používá k prevenci vzniku rezistence a ke zkrácení délky léčby. Odolnost z Mycobacterium tuberculosis na rifampicin vyvíjí rychle, pokud je použit bez další antibiotika, s laboratorními odhady rezistence od 10 -7 až 10 -10 na tuberculosis bakterie na generaci.
Rifampicin lze použít samostatně u pacientů s latentní infekcí tuberkulózy k prevenci nebo prodloužení vývoje aktivního onemocnění, protože je přítomen pouze malý počet bakterií. Cochranův přehled nenalezl žádný rozdíl v účinnosti mezi 3 až 4měsíčním režimem rifampicinu a 6měsíčním režimem isoniazidu pro prevenci aktivní tuberkulózy u pacientů neinfikovaných HIV a pacientů, kteří dostávali rifampicin, měli nižší míru hepatotoxicity . Kvalita důkazů však byla posouzena jako nízká. Kratší 2měsíční kúra rifampicinu a pyrazinamidu byla dříve doporučena, ale vzhledem k vysoké míře hepatotoxicity se již nedoporučuje.
Rifampicin by měl být užíván na prázdný žaludek se sklenicí vody. Obvykle se užívá buď nejméně hodinu před jídlem, nebo 2 hodiny po jídle.
Rifampicin se také používá k léčbě netuberkulózních mykobakteriálních infekcí včetně lepry (Hansenova choroba) a Mycobacterium kansasii .
Při multidrogové terapii používané jako standardní léčba Hansenovy choroby se rifampicin vždy používá v kombinaci s dapsonem a clofaziminem, aby se zabránilo vzniku rezistence na léčiva.
Používá se také k léčbě infekcí Mycobacterium ulcerans spojených s vředem Buruli , obvykle v kombinaci s klarithromycinem nebo jinými antibiotiky.
Další bakterie a prvoci
V roce 2008 předběžné důkazy ukázaly, že rifampicin může být užitečný při léčbě methicilin rezistentního Staphylococcus aureus ( MRSA ) v kombinaci s jinými antibiotiky, včetně obtížně léčitelných infekcí, jako je osteomyelitida a infekce protetických kloubů. Pokud v roce 2012 byla kombinovaná terapie rifampicinem užitečná pro pyogenní vertebrální osteomyelitidu, nebylo jasné. Metaanalýza dospěla k závěru, že přidání přídavného rifampicinu k beta-laktamu nebo vankomycinu může zlepšit výsledky v bakteremii staphylococcus aureus. Novější studie však nezjistila žádný užitek z přídavného rifampicinu.
Používá se také jako preventivní léčba proti infekcím Neisseria meningitidis ( meningokokové ). Rifampicin se také doporučuje jako alternativní léčba infekcí přenášených klíšťaty patogeny Borrelia burgdorferi a Anaplasma phagocytophilum, pokud je léčba doxycyklinem kontraindikována, například u těhotných žen nebo u pacientů s anamnézou alergie na tetracyklinová antibiotika.
Někdy se také používá k léčbě infekcí druhy Listeria , Neisseria gonorrhoeae , Haemophilus influenzae a Legionella pneumophila . U těchto nestandardních indikací by mělo být před zahájením léčby rifampicinem (pokud je to možné) provedeno testování antimikrobiální citlivosti.
Enterobacteriaceae , Acinetobacter druhy a Pseudomonas druhy jsou skutečně rezistentní vůči rifampicinu.
Byl použit s amfotericinem B při převážně neúspěšných pokusech o léčbu primární amébové meningoencefalitidy způsobené Naegleria fowleri .
Rifampicin může být použit jako monoterapie po dobu několika dnů jako profylaxe proti meningitidě, ale rezistence se rychle vyvíjí během dlouhodobé léčby aktivních infekcí, takže se lék vždy používá proti aktivním infekcím v kombinaci s jinými antibiotiky.
Rifampicin je relativně neúčinný proti spirochetám , což vedlo k jeho použití jako selektivního činidla schopného je izolovat v materiálech kultivovaných v laboratořích.
Viry
Rifampicin má určitou účinnost proti viru vakcínie .
Citlivost na patogen
Minimální inhibiční koncentrace rifampicinu pro několik lékařsky významných patogenů jsou:
- Mycobacterium tuberculosis - 0,002 - 64 µg/ml
- Mycobacterium bovis - 0,125 µg/ml
- Staphylococcus aureus (rezistentní na methicilin) - ≤ 0,006–256 µg/ml
- Chlamydia pneumoniae - 0,005 µg/ml
Primární biliární cholangitida
Rifampicin se používá k léčbě svědění způsobeného primární biliární cholangitidou . Nežádoucí účinky související s léčbou zahrnují hepatotoxicitu , nefrotoxicitu , hemolýzu a interakce s jinými léky. Z těchto důvodů, jakož i z určitých etických obav týkajících se používání antibiotik mimo označení, rifampin jako velmi účinné preventivní antibiotikum pro meningitidu není považován za vhodný pro svědění.
Hidradenitis suppurativa
Rifampicin s klindamycinem byl použit k léčbě kožního onemocnění hidradenitis suppurativa .
Nepříznivé účinky
Nejzávažnějším nežádoucím účinkem je hepatotoxicita a lidé, kteří jej dostávají, často podstupují základní a časté testy jaterních funkcí, aby zjistili včasné poškození jater.
Mezi běžnější vedlejší účinky patří horečka, gastrointestinální poruchy, vyrážky a imunologické reakce. Užívání rifampicinu obvykle způsobuje, že určité tělesné tekutiny, jako je moč, pot a slzy, získají oranžovo-červenou barvu, což je benigní vedlejší účinek, který však může být děsivý, pokud se neočekává. Toho lze také použít ke sledování účinné absorpce léčiva (pokud není v moči vidět zbarvení léčiva, pacient si může přát posunout dávku léku dále od jídla nebo mléka). Odbarvení potu a slz není přímo patrné, ale pot může skvrnit světlé oblečení oranžově a slzy mohou trvale obarvit měkké kontaktní čočky. Vzhledem k tomu, že rifampicin může být vylučován do mateřského mléka, je třeba se během kojení vyvarovat kojení.
Mezi další nežádoucí účinky patří:
- Toxicita jater - hepatitida , selhání jater v závažných případech
- Respirační - dušnost
- Kožní - zrudnutí, svědění, vyrážka, hyperpigmentace, zarudnutí a slzení očí
- Břišní - nevolnost , zvracení, křeče v břiše, průjem
- Příznaky podobné chřipce- zimnice, horečka, bolest hlavy, artralgie a malátnost . Rifampicin má dobrou penetraci do mozku, což může přímo vysvětlit určitou malátnost a dysforii u menšiny uživatelů.
- Alergická reakce - vyrážky, svědění, otok jazyka nebo hrdla, silné závratě a potíže s dýcháním
Chemická struktura
Rifampicin je polyketid patřící do chemické třídy sloučenin nazývaných ansamyciny , pojmenované tak podle jejich heterocyklické struktury obsahující naftochinonové jádro překlenuté alifatickým řetězcem ansa. Naftochinonový chromofor dává rifampicinu charakteristickou červenooranžovou krystalickou barvu.
Kritickými funkčními skupinami rifampicinu v jeho inhibiční vazbě na bakteriální RNA polymerázu jsou čtyři kritické hydroxylové skupiny ansa můstku a naftholového kruhu, které tvoří vodíkové vazby se zbytky aminokyselin na proteinu.
Rifampicin je 3- (4-methyl-1-piperazinyl) -iminomethylový derivát rifamycinu SV .
Interakce
Rifampicin je nejsilnější známý induktor z jaterního cytochromu P450 enzymový systém, včetně izoenzym CYP2B6 , CYP2C8 , CYP2C9 , CYP2C19 , CYP3A4 , CYP3A5 a CYP3A7 . Zvyšuje metabolismus mnoha léků a v důsledku toho je může snižovat jejich účinnost nebo dokonce neúčinnost. Například pacienti podstupující dlouhodobou antikoagulační léčbu warfarinem musí zvýšit dávkování warfarinu a nechat si často kontrolovat srážlivost, protože jejich nedodržení by mohlo vést k nedostatečné antikoagulaci, což by mělo za následek závažné důsledky tromboembolie.
Rifampicin může snížit účinnost antikoncepčních pilulek nebo jiné hormonální antikoncepce zavedením systému cytochromu P450 do té míry, že došlo k nechtěnému otěhotnění u žen, které používají perorální antikoncepci a užívaly rifampicin i pro velmi krátké cykly (například jako profylaxe proti expozici bakteriální meningitidě).
Mezi další interakce patří snížené hladiny a nižší účinnost antiretrovirových látek , everolimu , atorvastatinu , rosiglitazonu , pioglitazonu , celecoxibu , klarithromycinu , kaspofunginu , vorikonazolu a lorazepamu .
Rifampicin je antagonistický vůči mikrobiologickým účinkům antibiotik gentamicin a amikacin. Aktivitu rifampicinu proti některým druhům mykobakterií lze potencovat isoniazidem (prostřednictvím inhibice syntézy mykolátu) a ambroxolem (prostřednictvím účinků řízených hostitelem v autofagii a farmakokinetice).
Farmakologie
Mechanismus účinku
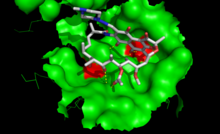
Rifampicin inhibuje bakteriální DNA-dependentní syntézu RNA inhibicí bakteriální DNA-dependentní RNA polymerázy .
Data krystalové struktury a biochemická data naznačují, že rifampicin se váže na kapsu podjednotky RNA polymerázy beta v kanálu DNA/RNA, ale mimo aktivní místo. Inhibitor brání syntéze RNA fyzickým blokováním prodloužení, a tím brání syntéze hostitelských bakteriálních proteinů. Pomocí tohoto mechanismu „sterické okluze“ rifampicin blokuje syntézu druhé nebo třetí fosfodiesterové vazby mezi nukleotidy v páteři RNA, což brání prodloužení 5 'konce transkriptu RNA za více než 2 nebo 3 nukleotidy.
V nedávné studii bylo prokázáno, že rifampicin se váže na reduktázu cytochromu P450 a mění jeho konformaci i aktivitu směrem k podpoře metabolismu progesteronu prostřednictvím CYP21A2 .
Mechanismus odporu
Rezistence na rifampicin vzniká mutacemi, které mění zbytky vazebného místa rifampicinu na RNA polymeráze, což vede ke snížení afinity k rifampicinu. Rezistenční mutace mapuje gen rpoB , kódující beta podjednotku RNA polymerázy. Většina mutací rezistence v E. coli je ve 3 klastrech na rpoB . Klastr I je aminokyselina 509 až 533, klastr II je aminokyselina 563 až 572 a klastr III je aminokyselina 687.
Při popisu mutací v rpoB u jiných druhů se obvykle používá odpovídající počet aminokyselin v E. coli . U Mycobacterium tuberculosis je většina mutací vedoucích k rezistenci na rifampicin v klastru I, v 81bp hotspotové jádrové oblasti zvané RRDR pro „oblast určující rezistenci na rifampcin“. Nejběžnější mutací je změna aminokyseliny 531 ze serinu na leucin, která je výsledkem změny v sekvenci DNA TCG na TTG. Rezistence na tuberkulózu se také objevila v důsledku mutací v N-koncové oblasti rpoB a klastru III.
Alternativní mechanismus rezistence je prostřednictvím Arr-katalyzované ADP-ribosylace rifampicinu. S pomocí enzymu Arr produkovaného patogenem Mycobacterium smegmatis se ADP-ribóza přidá k rifampicinu v jedné z jeho hydroxyskupin s ansa řetězcem, čímž se lék deaktivuje.
Rezistence při tuberkulóze
Mykobakteriální rezistence na rifampicin se může vyskytovat samostatně nebo společně s rezistencí na jiná antituberkulární léčiva první linie. Včasná detekce takové multirezistentní nebo značně rezistentní tuberkulózy je rozhodující pro zlepšení výsledků pacientů zavedením vhodné léčby druhé linie a pro snížení přenosu tuberkulózy odolné vůči lékům. Tradiční metody detekce rezistence zahrnují mykobakteriální kulturu a testování citlivosti na léčivo, jejichž výsledky mohou trvat až 6 týdnů. Test Xpert MTB/RIF je automatizovaný test, který dokáže detekovat rezistenci na rifampicin a také diagnostikovat tuberkulózu. Cochrane přezkoumání aktualizována v roce 2014 k závěru, že pro detekci rifampicin odporu, Xpert MTB / RIF byl přesný, že je (95%), citlivý a (98%), specifické.
Farmakokinetika
Perorálně podávaný rifampicin má za následek maximální plazmatické koncentrace přibližně za 2–4 hodiny. Kyselina 4-aminosalicylová (další lék proti tuberkulóze ) významně snižuje absorpci rifampicinu a maximální koncentrace mohou být nižší. Pokud musí být tato dvě léčiva používána souběžně, musí být podávána odděleně s intervalem 8 až 12 hodin mezi podáním.
Rifampicin se snadno vstřebává z gastrointestinálního (GI) traktu; jeho esterová funkční skupina je rychle hydrolyzována ve žluči a je katalyzována vysokým pH a esterázami specifickými pro substrát . Asi po 6 hodinách je téměř veškerý lék deacetylován. I v této deacetylované formě je rifampicin stále silným antibiotikem; však již nemůže být znovu absorbován střevy a je vyloučen z těla. Pouze asi 7% podaného léčiva se vylučuje v nezměněné formě močí, ačkoli vylučování močí tvoří pouze asi 30% vylučování léčiva. Asi 60% až 65% se vylučuje stolicí.
Poločas rifampicinu se pohybuje v rozmezí 1,5 až 5,0 hodiny, když porucha funkce jater významně to zvyšuje. Konzumace jídla brání jeho absorpci z GI traktu a lék je rychleji eliminován. Když je rifampicin užíván s jídlem, jeho maximální koncentrace v krvi klesá o 36%. Antacida neovlivňují jeho absorpci. Snížení absorpce rifampicinu s jídlem někdy stačí k tomu, aby znatelně ovlivnilo barvu moči, což lze použít jako ukazatel, zda byla dávka léčiva účinně absorbována či nikoli.
Distribuce léčiva je vysoká v celém těle a dosahuje účinných koncentrací v mnoha orgánech a tělních tekutinách, včetně mozkomíšního moku . Jelikož je látka samotná červená, je toto vysoké rozložení důvodem oranžovo-červené barvy slin, slz, potu, moči a výkalů. Asi 60% až 90% léčiva se váže na plazmatické bílkoviny.
Použití v biotechnologiích
Rifampicin inhibuje bakteriální RNA polymerázu, proto se běžně používá k inhibici syntézy hostitelských bakteriálních proteinů během exprese rekombinantního proteinu v bakteriích. RNA kódující rekombinantní gen je obvykle transkribována z DNA virovou T7 RNA polymerázou , která není ovlivněna rifampicinem.
Dějiny
V roce 1957 byl vzorek půdy z borového lesa na francouzské riviéře přivezen k analýze do výzkumné laboratoře Lepetit Pharmaceuticals v italském Miláně . Tam výzkumná skupina vedená Piero Sensi a Maria Teresa Timbal objevila novou bakterii. Tento nový druh produkoval novou třídu molekul s antibiotickou aktivitou. Protože Sensi, Timbal a vědci měli obzvláště rádi francouzskou krimi Rififi (o loupeži drahokamů a konkurenčních gangech), rozhodli se tyto sloučeniny nazvat rifamyciny . Po dvou letech pokusů o získání stabilnějších polosyntetických produktů byla v roce 1965 vyrobena nová molekula s vysokou účinností a dobrou snášenlivostí, která dostala název rifampicin.
Rifampicin byl poprvé prodán v Itálii v roce 1968 a byl schválen FDA v roce 1971.
Společnost a kultura
Nečistoty způsobující rakovinu
V srpnu 2020 se americký úřad pro kontrolu potravin a léčiv (FDA) dozvěděl o nitrosaminových nečistotách v určitých vzorcích rifampinu. FDA a výrobci zkoumají původ těchto nečistot v rifampinu a agentura vyvíjí testovací metody pro regulátory a průmysl k detekci 1-methyl-4-nitrosopiperazinu (MNP). MNP patří do třídy nitrosaminů, z nichž některé jsou klasifikovány jako pravděpodobné nebo možné lidské karcinogeny (látky, které by mohly způsobit rakovinu), na základě laboratorních testů, jako jsou studie karcinogenity hlodavců. Ačkoli nejsou k dispozici žádné údaje pro přímé hodnocení karcinogenního potenciálu MNP, byly k výpočtu mezních hodnot celoživotní expozice pro MNP použity informace dostupné o úzce příbuzných sloučeninách nitrosaminu.
V lednu 2021 FDA pokračuje ve vyšetřování přítomnosti 1-methyl-4-nitrosopiperazinu (MNP) v rifampinu nebo 1-cyklopentyl-4-nitrosopiperazinu (CPNP) v rifapentinu schváleném k prodeji v USA.
Jména
Rifampicin je INN a BAN , zatímco rifampin je USAN . Rifampicin může být zkrácen R, RMP, RA, RF nebo RIF (USA).
Rifampicin je také ve Spojených státech známý jako rifaldazin, rofact a rifampin, také jako rifamycin SV.
Jeho chemický název je 5,6,9,17,19,21-hexahydroxy-23-methoxy-2,4,12,16,18,20,22-heptamethyl-8- [N- (4-methyl-1- piperazinyl) formimidoyl] -2,7- (epoxypentadeca [1,11,13] trienimino) -nafto [2,1-b] furan-1,11 (2H) -dion 21-acetát.
Rifampicin je k dispozici pod mnoha značkami po celém světě.
Reference
externí odkazy
- „Rifampicin“ . Informační portál o drogách . Americká národní lékařská knihovna.