Selenide - Selenide
Selenidu je chemická sloučenina obsahující selen anion s oxidačního čísla -2 (Se 2- ), stejně jako síra dělá na sulfid . Chemie selenidů a sulfidů je podobná. Podobně jako u sulfidů je ve vodném roztoku selenidový iont Se 2− převládající pouze za velmi zásaditých podmínek. V neutrálních podmínkách je nejběžnější iont selenidu vodíku , HSe - . V kyselých podmínkách vzniká selenid vodíku , H 2 Se.
Některé selenidy reagují na oxidaci vzduchem. Vzhledem k větší redukční síle selenidu se selenidy kovů snadněji rozkládají na prvky než sulfidy ( teluridy jsou ještě labilnější). Selenidy elektropozitivních kovů: jako je selenid hlinitý snadno hydrolyzuje, dokonce i ve vlhkém vzduchu, za vzniku toxického plynného selenidu vodíku.
Čisté selenidové minerály jsou vzácné, místo toho má selen tendenci částečně nahrazovat sulfid v mnoha sulfidových minerálech . Stupeň substituce je pouze komerčně zajímavý pro rudy sulfidu měďnatého, v takovém případě se selen získává jako vedlejší produkt rafinace mědi. Některé selenidové minerály zahrnují ferroselit a umangit .
= Reakce
Selenidy alkalických kovů reagují s elementárním selenem za vzniku solí polyselenidu .
Selenid kovu
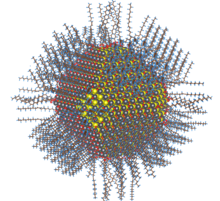
Kvantové tečky a nanočástice selenidu kovu lze připravit řadou dostupných syntetických metod, z nichž mnohé vyžadují vysoké teploty a nebezpečné prekurzorové sloučeniny. Částice mohou být přizpůsobeny pro různé aplikace změnou ligandů koordinovaných na kladně nabitou vnější vrstvu. K použití je k dispozici mnoho reakcí výměny ligandů, které obchodují s ligandy typu X, L a Z, jejichž mechanismus je stále ve studii.
Aplikace
Kvantové tečky na bázi selenidů kovů byly značně pro své charakteristické spektrální vlastnosti. Slitiny jádra a skořepiny sulfidu kademnatého a selenidu jsou zajímavé pro zobrazování a fototerapii .
Příklady
- Selenid galia (II)
- Selenid india (III)
- Selenid sodný
- Selenid kademnatý
- Selenid zinečnatý
- Selenid olova
- Selenid mědi