Peroxid sodný - Sodium peroxide

|
|
|
|

|
|
| Jména | |
|---|---|
| Ostatní jména
Oxid disodný
Flocool Solozone Peroxid sodný |
|
| Identifikátory | |
|
3D model ( JSmol )
|
|
| ChemSpider | |
| Informační karta ECHA |
100,013,828 |
| Číslo ES | |
|
PubChem CID
|
|
| Číslo RTECS | |
| UNII | |
| UN číslo | 1504 |
|
CompTox Dashboard ( EPA )
|
|
|
|
|
|
| Vlastnosti | |
| Na 2 O 2 | |
| Molární hmotnost | 77,98 g/mol |
| Vzhled | žlutý až bílý prášek |
| Hustota | 2,805 g / cm 3 |
| Bod tání | 460 ° C (860 ° F; 733 K) (rozkládá se) |
| Bod varu | 657 ° C (1215 ° F; 930 K) (rozkládá se) |
| reaguje prudce | |
| Rozpustnost | rozpustný v kyselině nerozpustný v zásadě reaguje s ethanolem |
| −28,10 · 10 −6 cm 3 /mol | |
| Struktura | |
| šestihranný | |
| Termochemie | |
|
Tepelná kapacita ( C )
|
89,37 J/(mol · K) |
|
Standardní molární
entropie ( S |
95 J/(mol · K) |
|
Standardní entalpie
tvorby (Δ f H ⦵ 298 ) |
−515 kJ · mol −1 |
|
Gibbsova volná energie (Δ f G ˚)
|
−446,9 kJ/mol |
| Nebezpečí | |
| Bezpečnostní list | Externí bezpečnostní list |
|
Klasifikace EU (DSD) (zastaralá)
|
|
| R-věty (zastaralé) | R8 , R35 |
| S-věty (zastaralé) | (S1/2) , S8 , S27 , S39 , S45 |
| NFPA 704 (ohnivý diamant) | |
| Bod vzplanutí | Nehořlavé |
| Související sloučeniny | |
|
Jiné kationty
|
Peroxid lithný Peroxid draselný Peroxid rubidia Peroxid česný |
|
Oxid sodný Superoxid sodný |
|
|
Související sloučeniny
|
Hydroxid sodný Peroxid vodíku |
|
Pokud není uvedeno jinak, jsou údaje uvedeny pro materiály ve standardním stavu (při 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Reference na infobox | |
Peroxid sodný je anorganická sloučenina se vzorcem Na 2 O 2 . Tato nažloutlá pevná látka je produktem sodíku zapáleného v přebytku kyslíku. Je to silná základna. Tento kovový peroxid existuje v několika hydrátů a peroxyhydrates včetně Na 2 O 2 · 2H 2 O 2 · 4H 2 O, Na 2 O 2 · 2H 2 O, Na 2 O 2 · 2H 2 O 2 , a Na 2 O 2 · 8H 2 O. Oktahydrát, který se snadno připravuje, je na rozdíl od bezvodého materiálu bílý.
Vlastnosti
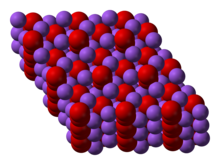
Peroxid sodný krystalizuje s hexagonální symetrií. Po zahřátí hexagonální forma prochází přechodem do fáze neznámé symetrie při 512 ° C. Při dalším zahřívání nad teplotu varu 657 ° C se sloučenina rozkládá na Na 2 O a uvolňuje O 2 .
- 2 Na 2 O 2 → 2 Na 2 O + O 2
Příprava
Oktahydrát se vyrábí zpracováním hydroxidu sodného s peroxidem vodíku.
Peroxid sodný lze připravit ve velkém měřítku reakcí kovového sodíku s kyslíkem při 130–200 ° C, což je proces, při kterém vzniká oxid sodný , který v samostatném stupni absorbuje kyslík:
- 4 Na + O 2 → 2 Na 2 O
- 2 Na 2 O + O 2 → 2 Na 2 O 2
Může být také vyroben průchodem ozónového plynu přes pevný jodid sodný uvnitř platinové nebo palladiové trubice. Ozón oxiduje sodík za vzniku peroxidu sodného. Jódu může být sublimovaný pomocí mírného zahřívání. Platina nebo palladium katalyzuje reakci a není napadena peroxidem sodným.
Využití
Peroxid sodný hydrolyzuje , čímž se získá hydroxid sodný a peroxid vodíku podle reakce
- Na 2 O 2 + 2 H 2 O → 2 NaOH + H 2 O 2
Peroxid sodný byl používán k bělení buničiny pro výrobu papíru a textilií. V současné době se používá hlavně pro specializované laboratorní operace, např. Těžbu minerálů z různých rud. Peroxid sodný může být pod obchodními názvy Solozone a Flocool . V chemických přípravcích se jako oxidační činidlo používá peroxid sodný. Používá se také jako zdroj kyslíku reakcí s oxidem uhličitým za vzniku kyslíku a uhličitanu sodného:
- 2 Na 2 O 2 + 2 CO 2 → 2 Na 2 CO 3 + O 2
Je tedy zvláště užitečný v potápěčských zařízeních, ponorkách atd. Peroxid lithný a superoxid draselný mají podobné použití.

