Threonin - Threonine

Kosterní vzorec z L -threonin
|
|||
|
|
|||
| Jména | |||
|---|---|---|---|
|
Název IUPAC
Threonin
|
|||
| Ostatní jména
2-Amino-3-hydroxybutanová kyselina
|
|||
| Identifikátory | |||
|
3D model ( JSmol )
|
|||
| ČEBI | |||
| CHEMBL | |||
| ChemSpider | |||
| DrugBank | |||
| Informační karta ECHA |
100 000,704 |
||
| Číslo ES | |||
|
PubChem CID
|
|||
| UNII | |||
|
CompTox Dashboard ( EPA )
|
|||
|
|||
|
|||
| Vlastnosti | |||
| C 4 H 9 N O 3 | |||
| Molární hmotnost | 119,120 g · mol −1 | ||
| (H20, g/dl) 10,6 (30 °), 14,1 (52 °), 19,0 (61 °) | |||
| Kyselost (p K a ) | 2,63 (karboxyl), 10,43 (amino) | ||
| Stránka doplňkových údajů | |||
|
Index lomu ( n ), dielektrická konstanta (ε r ) atd. |
|||
|
Termodynamická
data |
Fázové chování pevná látka – kapalina – plyn |
||
| UV , IR , NMR , MS | |||
|
Pokud není uvedeno jinak, jsou údaje uvedeny pro materiály ve standardním stavu (při 25 ° C [77 ° F], 100 kPa). |
|||
|
|
|||
| Reference na infobox | |||
Threonin (symbol Thr nebo T ) je aminokyselina , která se používá v biosyntéze z proteinů . Obsahuje a-aminoskupinu (která je v protonovaném -NH+
3forma za biologických podmínek), je karboxylová skupina (která je v deprotonované -COO - forma za biologických podmínek), a postranní řetězec obsahující hydroxylové skupiny , takže je polární bez náboje aminokyselin. Je nezbytný u lidí, což znamená, že si ho tělo neumí syntetizovat: musí být získáno ze stravy. Threonin je syntetizován z aspartátu v bakteriích, jako je E. coli . Je kódován všemi kodony začínajícími AC (ACU, ACC, ACA a ACG).
Boční řetězce threoninu jsou často vázány vodíkem; nejběžnější vytvořené malé motivy jsou založeny na interakcích se serinem : ST obraty , ST motivy (často na začátku alfa helixy) a ST sponky (obvykle uprostřed alfa helixy).
Modifikace
Threoninový zbytek je citlivý na četné posttranslační modifikace . Hydroxylové postranní řetězec může podstoupit O -vázané glykosylace . Kromě toho, threoninové zbytky podrobeny fosforylaci působením threoninovým kinázy . Ve své fosforylované formě může být označován jako fosfothreonin . Fosfothreonin má tři potenciální koordinační místa (karboxyl, amin a fosfátová skupina) a stanovení způsobu koordinace mezi fosforylovanými ligandy a ionty kovů vyskytujícími se v organismu je důležité pro vysvětlení funkce fosfothreoninu v biologických procesech.
Dějiny
Threonin byl poslední z 20 běžných proteinogenních aminokyselin, které byly objeveny. Objevil ho v roce 1936 William Cumming Rose , spolupracující s Curtisem Meyerem. Aminokyselina byla pojmenována threonin, protože měla podobnou strukturu jako kyselina threonová , monosacharid se čtyřmi uhlíky s molekulárním vzorcem C 4 H 8 O 5
Stereoisomery
  |
|
L -Treonin (2 S , 3 R ) a D -Treonin (2 R , 3 S ) |
 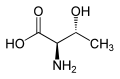 |
| L -Allothreonin (2 S , 3 S ) a D -Allothreonine (2 R , 3 R ) |
Threonin je jednou ze dvou proteinogenních aminokyselin se dvěma stereogenními centry, druhým je izoleucin . Threonin může existovat ve čtyřech možných stereoizomerech s následujícími konfiguracemi: (2 S , 3 R ), (2 R , 3 S ), (2 S , 3 S ) a (2 R , 3 R ). Název L- threonin se však používá pro jeden jediný stereoizomer , ( 2S , 3R ) -2-amino-3-hydroxybutanovou kyselinu. Druhý stereoizomer (2 S , 3 S ), který se v přírodě vyskytuje jen zřídka, se nazývá L -alothreonin. Dva stereoizomery ( 2R , 3S )-a ( 2R , 3R ) -2-amino-3-hydroxybutanová kyselina mají pouze malý význam.
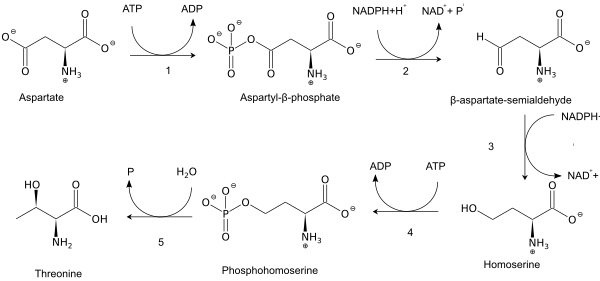
Biosyntéza
Jako esenciální aminokyselina není threonin syntetizován u lidí a musí být přítomen v bílkovinách ve stravě. Dospělí lidé vyžadují přibližně 20 mg/kg tělesné hmotnosti/den. V rostlinách a mikroorganismech je threonin syntetizován z kyseliny asparagové prostřednictvím α-aspartyl-semialdehydu a homoserinu . Homoserin prochází O -fosforylací ; tento fosfátový ester podléhá hydrolýze souběžně s přemístěním skupiny OH. Enzymy zapojené do typické biosyntézy threoninu zahrnují:
- aspartokinasa
- β-aspartát semialdehyd dehydrogenáza
- homoserine dehydrogenase
- homoserin kináza
- threonin syntáza .
Metabolismus
Threonin je metabolizován nejméně třemi způsoby:
- U mnoha zvířat se přeměňuje na pyruvát prostřednictvím threonindehydrogenázy . Meziprodukt v této dráze může podstoupit thiolýzu s CoA za vzniku acetyl-CoA a glycinu .
- U lidí je gen pro threonindehydrogenázu neaktivní pseudogen , proto je threonin přeměněn na α-ketobutyrát . Mechanismus prvního kroku je analogický mechanismu katalyzovanému serinovou dehydratázou a reakce serinové a threoninové dehydratázy jsou pravděpodobně katalyzovány stejným enzymem.
- V mnoha organismů, je O-fosforylovány pomocí kinázy přípravný k dalšímu metabolismu. To je zvláště důležité u bakterií jako součást biosyntézy kobalaminu ( vitamín B12 ), protože produkt je přeměněn na (R) -1-aminopropan-2-ol pro začlenění do vedlejšího řetězce vitaminu.
- Threonin se používá k syntéze glycinu během endogenní produkce L-karnitinu v mozku a játrech potkanů.
Prameny
Mezi potraviny s vysokým obsahem threoninu patří tvaroh , drůbež , ryby , maso , čočka , fazole černé želvy a sezamová semínka.
Racemický threonin lze připravit z kyseliny krotonové alfa-funkcionalizací za použití octanu rtuťnatého .