Triethylaluminium - Triethylaluminium

|
|
|
|
| Jména | |
|---|---|
|
Název IUPAC
Triethylaluman
|
|
| Identifikátory | |
|
3D model ( JSmol )
|
|
| Zkratky | ČAJ, ČAJ, TEAL |
| ChemSpider | |
| Informační karta ECHA |
100,002,382 |
| Číslo ES | |
|
PubChem CID
|
|
| UNII | |
|
CompTox Dashboard ( EPA )
|
|
|
|
| Vlastnosti | |
| C 12 H 30 Al 2 | |
| Molární hmotnost | 228,335 g · mol −1 |
| Vzhled | Bezbarvá kapalina |
| Hustota | 0,8324 g/ml při 25 ° C |
| Bod tání | -46 ° C (-51 ° F, 227 K) |
| Bod varu | 128 až 130 ° C (262 až 266 ° F; 401 až 403 K) při 50 mmHg |
| Nebezpečí | |
| Hlavní nebezpečí | pyroforický |
| R-věty (zastaralé) | R14 R17 R34 |
| S-věty (zastaralé) | S16 S43 S45 |
| NFPA 704 (ohnivý diamant) | |
| Bod vzplanutí | −18 ° C (0 ° F, 255 K) |
| Související sloučeniny | |
|
Související sloučeniny
|
Trimethylaluminium |
|
Pokud není uvedeno jinak, jsou údaje uvedeny pro materiály ve standardním stavu (při 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Reference na infobox | |
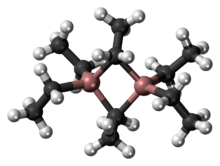
Triethylaluminium je jedním z nejjednodušších příkladů organoaluminiové sloučeniny. Přes svůj název má vzorec Al 2 ( C 2 H 5 ) 6 (zkráceně Al 2 Et 6 nebo TEA), protože existuje jako dimer . Tato bezbarvá kapalina je pyroforická . Je to průmyslově důležitá sloučenina, blízce příbuzná trimethylaluminiu .
Struktura a lepení
Struktura a vazby v Al 2 R 6 a diboranu jsou analogické (R = alkyl). Pokud jde o Al 2 Me 6 , vzdálenosti Al-C (terminál) a Al-C (přemosťování) jsou 1,97, respektive 2,14 Å. Centrum Al je čtyřboké. Atomy uhlíku přemosťujících ethylových skupin jsou obklopeny pěti sousedy: uhlíkem, dvěma atomy vodíku a dvěma atomy hliníku. Ethylové skupiny se snadno vyměňují intramolekulárně. Při vyšších teplotách dimer praskne na monomerní AlEt 3 .
Syntéza a reakce
Triethylaluminium může být vytvořeno několika způsoby. Objev efektivní cesty byl významným technologickým úspěchem. Vícestupňový proces využívá kovový hliník, plynný vodík a ethylen , shrnuté následovně:
- 2 Al + 3 H 2 + 6 C 2 H 4 → Al 2 Et 6
Díky této účinné syntéze je triethylaluminium jednou z nejdostupnějších organoaluminiových sloučenin.
Triethylaluminium lze také generovat z ethylaluminium sesquichloridu (Al 2 Cl 3 Et 3 ), který vzniká zpracováním hliníkového prášku chloroethanem . Redukce ethylaluminium sesquichloridu alkalickým kovem, jako je sodík, poskytne triethylaluminium:
- 3 Al 2 Cl 3 Et 3 + 9 Na → 2 Al 2 Et 6 + 2 Al + 9 NaCl
Reaktivita
Al -C vazby triethylaluminia jsou polarizovány do takové míry, že uhlík je snadno protonován a uvolňuje etan:
- Al 2 Et 6 + 6 HX → 2 AlX 3 + 6 EtH
K této reakci lze použít i slabé kyseliny, jako jsou koncové acetyleny a alkoholy.
Vazba mezi dvojicí center hliníku je relativně slabá a může být štěpena Lewisovými bázemi (L) za vzniku aduktů vzorce AlEt 3 L:
- Al 2 Et 6 + 2 L → 2 LAlEt 3
Aplikace
Prekurzory mastných alkoholů
Triethylaluminium se průmyslově používá jako meziprodukt při výrobě mastných alkoholů , které se přeměňují na detergenty . První krok zahrnuje oligomerizaci ethylenu Aufbauovou reakcí, která poskytne směs trialkylaluminiových sloučenin (zjednodušeně zde jako oktylové skupiny):
- Al 2 (C 2 H 5 ) 6 + 18 C 2 H 4 → Al 2 (C 8 H 17 ) 6
Následně se tyto trialkylové sloučeniny oxidují na alkoxidy hliníku , které se poté hydrolyzují:
- Al 2 (C 8 H 17 ) 6 + 3 O 2 → Al 2 (OC 8 H 17 ) 6
- Al 2 (OC 8 H 17 ) 6 + 6 H 2 O → 6 C 8 H 17 OH + 2 "Al (OH) 3 "
Kokatalyzátory při polymeraci olefinů
Při katalýze Ziegler-Natta se používá velké množství TEAL a příbuzných alkylů hliníku . Slouží k aktivaci katalyzátoru přechodného kovu jak jako redukční činidlo, tak jako alkylační činidlo . TEAL také funguje tak, že zachycuje vodu a kyslík.
Činidlo v organické a organokovové chemii
Triethylaluminium má specializované použití jako prekurzor jiných organoaluminiových sloučenin, jako je diethylaluminiumkyanid :
Pyroforický prostředek
Triethylaluminium se vznítí při kontaktu se vzduchem a vznítí se a/nebo se rozkládá při kontaktu s vodou a jakýmkoli jiným oxidačním činidlem - je to jedna z mála látek dostatečně pyroforických, aby se vznítila při kontaktu s kryogenním kapalným kyslíkem . Entalpie spalování , Δ c H °, je -5105,70 ± 2,90 K J / mol (-22,36 kJ / g ). Díky snadnému zapalování je obzvláště žádoucí jako zapalovač raketových motorů . SpaceX Falcon 9 raketa používá triethylaluminium- triethylboranu směsi jako prvního stupně zapalovačem.
Triethylaluminium zahuštěný s polyisobutylen se používá jako zápalné zbraně , jako alternativa k pyroforní napalmu ; např. v klipu M74 držící čtyři rakety pro odpalovací zařízení M202A1 . V této aplikaci je známý jako TPA, zahuštěný pyrotechnický prostředek nebo zahuštěný pyroforický prostředek . Obvyklé množství zahušťovadla je 6%. Množství zahušťovadla lze snížit na 1%, pokud se přidají další ředidla. Například n-hexan lze použít se zvýšenou bezpečností tím, že se sloučenina stane nepyroforickou, dokud se ředidlo neodpaří, přičemž v tomto okamžiku vzniká kombinovaná ohnivá koule jak z par trietylaluminia, tak z hexanu. M202 byl vyřazen z provozu v polovině 80. let kvůli problémům s bezpečností, přepravou a skladováním. Někteří viděli omezené použití ve válce v Afghánistánu proti jeskyním a opevněným sloučeninám.
Viz také
- Triethylboran , používaný jako zapalovač v proudových / náporových motorech Pratt & Whitney J58 .
- Trimethylaluminium


![{\ displaystyle {\ ce {{1/2Al2Et6}+ HCN ->}} \ {\ tfrac {1} {n}} {\ ce {[Et2AlCN]}} _ {n}+ {\ ce {C2H6}} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/b73bebe835386dae4e699b7a9b65a76a0f6853f3)