Triple point - Triple point
V termodynamice je trojným bodem látky teplota a tlak, při kterém tři fáze ( plyn , kapalina a pevná látka ) této látky koexistují v termodynamické rovnováze . Je to teplota a tlak, při kterých se setkávají sublimační křivka, fúzní křivka a křivka vaporizace . Například trojitý bod rtuti se vyskytuje při teplotě -38,83440 ° C (-37,90192 ° F) a tlaku 0,165 m Pa .
Kromě trojného bodu pro pevnou, kapalnou a plynnou fázi může trojitý bod zahrnovat více než jednu pevnou fázi pro látky s více polymorfními fázemi . Helium-4 je speciální případ, který představuje trojitý bod zahrnující dvě různé tekuté fáze ( bod lambda ).
Trojitý bod vody byl použit k definování kelvinů , základní jednotky termodynamické teploty v Mezinárodním systému jednotek (SI). Hodnota trojného bodu vody byla stanovena podle definice, nikoli měřena, ale to se změnilo s redefinicí základních jednotek SI v roce 2019 . Trojité body několika látek se používají k definování bodů v mezinárodní teplotní stupnici ITS-90 v rozmezí od trojného bodu vodíku (13,8033 K) do trojného bodu vody (273,16 K, 0,01 ° C nebo 32,018 ° F) .
Termín „trojitý bod“ vytvořil v roce 1873 James Thomson , bratr lorda Kelvina .
Trojitý bod vody
Trojitý bod plyn – kapalina – tuhá látka
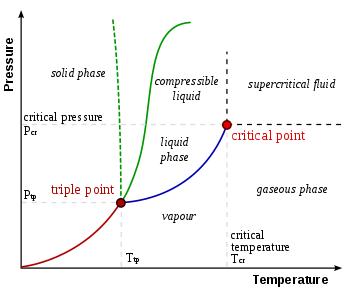
Jediná kombinace tlaku a teploty, při které může kapalná voda , pevný led a vodní pára koexistovat ve stabilní rovnováze, nastává přesně při 273.1600 K (0,0100 ° C; 32,0180 ° F) a parciálním tlaku par 611,657 pascalů (6,11657 mbar; 0,00603659 atm). V tom okamžiku je možné změnit veškerou látku na led, vodu nebo páru provedením libovolně malých změn tlaku a teploty. I když je celkový tlak systému výrazně nad trojným bodem vody, za předpokladu, že parciální tlak vodní páry je 611,657 pascalů , pak může být systém stále uveden do trojného bodu vody. Přesně řečeno, povrchy oddělující různé fáze by měly být také dokonale ploché, aby se negovaly účinky povrchového napětí.
Trojitý bod vody plyn - kapalina - pevná látka odpovídá minimálnímu tlaku, při kterém může existovat kapalná voda. Při tlacích pod trojným bodem (jako ve vesmíru ) se pevný led při zahřívání na konstantní tlak převádí přímo na vodní páru v procesu známém jako sublimace . Nad trojným bodem se pevný led při zahřívání na konstantní tlak nejprve roztaví za vzniku kapalné vody a poté se odpaří nebo se vaří za vzniku páry při vyšší teplotě.
U většiny látek je trojitý bod plyn – kapalina – pevná látka také minimální teplotou, při které může kapalina existovat. U vody to však není pravda, protože teplota tání obyčejného ledu klesá v závislosti na tlaku, jak ukazuje přerušovaná zelená čára ve fázovém diagramu . Při teplotách těsně pod trojným bodem transformuje komprese při konstantní teplotě vodní páru nejprve na pevnou látku a poté na kapalinu (vodní led má nižší hustotu než kapalná voda, takže rostoucí tlak vede ke zkapalnění ).
Tříbodový tlak vody byl během mise Mariner 9 na Mars použit jako referenční bod k definování „hladiny moře“. Novější mise používají k definování nadmořské výšky na Marsu místo tlaku laserovou altimetrii a gravitační měření.
Fáze vysokého tlaku
Při vysokých tlacích má voda komplexní fázový diagram s 15 známými fázemi ledu a několika trojitými body, včetně 10, jejichž souřadnice jsou v diagramu znázorněny. Například trojný bod při 251 K (-22 ° C) a 210 MPa (2070 atm) odpovídá podmínkám pro soužití ledu Ih (obyčejný led), ledu III a kapalné vody, vše v rovnováze. Existují také tři body pro koexistenci tří pevných fází, například ledu II , ledu V a ledu VI při 218 K (-55 ° C) a 620 MPa (6120 atm).
U těch vysokotlakých forem ledu, které mohou existovat v rovnováze s kapalinou, diagram ukazuje, že teploty tání rostou s tlakem. Při teplotách nad 273 K (0 ° C) vede zvýšení tlaku na vodní páru nejprve v kapalné vodě a poté ve vysokotlaké formě ledu. V dosahu251–273 K , nejprve se vytvoří led I, poté tekutá voda a poté led III nebo led V, následované dalšími ještě hustšími vysokotlakými formami.

| Fáze ve stabilní rovnováze | Tlak | Teplota |
|---|---|---|
| kapalná voda, led I h a vodní pára | 611,657 Pa | 273,16 K (0,01 ° C) |
| kapalná voda, led I h a led III | 209,9 MPa | 251 K (−22 ° C) |
| kapalná voda, led III a led V | 350,1 MPa | -17,0 ° C |
| kapalná voda, led V a led VI | 632,4 MPa | 0,16 ° C |
| ledu I h , ledu II a ledu III | 213 MPa | -35 ° C |
| led II, led III a led V | 344 MPa | -24 ° C |
| led II, led V a led VI | 626 MPa | -70 ° C |
Buňky s trojitým bodem
Triple-bodové buňky se používají při kalibraci z teploměrů . Pro náročné práce jsou tříbodové články typicky naplněny vysoce čistou chemickou látkou, jako je vodík, argon, rtuť nebo voda (v závislosti na požadované teplotě). Čistota těchto látek může být taková, že pouze jedna část z milionu je kontaminující látka, nazývaná „šest devítek“, protože je čistá z 99,9999%. Pokud se jedná o buňku na vodní bázi, použije se specifická izotopová kompozice nazvaná VSMOW, protože změny v izotopickém složení způsobují malé změny v trojném bodě. Články s trojitým bodem jsou při dosahování vysoce přesných a reprodukovatelných teplot tak účinné, že mezinárodní kalibrační standard pro teploměry ITS – 90 spoléhá na tříbodové články vodíku , neonů , kyslíku , argonu , rtuti a vody, které vymezují šest jeho definované teplotní body.
Tabulka trojitých bodů
Tato tabulka uvádí trojité body plyn - kapalina - pevná látka několika látek. Pokud není uvedeno jinak, data pocházejí z amerického Národního úřadu pro standardy (nyní NIST , Národní institut pro standardy a technologie).
| Látka | T [ K ] ( ° C ) | p [ kPa ]* ( atm ) |
|---|---|---|
| Acetylén | 192,4 K (-80,7 ° C) | 120 kPa (1,2 atm) |
| Amoniak | 195,40 K (-77,75 ° C) | 6,060 kPa (0,05981 atm) |
| Argon | 83,8058 K (−189,3442 ° C) | 68,9 kPa (0,680 atm) |
| Arsen | 1090 K (820 ° C) | 3628 kPa (35,81 atm) |
| Butan | 134,6 K (-138,6 ° C) | 7 × 10 −4 kPa (6,9 × 10 −6 atm) |
| Uhlík ( grafit ) | 4765 K (4492 ° C) | 10,132 kPa (100,00 atm) |
| Oxid uhličitý | 216,55 K (-56,60 ° C) | 517 kPa (5,10 atm) |
| Kysličník uhelnatý | 68,10 K (-205,05 ° C) | 15,37 kPa (0,1517 atm) |
| Chloroform | 175,43 K (-97,72 ° C) | 0,870 kPa (0,00859 atm) |
| Deuterium | 18,63 K (-254,52 ° C) | 17,1 kPa (0,169 atm) |
| Etan | 89,89 K (−183,26 ° C) | 1,1 × 10 −3 kPa (1,1 × 10 −5 atm) |
| Ethanol | 150 K (−123 ° C) | 4,3 × 10 −7 kPa (4,2 × 10 −9 atm) |
| Ethylen | 104,0 K (-169,2 ° C) | 0,12 kPa (0,0012 atm) |
| Kyselina mravenčí | 281,40 K (8,25 ° C) | 2,2 kPa (0,022 atm) |
| Helium-4 ( lambda bod ) | 2,1768 K (-270,9732 ° C) | 5,048 kPa (0,04982 atm) |
| Helium-4 ( hcp - bcc −He-II) | 1,463 K (-271,687 ° C) | 26,036 kPa (0,25696 atm) |
| Helium-4 (bcc-He-I-He-II) | 1,762 K (-271,388 ° C) | 29,725 kPa (0,29336 atm) |
| Helium-4 (hcp − bcc − He-I) | 1,772 K (-271,378 ° C) | 30,016 kPa (0,29623 atm) |
| Hexafluorethan | 173,08 K (-100,07 ° C) | 26,60 kPa (0,2625 atm) |
| Vodík | 13,8033 K (-259,3467 ° C) | 7,04 kPa (0,0695 atm) |
| Chlorovodík | 158,96 K (-114,19 ° C) | 13,9 kPa (0,137 atm) |
| Jód | 386,65 K (113,50 ° C) | 12,07 kPa (0,1191 atm) |
| Izobutan | 113,55 K (-159,60 ° C) | 1,9481 × 10 −5 kPa (1,9226 × 10 −7 atm) |
| Krypton | 115,76 K (-157,39 ° C) | 74,12 kPa (0,7315 atm) |
| Rtuť | 234,3156 K (-38,8344 ° C) | 1,65 × 10 −7 kPa (1,63 × 10 −9 atm) |
| Metan | 90,68 K (−182,47 ° C) | 11,7 kPa (0,115 atm) |
| Neon | 24,5561 K (-248,5939 ° C) | 43,332 kPa (0,42765 atm) |
| Oxid dusnatý | 109,50 K (-163,65 ° C) | 21,92 kPa (0,2163 atm) |
| Dusík | 63,18 K (-209,97 ° C) | 12,6 kPa (0,124 atm) |
| Oxid dusičitý | 182,34 K (-90,81 ° C) | 87,85 kPa (0,8670 atm) |
| Kyslík | 54,3584 K (-218,7916 ° C) | 0,14625 kPa (0,0014434 atm) |
| Palladium | 1825 K (1552 ° C) | 3,5 × 10 −3 kPa (3,5 × 10 −5 atm) |
| Platina | 2045 K (1772 ° C) | 2 × 10 −4 kPa (2,0 × 10 −6 atm) |
| Radon | 202 K (-71 ° C) | 70 kPa (0,69 atm) |
| (mono) Silane | 88,48 K (-184,67 ° C) | 0,019644 kPa (0,00019387 atm) |
| Oxid siřičitý | 197,69 K (-75,46 ° C) | 1,67 kPa (0,0165 atm) |
| Titan | 1.941 K (1668 ° C) | 5,3 × 10 −3 kPa (5,2 × 10 −5 atm) |
| Hexafluorid uranu | 337,17 K (64,02 ° C) | 151,7 kPa (1,497 atm) |
| Voda | 273,16 K (0,01 ° C) | 0,611657 kPa (0,00603659 atm) |
| Xenon | 161,3 K (−111,8 ° C) | 81,5 kPa (0,804 atm) |
| Zinek | 692,65 K (419,50 ° C) | 0,065 kPa (0,00064 atm) |
Poznámky:
- Pro srovnání, typický atmosférický tlak je 101,325 kPa (1 atm).
- Před novou definicí jednotek SI byl trojný bod vody, 273,16 K, přesné číslo.
Viz také
Reference
externí odkazy
-
 Média související s Triple point na Wikimedia Commons
Média související s Triple point na Wikimedia Commons

