Uranocen - Uranocene
|
|
|||
|
|
|||
| Jména | |||
|---|---|---|---|
|
Název IUPAC
Bis (η 8 -cyklooktatetraenyl) uran (IV)
|
|||
| Ostatní jména
Cyklooktatetraenid uranu
U (COT) 2 |
|||
| Identifikátory | |||
|
3D model ( JSmol )
|
|||
| ChemSpider | |||
|
PubChem CID
|
|||
|
CompTox Dashboard ( EPA )
|
|||
|
|||
|
|||
| Vlastnosti | |||
| C 16 H 16 U | |||
| Molární hmotnost | 446,33 g/mol | ||
| Vzhled | zelené krystaly | ||
| Nebezpečí | |||
| Hlavní nebezpečí | pyroforický a toxický | ||
|
Pokud není uvedeno jinak, jsou údaje uvedeny pro materiály ve standardním stavu (při 25 ° C [77 ° F], 100 kPa). |
|||
|
|
|||
| Reference na infobox | |||
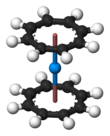
Uranocene , U (C 8 H 8 ) 2 , je organouranová sloučenina složená z atomu uranu vloženého mezi dva cyklooktatetraenidové kruhy. Byla to jedna z prvních syntetizovaných organoaktinidových sloučenin . Jedná se o zelenou pevnou látku citlivou na vzduch, která se rozpouští v organických rozpouštědlech. Uranocene, člen „ aktinocenů “, skupiny metalocenů zahrnujících prvky ze série aktinidů . Jedná se o nejstudovanější bis [8] annulen -kovový systém, i když nemá žádné známé praktické aplikace.
Syntéza, struktura a vazba
Uranocen byl poprvé popsán v roce 1968 skupinou Andrewa Streitwiesera , když byl připraven reakcí cyklooktatetraenidu dvojdrasného a tetrachloridu uranu v THF při 0 ° C:
Uranocen je vysoce reaktivní vůči kyslíku, je pyroforický na vzduchu, ale stabilní vůči hydrolýze . Rentgenová krystalová struktura uranocénu byla poprvé objasněna skupinou Kena Raymonda . Vzhledem k tomu, že molekula je U 4+ (C 8 H 8 2− ) 2 , skupiny η 8 - cyklooktatetraenidové skupiny jsou planární, jak se očekávalo u kruhu obsahujícího 10 π -elektronů , a jsou vzájemně rovnoběžné a tvoří sendvič obsahující atom uranu . V pevném stavu jsou prstence zastíněny, což dodává molekule symetrii D 8h . V roztoku se kroužky otáčejí s nízkoenergetickou bariérou.
Uran-cyklooktatetraenyl lepení bylo ukázáno fotoelektronové spektroskopie být primárně v důsledku míchání uranu 6d orbitalů ligandu do pí orbitaly a proto darování elektronické náboje do uranu, s menší takové interakce zahrnující uranu ( 5f ) 2 orbitaly. Výpočty elektronické teorie souhlasí s tímto výsledkem a poukazují na to, že slabší interakce orbitálů 5f s otevřeným pláštěm s orbitaly ligandu určuje | M J |, velikost kvantového čísla momentu hybnosti podél 8násobné osy symetrie základního stavu.
Spektroskopické vlastnosti
Uranocen je paramagnetický . Jeho magnetická citlivost je v souladu s hodnotami 3 nebo 4 pro | M J |, přičemž doprovodný magnetický moment je ovlivněn spojkou spin-orbita . Jeho spektrum NMR je v souladu s | M J | hodnota 3. Výpočty elektronické teorie od nejjednodušších po nejpřesnější také dávají | M J | hodnoty 3 pro základní stav a 2 pro první excitovaný stav, což odpovídá označení symetrie dvojité skupiny E 3g a E 2g pro tyto stavy.
Zelená barva uranocénu je dána třemi silnými přechody ve viditelném spektru . Kromě zjištění vibračních frekvencí Ramanova spektra indikují přítomnost nízko položeného ( E 2g ) excitovaného elektronického stavu. Na základě výpočtů jsou viditelné přechody přiřazeny přechodům primárně 5f až 6d , což vede ke stavům E 2u a E 3u .
Analogické sloučeniny
Analogické sloučeniny ve formě M (C 8 H 8 ) 2 existují pro M = ( Nd , Tb , Pu , Pa , Np , Th a Yb ). Rozšíření zahrnují vzduchem stabilní derivát U (C 8 H 4 Ph 4 ) 2 a cykloheptatrienylové druhy [U (C 7 H 7 ) 2 ] - . Naproti tomu, bis (cyclooctatetraene) železo má velmi odlišnou strukturu, přičemž po jednom z r 6 - a r | 4 -C 8 H 8 ligandy.
Reference
Další čtení
- Prvky f , Nikolas Kaltsoyannis a Peter Scott. ISBN 0-19-850467-5
- Chemistry of the Elements , NN Greenwood a A. Earnshaw. ISBN 0-08-022057-6
- Lanthanidy a aktinidy: Organoaktinidy