Agouti -signalizační protein - Agouti-signaling protein
Agouti-signalizační protein je protein, který u lidí je kódován ASIP genu . Je zodpovědný za distribuci melaninového pigmentu u savců. Agouti interaguje s receptorem melanokortinu 1, aby určil, zda melanocyt (pigmentová buňka) produkuje phaeomelanin (červený až žlutý pigment) nebo eumelanin (hnědý až černý pigment). Tato interakce je zodpovědná za vytváření zřetelných světlých a tmavých pruhů ve vlasech zvířat, jako jsou aguti , podle nichž je gen pojmenován. U jiných druhů, jako jsou koně , je aguti signalizace zodpovědná za určení, které části těla budou červené nebo černé. Myši s agouti divokého typu budou šedé , přičemž každý vlas bude částečně žlutý a částečně černý. Ztráta funkčních mutací u myší a jiných druhů způsobuje zbarvení černé srsti, zatímco mutace způsobující expresi v celém těle u myší způsobují žlutou srst a obezitu.
Agouti-signalizační protein (ASIP) je kompetitivní antagonista s alfa-melanocyty stimulujícím hormonem (α-MSH), který se váže na proteiny receptoru melanokortinu 1 (MC1R) . Aktivace α-MSH způsobuje produkci tmavšího eumelaninu, zatímco aktivace pomocí ASIP produkuje červenější phaeomelanin. To znamená, že kde a zatímco se aguti vyjadřuje, část vlasů, které rostou, bude vycházet žlutě než černě.
Funkce
U myší kóduje gen aguti parakrinní signální molekulu, která způsobuje, že melanocyty vlasových folikulů syntetizují žlutý pigment feomelanin namísto černého nebo hnědého pigmentu eumelaninu . Pleiotropní efekty konstituční exprese myšího genu zahrnují obezitu u dospělých , zvýšenou náchylnost k nádoru a předčasnou neplodnost. Tento gen je velmi podobný myšímu genu a kóduje sekretovaný protein, který může (1) ovlivnit kvalitu pigmentace vlasů , (2) působit jako inverzní agonista hormonu stimulujícího alfa-melanocyty , (3) hrát roli v neuroendokrinním systému aspekty působení melanokortinu a (4) mají funkční roli v regulaci metabolismu lipidů v adipocytech .
U myší představuje aguti alela divokého typu (A) šedý fenotyp, nicméně mnoho variant alel bylo identifikováno pomocí genetických analýz, které vedou k široké škále fenotypů odlišných od typického šedého pláště. Nejvíce studovanými variantami alel jsou smrtící žlutá mutace ( Ay ) a životaschopná žlutá mutace (A vy ), které jsou způsobeny ektopickou expresí aguti . Tyto mutace jsou také spojeny se žlutým obézním syndromem, který je charakterizován časným nástupem obezity , hyperinzulinemie a tumorigeneze . Myší aguti genové místo se nachází na chromozomu 2 a kóduje 131 aminokyselin proteinu. Tento protein signalizuje distribuci melaninových pigmentů v epiteliálních melanocytech umístěných na bázi vlasových folikulů, přičemž exprese je citlivější na ventrálních vlasech než na dorzálních. Agouti není přímo vylučován v melanocytech, protože působí jako parakrinní faktor na buňkách dermálních papil, aby inhiboval uvolňování melanokortinu . Melanokortin působí na folikulární melanocyty a zvyšuje produkci eumelaninu , melaninového pigmentu zodpovědného za hnědé a černé vlasy. Když je aguti vyjádřeno, dominuje produkce feomelaninu , melaninového pigmentu, který produkuje žluté nebo červené vlasy.
Struktura
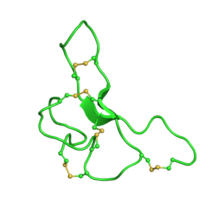
Signální peptid Agouti přijímá motiv cystinového uzlu inhibitoru . Spolu s homologním peptidem příbuzným Agouti jsou to jediné známé savčí proteiny, které přijaly tento záhyb. Peptid se skládá ze 131 aminokyselin.
Mutace
Letální žlutý mutace (A r ) byl první embryonální mutaci být charakterizován u myší, jak je homozygotní letální žluté myší (A r / A r ) umírá na počátku vývoje, v důsledku chyby v trophectoderm diferenciace. Smrtící žlutí homozygoti jsou dnes vzácní, zatímco smrtelně žlutí a životaschopní žlutí heterozygoti (A y /a a A vy /a) zůstávají běžnější. U myší divokého typu se aguti exprimuje v kůži pouze během růstu vlasů, ale tyto dominantní žluté mutace způsobují, že je exprimován i v jiných tkáních . Tato ektopická exprese z aguti genu je spojen s žluté obézní syndromu , vyznačující se tím, časný nástup obezity , hyperinzulinémie a vzniku nádorů .
Letální žlutý (A r ) mutace v důsledku upstream vypuštěním v počátečního místa aguti transkripce. Tato delece způsobí ztrátu genomové sekvence aguti , kromě promotoru a prvního nekódujícího exonu Raly , všudypřítomně exprimovaného genu u savců. Kódující exony z Agouti jsou umístěny pod kontrolou Raly promotor, iniciační všudypřítomný expresi Agouti , zvyšování produkce pheomelanin přes eumelanin a vede k vývoji žluté fenotypu.
Životaschopné žluté (A vy ) mutace je v důsledku změny v délce mRNA aguti , jako je exprimovaný gen delší než je normální délky genu Agouti. To je způsobeno inzercí retrotranspozonu jedné intracisternní částice A (IAP) proti proudu do počátečního místa transkripce aguti . Na proximálním konci genu pak neznámý promotor způsobí konstituční aktivaci aguti a jednotlivcům se projeví fenotypy konzistentní se smrtící žlutou mutací. Ačkoli mechanismus aktivace promotoru kontrolujícího životaschopnou žlutou mutaci není znám, síla barvy srsti koreluje se stupněm methylace genu , který je určen stravou matek a expozicí prostředí. Protože aguti sám inhibuje receptory melanokortinu zodpovědné za produkci eumelaninu, žlutý fenotyp se zhoršuje jak u smrtících žlutých, tak u životaschopných žlutých mutací, protože se zvyšuje exprese aguti genu. Agouti je jedinečný, protože ačkoli se jedná o recesivní alelu, heterozygoti budou vypadat žlutě, nikoli dominantní hnědá nebo černá.
Živé žluté (A vy /a) a smrtelně žluté (A y /a) heterozygoti zkrátily délku života a zvýšily riziko vzniku časného nástupu obezity, diabetes mellitus II. Typu a různých nádorů. Zvýšené riziko vzniku obezity je způsobeno dysregulací chuti k jídlu, protože aguti agonizuje protein související s aguti (AGRP), zodpovědný za stimulaci chuti k jídlu prostřednictvím hypotalamických NPY/AGRP orexigenních neuronů. Agouti také podporuje obezitu antagonizací melanocyt stimulujícího hormonu (MSH) na melanokortinovém receptoru (MC4R), protože MC4R je zodpovědný za regulaci příjmu potravy inhibicí signálů k chuti k jídlu. Zvýšení chuti k jídlu je spojeno se změnami v metabolismu živin v důsledku parakrinních účinků aguti na tukovou tkáň, zvýšení hladin jaterní lipogeneze , snížení hladin lipolýzy a zvýšení hypertrofie adipocytů. To zvyšuje tělesnou hmotnost a vede k potížím se ztrátou hmotnosti, protože metabolické dráhy se stávají neregulovanými. Hyperinzulinémie je způsobena mutacemi aguti , protože aguti protein funguje způsobem závislým na vápníku ke zvýšení sekrece inzulínu v beta buňkách pankreatu, což zvyšuje riziko inzulinové rezistence . Zvýšená tvorba tumoru je dána zvýšenou mitotickou mírou aguti , které jsou lokalizovány do epiteliálních a mezenchymálních tkání.
Methylace a dietní intervence
Správné fungování aguti vyžaduje methylaci DNA. Methylace se vyskytuje v šesti sekvencích bohatých na guanin-cytosin (GC) v 5 'dlouhé koncové repetici prvku IAP v životaschopné žluté mutaci. Metylace na genu způsobí, že gen nebude exprimován, protože způsobí vypnutí promotoru . In utero může dieta matky způsobit methylaci nebo demetylaci. Když je tato oblast nemetylovaná, dochází k ektopické expresi aguti a jsou zobrazeny žluté fenotypy, protože místo eumelaninu je exprimován phaeomelanin. Když je oblast methylována, aguti se exprimuje normálně a vyskytují se šedé a hnědé fenotypy (eumelanin). Epigenetický stav prvku IAP je určen úrovní methylace, protože jedinci vykazují širokou škálu fenotypů na základě stupně methylace DNA. Zvýšená methylace koreluje se zvýšenou expresí normálního aguti genu. Nízké hladiny methylace mohou vyvolat genový otisk, což vede k tomu, že potomci vykazují konzistentní fenotypy svým rodičům, protože ektopická exprese aguti je zděděna prostřednictvím negenomických mechanismů.
Methylace DNA je určena in utero výživou matky a expozicí prostředí. Methyl je syntetizován de novo, ale je dosažen dietou kyselinou listovou, methioninem, betainem a cholinem, protože tyto živiny vstupují do konzistentní metabolické dráhy pro methylovou syntézu. Pro syntézu methylu je zapotřebí dostatečný zinek a vitamín B12 , které působí jako kofaktory pro přenos methylových skupin.
Pokud je během raného embryonálního vývoje k dispozici neadekvátní methyl, nemůže dojít k methylaci DNA, což zvyšuje ektopickou expresi aguti a vede k prezentaci smrtících žlutých a životaschopných žlutých fenotypů, které přetrvávají až do dospělosti. To vede k rozvoji syndromu žluté obezity , který zhoršuje normální vývoj a zvyšuje náchylnost k rozvoji chronických onemocnění. Klíčovým preventivním opatřením ke snížení mimoděložní exprese agouti u potomků je zajištění mateřské stravy s vysokým obsahem metylových ekvivalentů . Intervence diety prostřednictvím methylové suplementace snižuje otisk na aguti lokusu, protože zvýšená spotřeba methylu způsobí, že se prvek IAP stane zcela methylovaným a ektopická exprese aguti se sníží. To snižuje podíl potomků, kteří mají žlutý fenotyp, a zvyšuje počet potomků, kteří se podobají agouti divokým typům myší se šedými kabáty. Dvě geneticky identické myši mohly vypadat velmi odlišně fenotypicky kvůli dietě matek, zatímco myši byly v děloze. Pokud myši mají gen aguti, mohou být vyjádřeny v důsledku toho, že matka jí typickou dietu a potomstvo by mělo žlutý kabát. Pokud by stejná matka jedla dietu bohatou na methyl doplněnou zinkem, vitamínem B12 a kyselinou listovou, potom by se aguti gen pro potomky pravděpodobně metyloval, nebyl by exprimován a místo toho by barva srsti byla hnědá. U myší je žlutá barva srsti také spojena se zdravotními problémy u myší, včetně obezity a cukrovky.
Lidský homolog
Signální protein Agouti (ASP) je lidský homolog myších aguti . Je kódován genem lidského aguti na chromozomu 20 a je to protein sestávající ze 132 aminokyselin. Je exprimován mnohem šířeji než myší aguti a nachází se v tukové tkáni, slinivce, varlatech a vaječnících, zatímco myší aguti je exprimován pouze v melanocytech. ASP má 85% podobnost s myší formou aguti . Protože mimoděložní exprese myších aguti vede k rozvoji syndromu žluté obezity , očekává se, že bude u lidí konzistentní. Žlutých obézních syndrom zvyšuje vývoj mnoha chronických onemocnění, včetně obezity, diabetes mellitus typu II a vzniku nádorů.
ASP má podobnou farmakologickou aktivaci jako myší aguti , protože receptory melanokortinu jsou inhibovány kompetitivním antagonismem. Inhibice melanokortinu pomocí ASP může být také prostřednictvím nekonkurenčních metod, což rozšiřuje jeho spektrum účinků. Funkce ASP se liší od myších aguti . ASP ovlivňuje kvalitu pigmentace vlasů, zatímco myší aguti řídí distribuci pigmentů, které určují barvu srsti. ASP má neuroendokrinní funkce konzistentní s myšími aguti , protože agonizuje prostřednictvím neuronů AgRP v hypotalamu a antagonizuje MSH na MC4R, které snižují signály sytosti. AgRP působí jako stimulátor chuti k jídlu a zvyšuje chuť k jídlu a zároveň snižuje metabolismus. Kvůli těmto mechanismům může být AgRP spojen se zvýšenou tělesnou hmotností a obezitou u lidí i myší. Nadměrná exprese AgRP byla spojena s obezitou u mužů, zatímco některé polymorfismy AgRP byly spojeny s poruchami příjmu potravy, jako je mentální anorexie . Mechanismus, který je základem hyperinzulinémie u lidí, je v souladu s myšími aguti , protože sekrece inzulínu je zvýšena prostřednictvím signalizace citlivé na vápník v pankreatických beta buňkách. Mechanismus tumorigeneze indukované ASP zůstává u lidí neznámý.
Viz také
Reference
Další čtení
- Wilczynski AM, Joseph CG, Haskell-Luevano C (září 2005). „Současné trendy ve vztazích mezi strukturou a aktivitou antagonisty melanocortinového receptoru endogenního agouti proteinu (AGRP)“. Recenze lékařského výzkumu . 25 (5): 545–56. doi : 10.1002/med.20037 . PMID 16044415 . S2CID 116767 .
- Pritchard LE, White A (říjen 2005). „Protein související s Agouti: více než antagonista receptoru melanokortinu-4?“. Peptidy . 26 (10): 1759–70. doi : 10,1016/j.peptides.2004.11.036 . PMID 15996791 . S2CID 21598037 .
- Stütz AM, CD Morrison, Argyropoulos G (říjen 2005). „Protein související s aguti a jeho role v energetické homeostáze“. Peptidy . 26 (10): 1771–81. doi : 10,1016/j.peptides.2004.12.024 . PMID 15961186 . S2CID 9749408 .
- Millhauser GL, McNulty JC, Jackson PJ, Thompson DA, Barsh GS, Gantz I (červen 2003). „Smyčky a odkazy: strukturální pohledy na pozoruhodnou funkci proteinu souvisejícího s aguti“ (PDF) . Annals of the New York Academy of Sciences . 994 (1): 27–35. Bibcode : 2003 NYASA.994 ... 27 mil . doi : 10.1111/j.1749-6632.2003.tb03159.x . hdl : 2027,42/75746 . PMID 12851295 . S2CID 46576434 .
- Barsh GS, He L, Gunn TM (2002). „Genetické a biochemické studie systému Agouti-atraktin“. Journal of Receptor and Signal Transduction Research . 22 (1–4): 63–77. doi : 10,1081/RRS-120014588 . PMID 12503608 . S2CID 25089838 .
- Millington GW (květen 2006). „Proopiomelanocortin (POMC): kožní role jejích melanokortinových produktů a receptorů“. Klinická a experimentální dermatologie . 31 (3): 407–12. doi : 10.1111/j.1365-2230.2006.02128.x . PMID 16681590 . S2CID 25213876 .
externí odkazy
- agouti+protein v Americké národní knihovně lékařských lékařských oborových nadpisů (MeSH)
Tento článek včlení text z Národní lékařské knihovny Spojených států , který je veřejně dostupný .




