Dusičnan alkalického kovu - Alkali metal nitrate
Dusičnany alkalických kovů jsou chemické sloučeniny sestávající z alkalických kovů ( lithium , sodík , draslík , rubidium a cesium ) a dusičnanového iontu. Pouze dva mají hlavní komerční hodnotu, sodné a draselné soli. Jsou to bílé, ve vodě rozpustné soli s bodem tání v rozmezí od 255 ° C ( LiNO
3) až 414 ° C ( CsNO
3) pouze při relativně úzkém rozpětí 159 ° C.
| Sloučenina | Chemický vzorec | Molární hmotnost | Bod tání | Struktura |
|---|---|---|---|---|
| Dusičnan lithný | LiNO 3 | 68,946 g / mol | 255 ° C (491 ° F; 528 K) |

|
| Dusičnan sodný | NaNO 3 | 84,9947 g / mol | 308 ° C (586 ° F; 581 ° K) |
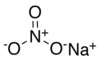
|
| Dusičnan draselný | KNO 3 | 101,1032 g / mol | 334 ° C (633 ° F; 607 K) |

|
| Dusičnan rubidný | RbNO 3 | 147,473 g / mol | 310 ° C (590 ° F; 583 K) |

|
| Dusičnan cesný | CsNO 3 | 194,91 g / mol | 414 ° C (777 ° F; 687 K) |

|
Teplota tání z dusičnanů alkalických kovů, má tendenci se zvyšovat od 255 ° C do 414 ° C (s anomálie pro rubidium jsou správně vyrovnány v řadě) jako atomové hmotnosti a iontový poloměr (nahý kationtu ) z alkalických kovů se zvyšuje , jít dolů ve sloupci. Podobně, ale není zde uvedeno v tabulce, se rozpustnost těchto solí ve vodě také snižuje s atomovou hmotou kovu.
Aplikace
Jako hnojiva se běžně používají dusičnany sodné a draselné . Jelikož jsou také silnými oxidačními činidly , vstupují do pyrotechnických směsí a do výroby výbušnin .
Menší použití je pro barvení světla vyzařovaného zábavní pyrotechnikou :
- dusičnan lithný vytváří červenou barvu,
- dusičnan sodný vytváří žlutou / oranžovou barvu,
- dusičnan draselný a dusičnan rubidný produkují fialové barvy,
- dusičnan česný produkuje indigovou barvu.
V obecné rovině je vyzařované barva postupně změní z červené na fialové ve viditelném spektru světla při jízdě v koloně z alkalických kovů, v periodické tabulce, z Mendělejev . Odpovídá to snížení vlnové délky světla emitovaného během kroku odbuzení elektronů v atomech přivedených při vysoké teplotě. Fotony emitované cesiem jsou energetičtější než fotony lithia .
Viz také
Reference

