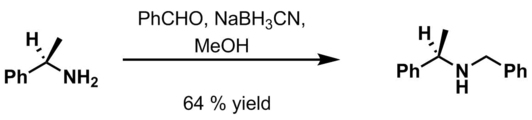Benzylová skupina - Benzyl group
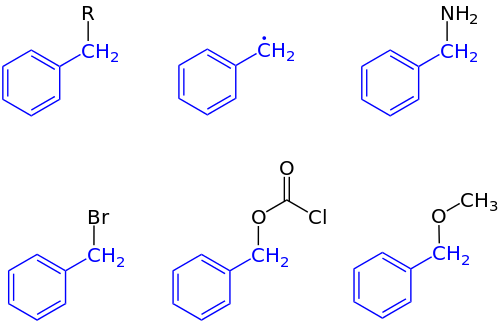
V organické chemii , benzylová skupina je substituent nebo molekulární fragment mající strukturu C 6 H 5 CH 2 -. Benzyl vybaven benzenový kruh, připojený ke CH 2 skupinu.
Nomenklatura
Podle názvosloví IUPAC předpona benzyl týká C 6 H 5, CH 2 substituent, jako je například benzylchlorid a benzylbenzoát . Benzyl je nelze zaměňovat s fenylovou skupinou se vzorcem C 6 H 5 . Termín benzyl se používá k popisu polohy prvního uhlíku navázaného na benzen nebo jiný aromatický kruh. Například, (C 6 H 5 ), (CH 3 ) 2 C + se označuje jako "benzylového" karbokationtu. Benzylový volný radikál má vzorec C.
6H
5CH•
2. Benzylový kation nebo fenylkarbeniový iont je karbokationt vzorce C.
6H
5CH+
2; benzyl aniont nebo fenylmethanidový ion je karbanion vzorce C
6H
5CH-
2. Žádný z těchto druhů nemůže být vytvořen ve významném množství ve fázi roztoku za normálních podmínek, ale jsou užitečnými referenty pro diskusi o reakčních mechanismech a mohou existovat jako reaktivní meziprodukty.
Zkratky
Zkratka „Bn“ označuje benzyl. Například benzylalkohol může být reprezentován jako BnOH. Tato zkratka je nelze zaměňovat s „Bz“, což je zkratka pro benzoylovou skupinu C 6 H 5 C (O) -, nebo je fenylová skupina, C 6 H 5 , zkráceně „Ph“. Matoucí je, že ve staré literatuře se „Bz“ používalo také pro benzyl.
Reaktivita benzylových center
Zvýšená reaktivita benzylových pozic je přičítána nízké disociační energii vazby pro benzylové C-H vazby. Konkrétně se jedná o vazbu C 6 H 5 CH 2 -H, je asi 10 až 15% méně než jiné druhy CH vazeb. Sousední aromatický kruh stabilizuje benzylové radikály. Níže uvedená data srovnávají benzylovou vazbu C-H se souvisejícími silami vazby C-H.
| Pouto | Pouto | Energie disociace vazeb | Komentář | |
|---|---|---|---|---|
| (kcal / mol) | (kJ / mol) | |||
| C 6 H 5 CH 2 −H | benzylová vazba C-H | 90 | 377 | podobné allylovým C-H vazbám takové vazby vykazují zvýšenou reaktivitu |
| H 3 C - H | methylová vazba C-H | 105 | 439 | jedna z nejsilnějších alifatických C-H vazeb |
| C 2 H 5 −H | ethylová vazba C-H | 101 | 423 | o něco slabší než H 3 C − H |
| C 6 H 5 −H | fenylová vazba C-H | 113 | 473 | srovnatelné s vinylovým radikálem, vzácné |
| CH 2 = CHCH 2 H | allylová vazba C – H | 89 | 372 | podobně jako benzyl CH |
| (C 6 H 4 ) 2 CH-H | fluorenyl C – H vazba | 80 | aktivovanější oproti difenylmethylu ( pKa = 22,6) | |
| (C 6 H 5 ) 2 CH-H | difenylmethyl C – H vazba | 82 | „dvakrát benzyl“ ( pKa = 32,2) | |
| (C 6 H 5 ) 3 C − H | trityl C – H vazba | 81 | 339 | "trojnásobně benzyl" |
Slabost vazby C-H odráží stabilitu benzylového radikálu. Ze souvisejících důvodů vykazují benzylové substituenty zvýšenou reaktivitu, například při oxidaci , halogenaci volných radikálů nebo hydrogenolýze . Jako praktický příklad v přítomnosti vhodných katalyzátorů oxiduje p - xylen výhradně v benzylových pozicích za vzniku kyseliny tereftalové :
- CH 3 C 6 H 4 CH 3 + 3 O 2 → HO 2 CC 6 H 4 CO 2 H + 2 H 2 O.
Touto metodou se ročně vyrobí miliony tun kyseliny tereftalové.
Funkcionalizace v benzylové poloze
V několika případech k těmto benzylovým transformacím dochází za podmínek vhodných pro laboratorní syntézu. Wohl-Ziegler reakce se brominate benzylového C-H vazbu: (ArCHR 2 → ArCBrR 2 ). Jakékoliv jiné než terciární benzylová alkylová skupina se oxiduje na karboxylovou skupinu působením vodného roztoku manganistanu draselného (KMnO 4 ), nebo koncentrované kyseliny dusičné (HNO 3 ): (ArCHR 2 → ArCOOH). Konečně, komplex oxidu chromového a 3,5-dimethylpyrazol (CrO 3 -dmpyz) se selektivně oxidují benzylového methylenovou skupinu na karbonyl: (arch 2 R → oblouku (O) R). Kyselina 2-jodoxybenzoová v DMSO funguje podobně.
Jako chránící skupina
Benzylové skupiny se občas používají jako chránící skupiny v organické syntéze. Jejich instalace a zejména jejich demontáž vyžadují relativně drsné podmínky, takže benzyl není obvykle chráněn.
Ochrana proti alkoholu
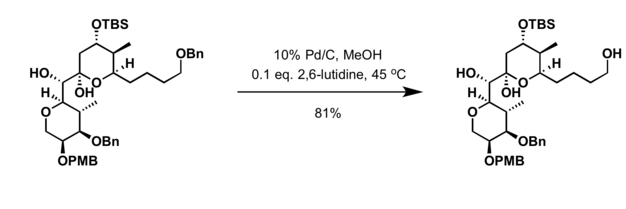
Benzyl se běžně používá v organické syntéze jako silná chránící skupina pro alkoholy a karboxylové kyseliny .
- Léčba alkoholu se silnou bází, jako je práškový hydroxid draselný nebo hydrid sodný a benzylhalogenid ( BnCl nebo BnBr )
- Monobenzylation z diolů může být dosaženo použitím Ag 2 O v dimethylformamidu (DMF), za teploty místnosti až zvýšené teploty
- Primární alkoholy lze selektivně benzylovat v přítomnosti fenolových funkčních skupin za použití Cu (acac) 2
Metody deprotekce
Benzylethery lze odstranit za redukčních podmínek , oxidačních podmínek a za použití Lewisových kyselin .
- Odstraněno pomocí hydrogenolýzy
- Jeden elektron proces s Na / NH 3 nebo Li / NH 3
- Skupiny chránící benzyl lze odstranit pomocí široké škály oxidačních činidel, včetně:
- CrO 3 / kyselina octová při teplotě okolí
- Ozón
- N- bromsukcinimid (NBS)
- N- jodosukcinimid (NIS)
- Trimethylsilyljodid (Me 3 SiI) v dichlormethanu při teplotě okolí (selektivity lze dosáhnout za určitých podmínek)
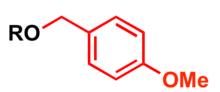
V P -methoxybenzyl chránící skupina
p -Methoxybenzyl ( PMB ) se používá jako chránící skupina pro alkoholy v organické syntéze ( 4-methoxybenzylthiol se používá k ochraně thiolů).
- Silná báze, jako je práškový hydroxid draselný nebo hydrid sodný a p- methoxybenzylhalogenid (chlorid nebo bromid)
- 4-methoxybenzyl-2,2,2-trichloracetimidát lze použít k instalaci skupiny PMB za přítomnosti:
- Skandium (III) triflát (Sc (OTf) 3 ) v toluenu při 0 ° C
-
Kyselina trifluormethansulfonová (TfOH) v dichlormethanu při 0 ° C
Metody deprotekce
- 2,3-Dichlor-5,6- dikyano - p- benzochinon (DDQ)
- Podmínky pro odstranění chránící skupiny z benzylové skupiny jsou použitelné pro odštěpení chránící skupiny PMB
Ochrana proti aminům
Benzylová skupina se příležitostně používá jako chránící skupina pro aminy v organické syntéze . Existují i jiné metody.
- Vodný roztok uhličitanu draselného a benzylhalogenid ( BnCl , BnBr ) v methanolu
-
Benzaldehyd , 6 M kyseliny chlorovodíkové a NaBH 3 CN v methanolu
Metody deprotekce
- Hydrogenace v přítomnosti palladiového katalyzátoru
Viz také
Reference
externí odkazy
-
 Chemický portál
Chemický portál
-
 Citace týkající se benzylové skupiny na Wikiquote
Citace týkající se benzylové skupiny na Wikiquote