Tetrachloroaluminate - Tetrachloroaluminate

|
|
| Jména | |
|---|---|
|
Název IUPAC
Tetrachloroaluminate (1–)
|
|
|
Systematický název IUPAC
Tetrachloroaluminate (1-) |
|
Ostatní jména
|
|
| Identifikátory | |
|
3D model ( JSmol )
|
|
| ChEBI | |
| ChemSpider | |
| 2297 | |
|
PubChem CID
|
|
|
|
|
|
| Vlastnosti | |
| AlCl 4 - | |
| Molární hmotnost | 168,88 g · mol -1 |
| Struktura | |
| T d | |
| Čtyřboká | |
| Hybridizace | sp 3 |
|
Pokud není uvedeno jinak, jsou uvedeny údaje o materiálech v jejich standardním stavu (při 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Reference Infoboxu | |
Tetrachloraluminátu [AlCl 4 ] - je anion vytvořena z hliníku a chlóru . Anion má čtyřboký tvar, podobný tetrachlormethanu, kde je uhlík nahrazen hliníkem. Některé tetrachlorhlinitany jsou rozpustné v organických rozpouštědlech a vytvářejí iontový nevodný roztok, díky čemuž jsou vhodné jako součást elektrolytů pro baterie. Například lithium tetrachloroaluminate se používá v některých lithiových bateriích .
Formace
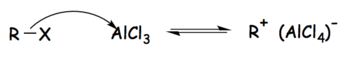
Tetrachloroaluminátové ionty vznikají jako meziprodukty při Friedel-Craftsových reakcích, když se jako katalyzátor použije chlorid hlinitý . V případě Friedel - Craftsovy alkylace lze reakci rozdělit do tří kroků následujícím způsobem:
Krok 1: Alkylhalogenid reaguje se silnou Lewisovou kyselinou za vzniku aktivovaného elektrofilu složeného z tetrachloraluminátového iontu a alkylové skupiny.
Krok 2: Aromatický kruh ( v tomto případě benzen ) reaguje s aktivovaným elektrofilem za vzniku alkylbenzeniové karbokationtu.
Krok 3: Alkylbenzeniumkarbokace reaguje s tetrachloroaluminátovým anionem, regeneruje aromatický kruh a Lewisovu kyselinu a vytváří kyselinu chlorovodíkovou (HCl).
Podobný mechanismus se vyskytuje i při Friedel - Craftsově acylaci.