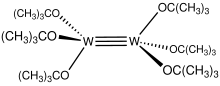
Hexa (terc -butoxy) ditungsten (III) - Hexa(tert-butoxy)ditungsten(III)
|
|
| Identifikátory | |
|---|---|
|
3D model ( JSmol )
|
|
| ChemSpider | |
|
PubChem CID
|
|
|
|
|
|
| Vlastnosti | |
| C 24 H 54 O 6 W 2 | |
| Molární hmotnost | 806,37 g · mol −1 |
| Vzhled | červená pevná látka |
| Hustota | 1,651 g / cm 3 |
|
Pokud není uvedeno jinak, jsou údaje uvedeny pro materiály ve standardním stavu (při 25 ° C [77 ° F], 100 kPa). |
|
| Reference na infobox | |
Hexa ( terc -butoxy) ditungsten (III) je koordinační komplex wolframu (III). Je to jeden z homoleptických alkoxidů wolframu. Je to červená, na vzduch citlivá pevná látka a přitahuje akademickou pozornost jako předchůdce mnoha derivátů organického wolframu . Je to příklad nábojově neutrálního komplexu s vazbou W≡W, který vzniká spojením dvojice kovových center d 3 . To přitahovalo zvláštní pozornost pro jeho reakce s alkyny, což vedlo k alkynové metateze .
Může být připraven reakcí metateze soli z thf komplexu ditungsten heptachloridu:
- NaW 2 Cl 7 (THF) 5 + 6 NaOBu-t → W 2 (OBu-t) 6 + 7 NaCl + 5 THF
Původně byl připraven alkoholýzou amidu W 2 (NMe 2 ) 6 .
Komplex a jeho analog dimolybdenu mají střídavou , ethanu podobnou konformaci. Vzdálenost MM je 233 hodin. Komplex je slabá Lewisova kyselina, tvořící adukty například se dvěma pyridinovými ligandy.
Viz také
Reference
- ^ Listemann, Mark L .; Schrock, Richard R. (1985). „Multiple kov uhlík. 35. Obecný trasy k tri -terc -Butoxytungsten Alkylidyn komplexy. Štěpení acetylenů podle Ditungsten hexa- terc -butoxid“. Organokovové . 4 : 74–83. doi : 10,1021/om00120a014 .
- ^ Broderick, Erin M .; Browne, Samuel C .; Johnson, Marc JA (2014). Dimolybden a Ditungsten Hexa (Alkoxidy) . Anorganické syntézy. 36 . str. 95–102. doi : 10,1002/9781118744994.ch18 . ISBN 9781118744994.
- ^ Chisholm, MH; Extine, M. (1975). „Nové metaloorganické sloučeniny wolframu (III)“. Journal of the American Chemical Society . 97 (19): 5625–5627. doi : 10,1021/ja00852a074 .
- ^ Chisholm, Malcolm H .; Gallucci, Judith C .; Hollandsworth, Carl B. (2006). "Krystalová a molekulární struktura W 2 (OBut) 6 a výpočty elektronické struktury na různých konformerech W 2 (OMe) 6 ". Mnohostěn . 25 (4): 827–833. doi : 10.1016/j.poly.2005.07.010 .
- ^ Budzichowski, Theodore A .; Chisholm, MH; Folting, Kristen; Huffman, John C .; Streib, William E .; Tiedtke, Darin B. (1998). "Adukty pyridinu, isokyanidu, karbodiimidu a allenu hexakis (Trifluormethyl t-botoxy) ditungstenu. Srovnání vazby ligandu na W 2 (Ot-Bu) 6 a W 2 (OCMe 2 CF 3 ) 6 ". Mnohostěn . 17 (5–6): 857–867. doi : 10,1016/S0277-5387 (97) 00290-8 .
