Methyllithium - Methyllithium

|
|
| Jména | |
|---|---|
|
Název IUPAC
Methyllithium
|
|
| Ostatní jména
Methanid lithný
|
|
| Identifikátory | |
|
3D model ( JSmol )
|
|
| 3587162 | |
| ČEBI | |
| ChemSpider | |
| Informační karta ECHA |
100,011,843 |
| Číslo ES | |
| 288 | |
|
PubChem CID
|
|
|
CompTox Dashboard ( EPA )
|
|
|
|
|
|
| Vlastnosti | |
| C H 3 Li | |
| Molární hmotnost | 21,98 g · mol −1 |
| Reaguje | |
| Nebezpečí | |
| Hlavní nebezpečí | pyroforický |
| NFPA 704 (ohnivý diamant) | |
|
Pokud není uvedeno jinak, jsou údaje uvedeny pro materiály ve standardním stavu (při 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Reference na infobox | |
Methyllithium je nejjednodušší organolithné činidlo s empirickým vzorcem CH 3 Li. Tato organokovová sloučenina s blokem s přijímá oligomerní strukturu jak v roztoku, tak v pevném stavu. Tato vysoce reaktivní sloučenina, vždy používaná v roztoku s etherem jako rozpouštědlem, je činidlem v organické syntéze i v organokovové chemii . Operace zahrnující methyllithium vyžadují bezvodé podmínky, protože sloučenina je vysoce reaktivní vůči vodě . Kyslík a oxid uhličitý jsou také nekompatibilní s MeLi. Methyllithium se obvykle nepřipravuje, ale kupuje se jako roztok v různých etherech.
Syntéza
Při přímé syntéze se na methylbromid působí suspenzí lithia v diethyletheru .
- 2 Li + MeBr → LiMe + LiBr
Bromid lithný tvoří komplex s methyllithiem. Většina komerčně dostupných methyllithia se skládá z tohoto komplexu. Methyllithium "bez halogenidů" se připravuje z methylchloridu. Chlorid lithný se vysráží z diethyletheru, protože s methyllithiem nevytváří silný komplex. Filtrát se skládá z poměrně čistého methyllithia.
Reaktivita
Methyllithium je díky zásadě částečného záporného náboje na uhlíku silně zásadité a vysoce nukleofilní, a proto je zvláště reaktivní vůči akceptorům elektronů a dárcům protonů. Na rozdíl od n-BuLi reaguje MeLi s THF při pokojové teplotě jen velmi pomalu a roztoky v etheru jsou neomezeně stabilní. Voda a alkoholy reagují prudce. Většina reakcí zahrnujících methyllithium probíhá pod teplotou místnosti. Ačkoli MeLi lze použít pro deprotonaci, běžně se používá n -butyllithium, protože je levnější a reaktivnější.
Methyllithium se používá hlavně jako syntetický ekvivalent methyl aniontového synthonu . Ketony například reagují za vzniku terciárních alkoholů ve dvou krocích:
- Ph 2 CO + MeLi → Ph 2 C (Me) OLi
- Ph 2 C (Me) OLi + H + → Ph 2 C (Me) OH + Li +
Nekovové halogenidy se převádějí na methyllithium na methylové sloučeniny:
- PCl 3 + 3 MeLi → PMe 3 + 3 LiCl
Takové reakce častěji využívají Grignardova činidla methylmagnesiumhalogenidy, které jsou často stejně účinné a méně nákladné nebo snadněji připravitelné in situ.
Reaguje také s oxidem uhličitým za vzniku octanu lithného :
- CH 3 Li + CO 2 → CH 3 CO 2 - Li +
Methylové sloučeniny přechodných kovů lze připravit reakcí MeLi s halogenidy kovů. Obzvláště důležité jsou tvorba organických měděných sloučenin ( Gilmanova činidla ), z nichž nejužitečnější je lithium dimethylcuprát . Toto činidlo je široce používáno pro nukleofilní substituce epoxidů , alkylhalogenidů a alkylsulfonátů , jakož i pro přidání konjugátu k a, P-nenasyceným karbonylovým sloučeninám methylovým aniontem. Bylo připraveno mnoho dalších methylových sloučenin přechodných kovů.
- ZrCl 4 + 6 MeLi → Li 2 ZrMe 6 + 4 LiCl
Struktura
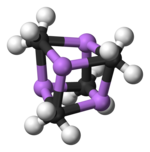
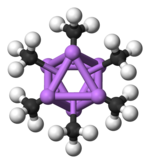
Dvě struktury byly ověřeny monokrystalu rentgenovou krystalografií , jakož i 6 Li, 7 Li, a 13 C NMR spektroskopií . Tetramerická struktura je zkreslený kubánský klastr s atomy uhlíku a lithia v alternativních rozích. Vzdálenosti Li-Li jsou 2,68 Á, téměř totožné s vazbou Li-Li v plynném dilithiu . Vzdálenosti C-Li jsou 2,31 Å. Uhlík je vázán na tři atomy vodíku a tři atomy Li. Nestálost (MeLi) 4 a jeho nerozpustnost v alkanech vyplývá ze skutečnosti, že klastry interagují prostřednictvím dalších meziklastrových agostických interakcí . Naproti tomu objemnější klastr (terciární-butylLi) 4 , kde jsou interakce mezi klastry vyloučeny sterickými efekty, je těkavý a rozpustný v alkanech.
Kód barvy: Li- fialová C- černá H- bílá
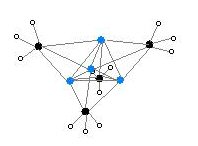
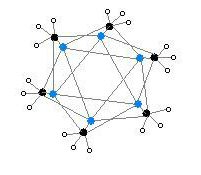
Hexamerická forma obsahuje šestihranné hranoly s atomy Li a C opět ve střídavých rozích.
Kód barvy: Li- fialová C- černá H- bílá
Stupeň agregace, "n" pro (MeLi) n , závisí na rozpouštědle a přítomnosti přísad (jako je bromid lithný). Uhlovodíková rozpouštědla, jako je benzen, podporují tvorbu hexameru, zatímco etherová rozpouštědla upřednostňují tetramer.
Lepení
Tyto shluky jsou považovány za „elektronově deficientní“, to znamená, že nedodržují oktetové pravidlo, protože molekulám na rozdíl od většiny organických sloučenin chybí dostatek elektronů, které by kolem každého atomu uhlíku vytvořily čtyři 2-centrované, 2 elektronové vazby . Hexamer je sloučenina 30 elektronů (30 valenčních elektronů.) Pokud jeden přidělí 18 elektronů pro silné vazby CH, zůstane 12 elektronů pro vazbu Li-C a Li-Li. Existuje šest elektronů pro šest vazeb kov-kov a jeden elektron na interakci methyl-η 3 lithia.
Síla vazby C-Li byla odhadnuta na přibližně 57 kcal /mol z IR spektroskopických měření.