Jodid thalia (I) - Thallium(I) iodide
|
|
| Jména | |
|---|---|
| Ostatní jména
Thallium monoiodide
Thallous jodide |
|
| Identifikátory | |
|
3D model ( JSmol )
|
|
| ChemSpider | |
| Informační karta ECHA |
100,029,272 |
|
PubChem CID
|
|
| UNII | |
|
Řídicí panel CompTox ( EPA )
|
|
|
|
|
|
| Vlastnosti | |
| TlI | |
| Molární hmotnost | 331,287 g / mol |
| Vzhled | žluté krystaly |
| Hustota | 7,1 g / cm 3 |
| Bod tání | 441,7 ° C (827,1 ° F; 714,8 K) |
| Bod varu | 824 ° C (1515 ° F; 1097 K) |
| 0,085 g / l (25 ° C) | |
| Rozpustnost | nerozpustný v alkoholu |
| −82,2 · 10 −6 cm 3 / mol | |
| Nebezpečí | |
|
Klasifikace EU (DSD) (zastaralé)
|
Vysoce toxický ( T + ) Nebezpečný pro životní prostředí ( N ) |
| R-věty (zastaralé) | R26 / 28 , R33 , R51 / 53 |
| S-věty (zastaralé) | (S1 / 2) , S13 , S28 , S45 , S61 |
| Bod vzplanutí | Nehořlavé |
| Související sloučeniny | |
|
Jiné anionty
|
Thallium (I) fluorid Thallium (I) chlorid Thallium (I) bromid |
|
Jiné kationty
|
Jodid galia (I) Jodid indný (I) |
|
Související sloučeniny
|
Jodid rtuťnatý Olovo (II) jodid |
|
Není-li uvedeno jinak, jsou uvedeny údaje o materiálech v jejich standardním stavu (při 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Reference Infoboxu | |
Jodid thalium (I) je chemická sloučenina vzorce TlI . To je neobvyklé v tom, že jedním z mála ve vodě nerozpustných kovových jodidů , spolu s AGI , Cul , SNI 2 , SNI 4 , PBI 2 a HGI 2 .
Chemie
TlI může být vytvořen ve vodném roztoku metodou syntézy jakékoli rozpustné soli thalia s jodidovým iontem. Rovněž se tvoří jako vedlejší produkt při jodaci fenolů podporovaných thaliem octanem thalium.
Pokusy oxidovat TLI na thalium (III) jodidu selhání, protože oxidace vytváří thalia (I), jodid , Tl + I 3 - .
Fyzikální vlastnosti
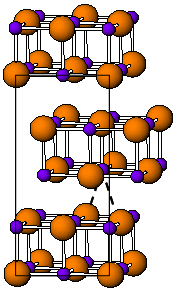
Forma Tl pokojové teploty je žlutá a má ortorombickou strukturu, kterou lze považovat za zkreslenou strukturu NaCl. Předpokládá se, že zkreslená struktura je způsobena příznivými interakcemi thallium-thallium, nejbližší vzdálenost Tl-Tl je 383 pm. Při teplotě 175 ° C se žlutá forma transformuje na červenou formu CsCl . Tento fázový přechod je doprovázen asi dvěma řády skoku elektrické vodivosti. Strukturu CsI lze stabilizovat až na teplotu místnosti dopováním TlI jinými halogenidy, jako jsou RbI, CsI, KI, AgI, TlBr a TlCl. Přítomnost nečistot tedy může být zodpovědná za koexistenci kubické a ortorombické fáze TlI za podmínek prostředí. Při vysokém tlaku 160 kbar se TlI stává kovovým vodičem. Nanometrové tenké filmy TlI pěstované na substrátech LiF, NaCl nebo KBr vykazují kubickou skalní strukturu.
Aplikace
Jodid thalia (I) se přidává k rtuťovým obloukovým lampám, aby se zlepšil jejich výkon. Produkované světlo je hlavně v modrozelené části spektra viditelného světla nejméně absorbované vodou, takže se používá pro podvodní osvětlení. Jodid thalia (I) se také používá ve stopových množstvích s NaI nebo CsI k výrobě scintilátorů používaných v detektorech záření.
Přirozený výskyt
Přírodní jodid thalia (I) byl nalezen teprve nedávno, jako ortorombický polymorf zvaný nataliyamalikit. Je fumarolického původu.
Bezpečnost
Stejně jako všechny sloučeniny thalia je jodid thalnatý vysoce toxický.
Reference
Citované zdroje
- Haynes, William M., ed. (2011). CRC Handbook of Chemistry and Physics (92. vydání). Boca Raton, FL: CRC Press . ISBN 1439855110 .
