Sloučenina vzácného plynu - Noble gas compound
Sloučeniny vzácných plynů jsou chemické sloučeniny, které zahrnují prvek z vzácných plynů , skupina 18 periodické tabulky . Ačkoli jsou vzácné plyny obecně nereaktivními prvky, bylo pozorováno mnoho takových sloučenin, zejména pokud jde o prvek xenon. Z hlediska chemie lze vzácné plyny rozdělit do dvou skupin: relativně reaktivní krypton (ionizační energie 14,0 eV), xenon (12,1 eV) a radon (10,7 eV) na jedné straně a velmi nereaktivní argon (15,8 eV), neon (21,6 eV) a helium (24,6 eV) na druhé straně. V souladu s touto klasifikací tvoří Kr, Xe a Rn sloučeniny, které lze izolovat hromadně při nebo blízko standardní teploty a tlaku (alespoň v zásadě pro vysoce radioaktivní radon), zatímco u He, Ne, Ar bylo pozorováno, že tvoří skutečnou chemické vazby pomocí spektroskopických technik, ale pouze při zmrazení do matrice vzácného plynu při teplotách 40 K nebo nižších, v nadzvukových proudech vzácného plynu nebo při extrémně vysokých tlacích s kovy.
Těžší vzácné plyny mají více elektronových obalů než lehčí. Vnější elektrony tedy podléhají stínícímu účinku z vnitřních elektronů, který je činí snadněji ionizovanými , protože jsou méně silně přitahovány k kladně nabitému jádru . To má za následek ionizační energii dostatečně nízkou na to, aby se vytvořily stabilní sloučeniny s nejvíce elektronegativními prvky , fluorem a kyslíkem, a dokonce za méně elektronegativních prvků, jako je dusík a uhlík, za určitých okolností.
Historie a pozadí
Když byla rodina ušlechtilých plynů poprvé identifikována na konci devatenáctého století, u žádného z nich nebylo pozorováno, že by vytvářelo nějaké sloučeniny, a původně se věřilo, že jsou to všechny inertní plyny (jak byly tehdy známé), které nemohou tvořit sloučeniny. S rozvojem atomové teorie na počátku dvacátého století, jejich inertnost byla připisována plné valence skořápky z elektronů , který je činí velmi chemicky stabilní a nereaktivní. Všechny vzácné plyny mají plně ů a p vnější elektronové vrstvy (kromě helia , která nemá p podúrovně), a proto netvoří chemické sloučeniny snadno. Jejich vysoká ionizační energie a téměř nulová elektronová afinita vysvětlují jejich nereaktivitu.
V roce 1933 Linus Pauling předpovídal, že těžší ušlechtilé plyny budou schopné tvořit sloučeniny s fluorem a kyslíkem . Konkrétně předpovídal existenci hexafluoridu kryptonu ( Kr F 6 ) a hexenfluoridu xenonu ( Xe F 6 ), spekuloval, že XeF 8 může existovat jako nestabilní sloučenina, a naznačil, že kyselina xenová bude tvořit perxenátové soli. Tyto předpovědi se ukázaly být docela přesné, i když následné předpovědi pro XeF 8 naznačovaly, že to bude nejen termodynamicky nestabilní, ale také kineticky nestabilní . Od roku 2013 nebyl XeF 8 vyroben, přestože aniont oktafluoroxenátu (VI) ( XeF2-
8) bylo pozorováno.
V roce 1960 ještě nebyla syntetizována žádná sloučenina s kovalentně vázaným atomem vzácného plynu. První publikovanou zprávou v červnu 1962 o sloučenině ušlechtilého plynu byl Neil Bartlett , který si všiml, že vysoce oxidující sloučenina hexafluorid platiny ionizovaný O 2 na O+
2. Jako ionizační energie O 2 na O+
2(1165 kJ mol −1 ) se téměř rovná ionizační energii Xe až Xe + (1170 kJ mol −1 ), zkusil reakci Xe s PtF 6 . To poskytlo krystalický produkt, xenon hexafluoroplatinát , jehož vzorec byl navržen jako Xe+
[PtF
6]-
. Později bylo prokázáno, že sloučenina je ve skutečnosti mnohem složitější, obsahující jak XeFPtF 5 a XeFPt 2 F 11 . Nicméně to byla první skutečná směs jakéhokoli ušlechtilého plynu.
První binární sloučeniny vzácného plynu byly popsány později v roce 1962. Bartlett syntetizoval xenon tetrafluorid (XeF 4 ) vystavením směsi xenonu a fluoru vysoké teplotě. Rudolf Hoppe mimo jiné syntetizoval xenon difluorid (XeF 2 ) reakcí prvků.
Po první úspěšné syntéze xenonových sloučenin byla provedena syntéza krypton-difluoridu ( KrF
2) byl zaznamenán v roce 1963.
Pravé sloučeniny vzácného plynu
V této části jsou neradioaktivní vzácné plyny zvažovány v sestupném pořadí podle atomové hmotnosti , což obecně odráží prioritu jejich objevu a šíři dostupných informací o těchto sloučeninách. Radioaktivní prvky radon a oganesson jsou těžší studovatelné a jsou zvažovány na konci sekce.
Xenonové sloučeniny
Po počátečních studiích 1962 na XeF 4 a XeF 2 zahrnují xenonové sloučeniny, které byly syntetizovány, další fluoridy ( XeF 6 ), oxyfluoridy (XeOF 2 , XeOF 4 , XeO 2 F 2 , XeO 3 F 2 , XeO 2 F 4 ) a oxidy ( XeO
2, XeO 3 a XeO 4 ). Xenonfluoridy reagují s několika dalšími fluoridy za vzniku fluoroxenátů, jako je oktafluoroxenát sodný ( Na+
2XeF2-
8) a fluoroxenoniové soli, jako je trifluoroxenonium hexafluoroantimonát ( XeF+
3SbF-
6).
Pokud jde o jiné halogenidové reaktivity, s krátkou životností excimers vzácných plynů halogenidů , jako je XeCl 2 nebo XeCl se připraví in situ, a používají se ve funkci excimerový laser .
V poslední době, xenon bylo prokázáno, že vyrábět širokou škálu sloučenin typu Xeo n X 2 , kde n je 1,2 nebo 3, a X je jakýkoliv elektronegativní skupina, jako je skupina CF 3 , C (SO 2 CF 3 ) 3 , N (SO 2 F) 2 , N (SO 2 CF 3 ) 2 , OTeF 5 , O (IO 2 F 2 ), atd .; řada sloučenin je působivá, obdobná jako u sousedního prvku jódu , narůstá na tisíce a zahrnuje vazby mezi xenonem a kyslíkem, dusíkem, uhlíkem, bórem a dokonce i zlatem, stejně jako kyselina perxenová, několik halogenidů a komplexní ionty .
Sloučenina Xe 2 + Sb 4 F 21 - obsahuje vazbu Xe – Xe, což je nejdelší známá vazba prvek-prvek (308,71 pm = 3,0871 Å ). Uvádí se, že krátkodobé excimery Xe 2 existují jako součást funkce excimerových laserů .
Kryptonové sloučeniny
Kryptonový plyn reaguje s plynným fluorem za extrémních podmínek nutí, tvoří KrF 2 podle následující rovnice:
- Kr + F 2 → KrF 2
KrF 2 reaguje se silnými Lewisovými kyselinami za vzniku solí KrF + a Kr
2F+
3 kationty . Příprava KrF
4 hlášeno Grosseem v roce 1963 pomocí Claasenovy metody, se následně ukázalo jako mylná identifikace.
Byly také popsány kryptonové sloučeniny s jinými vazbami než Kr-F (sloučeniny s atomy jinými než fluor ). KrF
2reaguje s B (OTeF
5)
3za vzniku nestabilní sloučeniny Kr (OTeF
5)
2, s vazbou krypton- kyslík . V kationtu se nachází vazba krypton- dusík [HC≡N – Kr – F]+
, vyrobený reakcí KrF
2 s [HC≡NH]+
[AsF-
6] pod -50 ° C.
Sloučeniny argonu
Objev HArF byl oznámen v roce 2000. Sloučenina může existovat v nízkoteplotních argonových maticích pro experimentální studie a byla také studována výpočetně . Argon hydridový ion ArH+
byl získán v 70. letech. Tento molekulární iont byl také identifikován v Krabí mlhovině na základě frekvence jeho světelných emisí.
Existuje možnost, že by se mohla připravit pevná sůl ArF + se SbF-
6nebo AuF-
6 anionty.
Neonové a heliové sloučeniny
Ionty, Ne +, (NeAr) +, (NeH) + a (HeNe +) jsou známy z optických a hmotnostních spektrometrických studií. Neon také tvoří nestabilní hydrát. Existuje několik empirických a teoretických důkazů o několika metastabilních sloučeninách hélia, které mohou existovat při velmi nízkých teplotách nebo extrémních tlacích. Stabilní kation HeH + byl popsán v roce 1925, ale nebyl považován za skutečnou sloučeninu, protože není neutrální a nelze jej izolovat. V roce 2016 vědci vytvořili heliovou sloučeninu disodný helid (Na 2 He), která byla první objevenou sloučeninou helia.
Sloučeniny radonu a oganessonu
Radon není chemicky inertní, ale jeho krátký poločas (3,8 dne pro 222 Rn) a vysoká energie jeho radioaktivity ztěžují zkoumání jeho jediného fluoridu (RnF 2 ), jeho uváděného oxidu (RnO 3 ) a jejich reakce produkty.
Oganessonové izotopy mají ještě kratší poločasy v rozmezí milisekund a dosud nejsou známy žádné sloučeniny, i když některé byly teoreticky předpovězeny. Očekává se, že bude ještě reaktivnější než radon, spíš jako normální prvek než vzácný plyn v jeho chemii.
Zprávy před xenon hexafluoroplatinátem a xenon tetrafluoridem
Klatráty

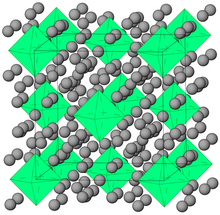
Před rokem 1962 byly jedinými izolovanými sloučeninami vzácných plynů klatráty (včetně hydrátů klatrátů ); jiné sloučeniny, jako jsou koordinační sloučeniny, byly pozorovány pouze spektroskopickými prostředky. Klatráty (také známé jako klecové sloučeniny) jsou sloučeniny vzácných plynů, ve kterých jsou zachyceny v dutinách krystalových mřížek určitých organických a anorganických látek. Podstatnou podmínkou pro jejich vznik je, aby atomy hosta (vzácný plyn) měly mít vhodnou velikost, aby se vešly do dutin krystalové mřížky hostitele; například Ar, Kr a Xe mohou tvořit klatráty s krystalickým β-chinolem, ale He a Ne se do nich nevejdou, protože jsou příliš malé. Kr a Xe se také mohou objevit jako hosté v krystalech melanoflogitu .
Krystaly helium-dusík (He (N 2 ) 11 ) byly pěstovány při teplotě místnosti při tlacích ca. 10 GPa v buňce diamantové kovadliny . Klatrát pevný argon-vodík (Ar (H 2 ) 2 ) má stejnou krystalovou strukturu jako fáze MgZn 2 Laves . Tvoří při tlaku mezi 4,3 a 220 GPa, ale Raman měření ukazují, že H 2 molekuly v Ar (H 2 ) 2 odloučí nad 175 GPa. Podobná pevná látka Kr (H 2 ) 4 se tvoří při tlacích nad 5 GPa. Má kubickou strukturu zaměřenou na obličej, kde jsou kryptonové oktaedry obklopeny náhodně orientovanými molekulami vodíku. Mezitím v pevném Xe (H 2 ) 8 atomů xenonu tvoří dimery uvnitř pevného vodíku .
Koordinační sloučeniny
Předpokládá se, že koordinační sloučeniny, jako je Ar · BF 3, existují při nízkých teplotách, ale nikdy nebyly potvrzeny. Také sloučeniny jako když s 2 a HgHe 2 bylo hlášeno, že byla vytvořena bombardováním elektrony, ale nedávný výzkum ukázal, že jsou pravděpodobně výsledkem Ten se adsorbuje na povrchu kovu; proto tyto sloučeniny nelze skutečně považovat za chemické sloučeniny.
Hydráty
Hydráty se tvoří stlačováním vzácných plynů ve vodě, kde se předpokládá, že molekula vody, silný dipól, indukuje slabý dipól v atomech vzácného plynu, což vede k interakci dipól-dipól. Těžší atomy jsou více ovlivněny než menších, proto XE • 5,75 H 2 O bylo hlášeno, že byl nejvíce stabilní hydrát; má teplotu tání 24 ° C. Byla také vyrobena deuterovaná verze tohoto hydrátu.
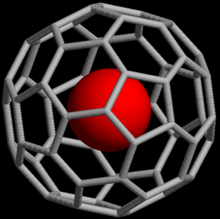
Fullerenové adukty
Ušlechtilé plyny mohou také tvořit endohedrální fullerenové sloučeniny, kde je atom vzácného plynu zachycen uvnitř molekuly fullerenu . V roce 1993 bylo zjištěno, že když C 60 je vystavena tlaku asi 3 bar He nebo Ne, komplexů He @ C 60 a Ne @ C 60 jsou vytvořeny. Za těchto podmínek byla jen asi jedna z každých 650 000 klecí C 60 dopována atomem helia ; při vyšších tlacích (3 000 bar) je možné dosáhnout výtěžku až 0,1%. Endohedral komplexy s argonem , krypton a xenon byly také získány, stejně jako četné adukty He @ C 60 .
Aplikace
Většina aplikací sloučenin vzácného plynu je buď jako oxidační činidlo, nebo jako prostředek k ukládání vzácných plynů v husté formě. Kyselina xenová je cenným oxidačním činidlem, protože nemá žádný potenciál pro zavádění nečistot - xenon se jednoduše uvolňuje jako plyn - a proto v tomto ohledu soupeří pouze s ozonem . Tyto perxenates jsou ještě silnější oxidační činidla. Oxidanty na bázi xenonu byly také použity pro syntézu karbokationtů stabilních při teplotě místnosti, v SO
2ClF roztok.
Stabilní soli xenonu obsahující velmi vysoké hmotnostní podíly fluoru (jako je tetrafluoramonium heptafluoroxenát, NF 4 XeF 7 a související tetrafluoramonium oktafluoroxenát (NF 4 ) 2 XeF 8 ) byly vyvinuty jako vysoce energetické oxidanty pro použití jako hnací látky v raketové technice .
Xenonfluoridy jsou dobrým fluoračním činidlem.
Klatráty se používají k oddělení He a Ne od Ar, Kr a Xe a také k přepravě Ar, Kr a Xe. (Například radioaktivní izotopy kryptonu a xenonu se obtížně skladují a likvidují a se sloučeninami těchto prvků lze manipulovat snadněji než s plynnými formami.) Klatráty radioizotopů mohou navíc poskytovat vhodné formulace pro experimenty vyžadující zdroje konkrétních typů záření; proto. Klatrát 85 Kr poskytuje bezpečný zdroj beta částic , zatímco klatrát 133 Xe poskytuje užitečný zdroj gama paprsků .
Oganesson nemá žádné aplikace.
Reference
Zdroje
- Khriachtchev, Leonid; Räsänen, Markku; Gerber, R. Benny (2009). „Hydridy vzácných plynů: nová chemie při nízkých teplotách“. Účty chemického výzkumu . 42 (1): 183–91. doi : 10,1021 / ar800110q . PMID 18720951 .