Elektronová hustota - Electron density
V kvantové chemii je elektronová hustota nebo elektronická hustota měřítkem pravděpodobnosti přítomnosti elektronu v nekonečně malém prvku prostoru obklopujícím daný bod. Jedná se o skalární veličinu závisející na třech prostorových proměnných a obvykle se označuje jako buď nebo . Hustota je definována prostřednictvím definice normalizovanou vlnovou funkcí elektronu, která sama závisí na proměnných ( prostorové a spinové souřadnice). Naopak hustota určuje modul vlnové funkce až do fázového faktoru, což poskytuje formální základ funkční hustotní teorie .
Podle kvantové mechaniky nelze kvůli principu nejistoty v atomovém měřítku předpovědět přesnou polohu elektronu, pouze pravděpodobnost jeho bytí v dané poloze; proto elektrony v atomech a molekulách působí, jako by byly „rozmazané“ v prostoru. U jednoelektronových systémů je elektronová hustota v libovolném bodě úměrná čtvercové velikosti vlnové funkce .
Definice
Elektronická hustota odpovídající normalizované -elektronové vlnové funkci (s a označující prostorové a spinové proměnné) je definována jako
kde je operátor odpovídající pozorovatelné hustotě
Výpočet, jak je definován výše, můžeme výraz zjednodušit následovně.
Slovy: držíme -li jeden elektron stále na místě , shrneme všechna možná uspořádání ostatních elektronů.
V Hartree -Fockových a hustotních funkčních teoriích je vlnová funkce obvykle reprezentována jako jeden Slaterův determinant sestrojený z orbitálů , s odpovídajícími povoláními . V těchto situacích se hustota zjednodušuje na
Obecné vlastnosti
Z jeho definice je elektronová hustota nezáporná funkce integrující se do celkového počtu elektronů. Dále u systému s kinetickou energií T hustota splňuje nerovnosti
U konečných kinetických energií umístí první (silnější) nerovnost druhou odmocninu hustoty do Sobolevova prostoru . Spolu s normalizací a non-negativitou definuje prostor obsahující fyzicky přijatelné hustoty jako
Druhá nerovnost umístí hustotu v L 3 prostoru . Spolu s normalizační vlastností umisťuje přijatelné hustoty v průsečíku L 1 a L 3 - nadmnožinu .
Topologie
Základní stav elektronická hustota z atomu je se domníval, že je monotónně rozpadající funkcí vzdálenosti od jádra .
Stav jaderného hrotu
Elektronická hustota zobrazuje vrcholy v každém jádru v molekule v důsledku neomezeného Coulombova potenciálu elektronové jádro. Toto chování je kvantifikováno podmínkou Katoho hrotu formulovanou jako sféricky zprůměrovaná hustota , o jakémkoli daném jádru jako
To znamená, že radiální derivace sféricky zprůměrované hustoty, hodnocená v jakémkoli jádru, se rovná dvojnásobku hustoty v tomto jádře vynásobené záporným atomovým číslem ( ).
Asymptotické chování
Podmínky jaderného hrotu poskytují chování téměř jaderné (malé ) hustoty jako
Rovněž je známé chování hustoty na velké vzdálenosti (velké )
kde I je ionizační energie systému.
Hustota odezvy
Další obecnější definicí hustoty je „hustota lineární odezvy“. Jedná se o hustotu, která při kontrakci s jakýmkoli bez spinů získá jeden elektronový operátor související vlastnost definovanou jako derivát energie. Například dipólový moment je derivátem energie vzhledem k vnějšímu magnetickému poli a není očekávanou hodnotou operátora nad vlnovou funkcí. U některých teorií jsou při konvergování vlnové funkce stejné. Počet okupací není omezen na rozsah od nuly do dvou, a proto někdy může být i hustota odezvy v určitých oblastech vesmíru záporná.
Přehled
V molekulách se kolem atomu a jeho vazeb obvykle nacházejí oblasti s velkou elektronovou hustotou . V delokalizovaných nebo konjugovaných systémech , jako je fenol , benzen a sloučeniny, jako je hemoglobin a chlorofyl , je elektronová hustota významná v celé oblasti, tj. V benzenu se nacházejí nad a pod rovinným kruhem. Někdy je to schematicky znázorněno jako řada střídajících se jednoduchých a dvojných vazeb. V případě fenolu a benzenu ukazuje kruh uvnitř šestiúhelníku delokalizovanou povahu sloučeniny. To je uvedeno níže:
Ve sloučeninách s více kruhovými systémy, které jsou propojeny, to již není přesné, proto se používají střídavé jednoduché a dvojné vazby. U sloučenin, jako je chlorofyl a fenol, některé diagramy ukazují tečkovanou nebo přerušovanou čáru, která představuje delokalizaci oblastí, kde je hustota elektronů vedle jednoduchých vazeb vyšší. Konjugované systémy mohou někdy představovat oblasti, kde je elektromagnetické záření absorbováno na různých vlnových délkách, což vede ke vzniku barevných sloučenin. V polymerech jsou tyto oblasti známé jako chromofory.
V kvantově chemických výpočtech je elektronová hustota ρ ( r ) funkcí souřadnic r definovaných tak, že ρ ( r ) d r je počet elektronů v malém objemu d r . Pro molekuly s uzavřeným obalem lze zapsat jako součet součinů základních funkcí, φ:
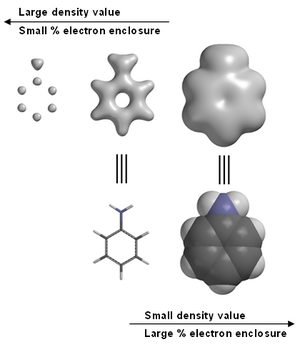
kde P je matice hustoty . Hustoty elektronů se často vykreslují na základě isosurface (an isodensity surface) s velikostí a tvarem povrchu určeným hodnotou zvolené hustoty nebo v procentech celkových uzavřených elektronů.
Software pro molekulární modelování často poskytuje grafické obrazy hustoty elektronů. Například v anilinu (viz obrázek vpravo). Grafické modely, včetně elektronové hustoty, jsou běžně používaným nástrojem v chemickém vzdělávání. Všimněte si, že na obrázku nejvíce vlevo anilinu jsou vysoké hustoty elektronů spojeny s uhlíky a dusíkem , ale vodíky s pouze jedním protonem v jejich jádrech nejsou viditelné. To je důvod, proč má rentgenová difrakce obtížnou lokalizaci pozic vodíku.
Většina softwarových balíků molekulárního modelování umožňuje uživateli zvolit hodnotu pro elektronovou hustotu, často nazývanou isovalue. Některý software také umožňuje specifikaci hustoty elektronů z hlediska procenta celkových uzavřených elektronů. V závislosti na isovalue (typickými jednotkami jsou elektrony na kubický bohr ) nebo procentuálním podílu uzavřených elektronů lze povrch elektronové hustoty použít k lokalizaci atomů, zdůraznění hustot elektronů spojených s chemickými vazbami nebo k označení celkové velikosti a tvaru molekuly.
Povrch elektronové hustoty také slouží jako plátno, na kterém lze zobrazit další elektronické vlastnosti. Mapa elektrostatického potenciálu (vlastnost elektrostatického potenciálu mapovaná na hustotě elektronů) poskytuje indikátor distribuce náboje v molekule. Mapa místního ionizačního potenciálu (vlastnost místního ionizačního potenciálu mapovaná na hustotě elektronů) poskytuje indikátor elektrofility. A mapa LUMO ( nejnižší neobsazený molekulární orbitál mapovaný na hustotě elektronů) může poskytnout indikaci pro nukleofilitu.
Experimenty
Mnoho experimentálních technik může měřit elektronovou hustotu. Například kvantová krystalografie pomocí rentgenového difrakčního skenování, kde jsou rentgenové paprsky vhodné vlnové délky zaměřeny na vzorek a měření jsou prováděna v průběhu času, poskytuje pravděpodobnostní znázornění umístění elektronů. Z těchto pozic lze pro krystalizované systémy často určit molekulární struktury a přesné rozdělení hustoty náboje. Kvantová elektrodynamika a některá odvětví kvantové teorie také studují a analyzují superpozici elektronů a další související jevy, jako je index NCI, který umožňuje studium nekovalentních interakcí pomocí elektronové hustoty. Analýza populace Mulliken je založena na hustotách elektronů v molekulách a je to způsob rozdělení hustoty mezi atomy za účelem odhadu atomových nábojů.
V transmisní elektronové mikroskopii (TEM) a hlubokém neelastickém rozptylu , stejně jako v dalších experimentech s vysokoenergetickými částicemi , vysoce energetické elektrony interagují s elektronovým mrakem, aby poskytly přímou reprezentaci elektronové hustoty. K sondování elektronové hustoty konkrétních jednotlivých atomů lze použít TEM, skenovací tunelovací mikroskopii (STM) a mikroskopii atomové síly (AFM).
Hustota odstřeďování
Hustota odstřeďování je elektronová hustota aplikovaná na volné radikály . Je definována jako celková elektronová hustota elektronů jednoho spinu minus celková elektronová hustota elektronů druhého spinu. Jedním ze způsobů, jak to experimentálně měřit, je elektronová spinová rezonance , neutronová difrakce umožňuje přímé mapování hustoty odstřeďování v 3D prostoru.
Viz také
- Mapa hustoty rozdílu
- Elektronový mrak
- Konfigurace elektronů
- Rozlišení (elektronová hustota)
- Hustota náboje
- Hustotní funkční teorie
- Pravděpodobnostní proud