Halogenová vazba - Halogen bond
K halogenové vazbě dochází, když existuje důkaz čisté přitažlivé interakce mezi elektrofilní oblastí spojenou s atomem halogenu v molekulární entitě a nukleofilní oblastí v jiné nebo stejné molekulární entitě.
Lepení
Porovnání vodíkových a halogenových vazeb:
- Vodíkové vazby
- Halogenové lepení
V obou případech je A (akceptor vodíkové/halogenové vazby) atom, skupina nebo molekula, která daruje elektrony elektronům chudým druhům HD nebo XD (dárci vodíkové nebo halogenové vazby). H je atom vodíku zapojený do vodíkové vazby a X je atom halogenu zapojený do halogenové vazby. Donor halogenové vazby přijímá elektrony, zatímco akceptor halogenové vazby elektrony daruje.
Mezi halogenovou vazbou a vodíkovou vazbou (HB) lze snadno vytvořit paralelní vztah . V obou typech vazeb existuje vztah elektron dárce / akceptor elektronu . Rozdíl mezi těmito dvěma je v tom, jaké druhy mohou působit jako donor elektronů/akceptor elektronů. Při vodíkových vazbách působí atom vodíku jako akceptor elektronů a tvoří nekovalentní interakci přijetím elektronové hustoty z místa bohatého na elektrony (donor elektronů). Při halogenové vazbě je atom halogenu akceptor elektronů. Současně normální kovalentní vazba mezi H nebo X a D oslabuje, takže se zdá, že elektronová hustota na H nebo X je snížena. Přenosy hustoty elektronů vedou k průniku van der Waalsových objemů.
Halogeny účastnící se halogenové vazby zahrnují: jod (I), brom (Br), chlor (Cl) a někdy fluor (F). Všechny čtyři halogeny jsou schopné působit jako dárci XB (jak bylo prokázáno teoretickými a experimentálními údaji) a sledují obecný trend: F <Cl <Br <I, přičemž nejsilnější interakce normálně tvoří jod.
Dihalogeny (I 2 , Br 2 atd.) Mají tendenci vytvářet silné halogenové vazby. Síla a účinnost chloru a fluoru při tvorbě XB závisí na povaze dárce XB. Pokud je halogen vázán na elektronegativní (elektrony stahující) skupinu, je pravděpodobnější, že vytvoří silnější halogenové vazby.
Například iodoperfluoroalkany jsou dobře navrženy pro krystalové inženýrství XB . Navíc, to je také důvod, proč F 2 může působit jako silné XB dárce, ale fluorované uhlovodíky jsou slabými donory XB, protože alkylová skupina připojena k fluoru není elektronegativní. Kromě toho je Lewisova báze (XB akceptor), má tendenci být elektronegativní, jak dobře a anionty jsou lepší XB akceptory než neutrálních molekul.
Halogenové vazby jsou silné, specifické a směrové interakce, které vedou k dobře definovaným strukturám. Síly halogenových vazeb se pohybují od 5 do 180 kJ/mol. Síla XB mu umožňuje konkurovat HB, které jsou o něco slabší v síle. Halogenové vazby mají tendenci se tvořit pod úhly 180 °, což bylo ukázáno ve studiích Odd Hassel s bromem a 1,4-dioxanem v roce 1954. Další faktor přispívající k síle halogenové vazby pochází z krátké vzdálenosti mezi halogenem (Lewisova kyselina, XB dárce) a Lewisova báze (akceptor XB). Atraktivní povaha halogenových vazeb vede k tomu, že vzdálenost mezi dárcem a akceptorem je kratší než součet van der Waalsových poloměrů. Interakce XB se stává silnější, protože vzdálenost mezi halogenovou a Lewisovou základnou klesá.
Dějiny
V roce 1814 Jean-Jacques Colin popsal vznik kapaliny-s kovovým leskem-když smíchal dohromady suchý plynný amoniak a suchý jód. Přesné složení výsledného komplexu I 2 ··· NH 3 stanovil o padesát let později Frederick Guthrie. Ve svém experimentu přidal I 2 do vodného amoniaku. Pravá podstata molekulární interakce byla možná poprvé pochopena teprve před půl stoletím po převratných objevech Roberta Mullikena o interakcích přenosu náboje a jejich podrobném popisu Odd Hassel.
V padesátých letech vyvinul Robert S. Mulliken podrobnou teorii komplexů donor-akceptor elektronů a klasifikoval je jako vnější nebo vnitřní komplexy. Vnější komplexy byly ty, ve kterých byla mezimolekulární interakce mezi elektronovým donorem a akceptorem slabá a měla velmi malý přenos náboje. Vnitřní komplexy mají rozsáhlou redistribuci náboje. Mullikenova teorie byla použita k popisu mechanismu, kterým dochází k tvorbě XB.
Přibližně ve stejném časovém období, ve kterém Mulliken rozvinul svoji teorii, začaly vznikat krystalografické studie prováděné Hasselem a staly se zlomovým bodem v chápání tvorby XB a jejích charakteristik.
První rentgenová krystalografická studie od Hasselovy skupiny přišla v roce 1954. V experimentu jeho skupina dokázala ukázat strukturu brom-1,4-dioxanátu pomocí rentgenových difrakčních technik. Experiment odhalil, že mezi atomy kyslíku dioxanu a bromu byla přítomna krátká mezimolekulární interakce. Vzdálenost O -Br v krystalu byla měřena na 2,71 Á, což naznačuje silnou interakci mezi atomy bromu a kyslíku. Kromě toho je vzdálenost menší než součet van der Waalsových poloměrů kyslíku a bromu (3,35 Å). Úhel mezi vazbou O -Br a Br -Br je asi 180 °. Toto byl první důkaz typických charakteristik nalezených při tvorbě halogenových vazeb a vedl Hassela k závěru, že atomy halogenu jsou přímo spojeny s dárcem elektronových párů se směrem vazby, který se shoduje s osami orbitálů osamělých párů v dárci elektronových párů molekula.
V roce 1969 získal Hassel Nobelovu cenu za chemii za mimořádný objev, že halogeny mohou v přítomnosti donorů elektronů působit jako elektrofilní, akceptory elektronů a samy se sestavovat do vysoce směrově organizovaných komplexů krystalického přenosu náboje. Časný recenzi o elektronový donor-akceptor poskytl Bent v roce 1968. Použití termínu „halogen“ vazby nebylo provedeno až 1978 Dumas a spolupracovníky, který zkoumal komplexy CCL 4 , CBR 4 , SiCl 4 , a Síbr 4 s tetrahydrofuranem , tetrahydropyranem , pyridinem , anisolem a di-n-butyletherem v organických rozpouštědlech.
Povaha a aplikace halogenové vazby se však začaly intenzivně studovat až v polovině 90. let. Systematická a rozsáhlá práce Legona a spolupracovníků, kteří studovali širokou škálu halogenově vázaných aduktů vytvořených v plynné fázi pomocí mikrovlnné spektroskopie, upozornila na podobnosti mezi halogenovými vazbami a známějšími interakcemi vodíkových vazeb. Výpočtové výpočty Politzera a Murraye byly zvláště významné, protože odhalily, že vysoká směrovost halogenové vazby je výsledkem anizotropního rozdělení hustoty elektronů kolem halogenového jádra a vydláždilo cestu k definici „σ-díry“.
V současné době je XB využíván pro řadu funkčních aplikací, např. Pro krystalovou techniku, supramolekulární chemii, polymerní vědy, tekuté krystaly, vodivé materiály a lékařskou chemii.
Aplikace
Krystalová technika
Krystalické inženýrství je rostoucí oblastí výzkumu, která spojuje pevnou a supramolekulární chemii. Tento jedinečný obor je interdisciplinární a spojuje tradiční obory, jako je krystalografie , organická chemie a anorganická chemie . V roce 1971 Schmidt poprvé založil obor publikací o fotodimerizaci v pevném stavu. Novější definice identifikuje krystalové inženýrství jako využití intermolekulárních interakcí pro krystalizaci a pro vývoj nových látek s různými požadovanými fyzikálně -chemickými vlastnostmi. Před objevením halogenových vazeb přístup ke krystalovému inženýrství zahrnoval použití vodíkových vazeb , koordinační chemie a interionové interakce pro vývoj kapalných krystalických a pevných krystalických materiálů. Kromě toho se halogenová vazba používá pro organizaci radikálních kationtových solí, výrobu molekulárních vodičů a vytváření konstruktů z tekutých krystalů. Od objevu halogenových vazeb existují nové molekulární sestavy. Vzhledem k jedinečné chemické povaze halogenových vazeb slouží tato mezimolekulární interakce jako další nástroj pro vývoj krystalového inženýrství.
První hlášené použití halogenové vazby při tvorbě tekutých krystalů provedl H. Loc Nguyen. Ve snaze vytvořit tekuté krystaly byly použity alkoxystilbazoly a pentafluoroiodobenzen. Předchozí studie společností Metrangolo a Resnati prokázaly užitečnost pentafluoroiodobenzenu pro struktury v pevném stavu. Pro nelineární optiku a metalomesogeny byly použity různé alkoxystilbazoly. Pomocí dalšího nálezu Resnatiho (např. N-I komplexy se tvoří silně) skupina vytvořila halogenem vázané komplexy s jodopentafluorobenzenem a 4-alkoxystilbazoly. Rentgenová krystalografie odhalila vzdálenost N-I 2,811 (4) Å a vazebný úhel byl 168,4 °. Podobné vzdálenosti N -I byly měřeny v pevných prášcích. Zjištěná vzdálenost N − I je kratší než součet Van Der Waalsových poloměrů pro dusík a jód (3,53 Å). Jednokrystalová struktura molekul naznačovala, že nebyly přítomny žádné kvadrupolární interakce. Bylo zjištěno, že komplexy na obrázku 4 jsou kapalně krystalické.
Pro testování pojmu zapojení polarizovatelnosti do síly halogenové vazby byl jako Lewisova báze použit bromopentafluorbenzen. V důsledku toho nebylo získáno ověření tvorby komplexu halogenových vazeb. Toto zjištění poskytuje větší podporu závislosti halogenových vazeb na atomové polarizovatelnosti. Pomocí podobných rámců dárce-akceptor autoři prokázali, že síla halogenové vazby v kapalném krystalickém stavu je srovnatelná s mezogeny vázanými vodíkem.
Příprava poly (dijododiacetylenu)
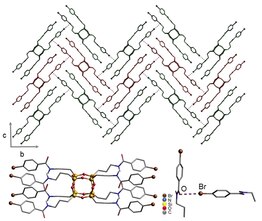
Aplikace využívající vlastnosti konjugovaných polymerů vyplynuly z prací Heegera, McDiaramida a Shirakawy s objevem, že polyacetylen je vodivý, i když obtížně zpracovatelný materiál. Od té doby se pracuje na napodobení páteře tohoto konjugovaného polymeru (např. Poly (p-fenylenevinylen)). Konjugované polymery mají mnoho praktických aplikací a používají se v zařízeních, jako jsou fotovoltaické články , organické diody emitující světlo , tranzistory s efektem pole a chemické senzory . Goroff a kol. připravený uspořádaný poly (dijododiacetylen) (PIDA) pomocí předběžného uspořádání monomeru (2) s lešením halogenových vazeb. PIDA je vynikajícím předchůdcem jiných konjugovaných polymerů, protože jod lze snadno transformovat. Například štěpení C -I je možné elektrochemickou redukcí .
Krystalické struktury monomeru (2) jsou neuspořádané materiály různého složení a konektivity. Hostitelé (3–7) byli vyšetřováni na jejich molekulární balení, primárně studiem kokrystalů monomeru (2) a příslušného hostitele. Jak (3), tak (4) předem organizovaný monomer (2), ale sterické shlukování kolem jódů bránilo úspěšné topologické polymeraci monomeru. Hostitelé (5–7) využívají vodíkové vazby a halogenové vazby k udržení monomeru (2) v optimální vzdálenosti od sebe, aby se usnadnila polymerace.
Ve skutečnosti, když byl použit hostitel 7, polymerace probíhala spontánně po izolaci kokrystalů. Krystalové struktury ukazují, že všechny polymerní řetězce jsou paralelní k síti vodíkových vazeb a hostitelské nitrily jsou každý halogenově vázány na atomy jódu. Polovina atomů jodu v (1) v krystalu je v těsném kontaktu s atomy kyslíku oxalamidu. Atomy kyslíku hostitele 7 působí jako akceptory vodíkové i halogenové vazby.

Porézní struktury
Porézní struktury mají různé využití. Mnoho chemiků a materiálových vědců pracuje na vylepšení metal-organických rámců (MOF) pro skladování vodíku pro použití v automobilech. Tyto vysoce organizované krystalické inkluzní komplexy mají potenciální využití v katalýze a molekulárních separačních zařízeních. Molekulární organizace je často řízena mezimolekulárními silami, jako je vodíková vazba . Využití vodíkových vazeb však často omezuje rozsah velikostí pórů, které jsou k dispozici, kvůli těsnému zabalení.
Pigge a kol., Využili interakce halogenových vazeb mezi aminy , dusíkovými heterocykly , karbonylovými skupinami a dalšími organickými halogenidy , ke konstrukci jejich porézních struktur. To je významné, protože organické krystalické sítě zprostředkované halogenovými vazbami, interakce výrazně slabší než vodíková vazba, jsou vzácné.
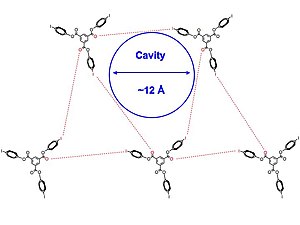
Krystalické struktury 1 a 2 [níže] byly získány v různých rozpouštědlech , jako je dichlormethan , pyridin a benzen . Autoři poznamenávají, že porézní inkluzní komplexy se zdají být částečně zprostředkovány nebývalými interakcemi I-π a halogenovou vazbou mezi jodovými a karbonylovými skupinami. Krystalová struktura [viz níže] se spojily v trojúhelníkovém seskupení a molekuly 2 jsou přibližně symetrické. Navíc všechny sady interakcí halogenových vazeb nejsou identické a všechny intermolekulární interakce mezi halogenem a akceptorem halogenových vazeb mírně překračují součet Van der Waalsova poloměru , což znamená o něco slabší halogenovou vazbu, což vede k větší flexibilitě struktura. 2D vrstvy se skládají navzájem rovnoběžně a vytvářejí kanály naplněné rozpouštědlem.
Interakce rozpouštědel jsou také zaznamenány při tvorbě hexagonálních struktur, zejména v pyridinu a chloroformu . Zpočátku krystaly, které tvoří tato řešení, vytvářejí usměrněné struktury. Postupem času se nové jehlovité struktury bez solvátů sbalí pevněji a tyto jehly jsou ve skutečnosti termodynamicky oblíbeným krystalem. Autoři doufají, že použijí tyto informace k lepšímu porozumění komplementární povaze vodíkových vazeb a halogenových vazeb za účelem návrhu malých molekul předpovídajících struktury.
Halogenová vazba v biologických makromolekulách
Nějakou dobu byl přehlížen význam halogenových vazeb na biologickou makromolekulární strukturu. Na základě jednokrystalových struktur v proteinové datové bance (PDB) (verze z července 2004), studie Auffingera a dalších na monokrystalových strukturách s rozlišením 3 Å nebo lépe zadaných do PDB odhalila, že v šesti bylo nalezeno více než 100 halogenových vazeb struktury nukleových kyselin na halogenované bázi a šedesát šest komplexů protein-substrát pro interakce halogen-kyslík. I když ne tak časté jako interakce halogen-kyslík, byly také identifikovány kontakty halogen-dusík a halogen-síra. Tato vědecká zjištění poskytují jedinečný základ pro objasnění úlohy halogenových vazeb v biologických systémech.
Na biomolekulární úrovni je halogenová vazba důležitá pro specificitu substrátu, vazbu a skládání molekul. V případě interakcí protein-ligand zahrnují nejběžnější vazby přenosu náboje s polarizovatelnými halogeny páteřní karbonylové a/nebo hydroxylové a karboxylátové skupiny aminokyselinových zbytků. V komplexech DNA a protein-ligand je typicky vzdálenost vazeb mezi donorovými atomy Lewisovy báze (např. O, S, N) a Lewisovou kyselinou (halogen) kratší než součet jejich Van der Waalsova poloměru. V závislosti na strukturním a chemickém prostředí mohou být interakce halogenových vazeb slabé nebo silné. V případě některých komplexů protein-ligand jsou halogenové vazby energeticky a geometricky srovnatelné s vodíkovými vazbami, pokud směrovost donor-akceptor zůstává konzistentní. Ukázalo se, že tato intermolekulární interakce je stabilizující a je konformačním determinantem ve strukturách protein-ligand a DNA.
Pro molekulární rozpoznávání a vazbu může být významné halogenové spojení. Příkladem tohoto tvrzení při navrhování léčiv je substrátová specificita pro vazbu IDD 594 na lidskou aldózreduktázu . EI Howard uvedl nejlepší rozlišení pro tento monomerní enzym. Tato biologická makromolekula se skládá z 316 zbytků a redukuje aldózy, kortikosteroidy a aldehydy. Předpokládá se, že D-sorbitol, produkt enzymatické přeměny D-glukózy, přispívá k následným účinkům patologie diabetu. Inhibice tohoto enzymu má tedy terapeutickou hodnotu.
Inhibitory na bázi aldehydu a karboxylátu jsou účinné, ale toxické, protože je narušena funkční aktivita aldehydreduktázy. Ukázalo se, že inhibitory karboxylátu a aldehydu jsou vodíkové vazby s Trp 111, Tyr 48 a His 110. „Kapsa specificity“, vytvořená v důsledku vazby inhibitoru, se skládá z Leu 300, Ala 299, Phe 122, Thr 113 a Trp 111. Aby byly inhibitory účinné, byly identifikovány klíčové zbytky interakce jako Thr 113 a Trp 111. IDD 594 byl navržen tak, aby halogen poskytoval selektivitu a byl účinný. Po navázání tato sloučenina indukuje konformační změnu, která způsobí, že dojde k halogenové vazbě mezi kyslíkem Thr a bromem inhibitoru. Vzdálenost vazby byla naměřena na 2,973 (4) Á. Je to tato O -Br halogenová vazba, která přispívá k velké účinnosti tohoto inhibitoru pro lidskou aldózoreduktázu spíše než pro aldehydreduktázu .