Trimethylaluminium - Trimethylaluminium
|
|
|
|
| Jména | |
|---|---|
|
Název IUPAC
Trimethylaluman
|
|
| Ostatní jména
Trimethylaluminium; trimethyl hlinitý; trimethyl hlinitý
|
|
| Identifikátory | |
|
3D model ( JSmol )
|
|
| ChemSpider | |
| Informační karta ECHA |
100 000,776 |
|
PubChem CID
|
|
| UNII | |
|
CompTox Dashboard ( EPA )
|
|
|
|
| Vlastnosti | |
| C 6 H 18 Al 2 | |
| Molární hmotnost | 144,17 g/mol 72,09 g/mol (C 3 H 9 Al) |
| Vzhled | Bezbarvá kapalina |
| Hustota | 0,752 g / cm 3 |
| Bod tání | 15 ° C (59 ° F; 288 K) |
| Bod varu | 125–130 ° C (257–266 ° F; 398–403 K) |
| Reaguje | |
| Tlak páry | |
| Viskozita | |
| Termochemie | |
|
Tepelná kapacita ( C )
|
155,6 J/mol · K |
|
Standardní molární
entropie ( S |
209,4 J/mol · K |
|
Standardní entalpie
tvorby (Δ f H ⦵ 298 ) |
−136,4 kJ/mol |
|
Gibbsova volná energie (Δ f G ˚)
|
−9,9 kJ/mol |
| Nebezpečí | |
| Hlavní nebezpečí | Pyroforický |
| Piktogramy GHS |
 
|
| Signální slovo GHS | Nebezpečí |
| H250 , H260 , H314 | |
| P222 , P223 , P231+232 , P280 , P370+378 , P422 | |
| NFPA 704 (ohnivý diamant) | |
| Bod vzplanutí | −17,0 ° C (1,4 ° F, 256,1 K) |
| Související sloučeniny | |
|
Související sloučeniny
|
Triethylaluminium |
|
Pokud není uvedeno jinak, jsou údaje uvedeny pro materiály ve standardním stavu (při 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Reference na infobox | |
Trimethylaluminium je jedním z nejjednodušších příkladů organoaluminiové sloučeniny. Přes svůj název má vzorec Al 2 ( CH 3 ) 6 (zkráceně Al 2 Me 6 nebo TMA), protože existuje jako dimer . Tato bezbarvá kapalina je pyroforická . Je to průmyslově důležitá sloučenina, blízce příbuzná triethylaluminiu .
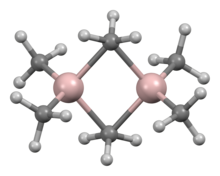
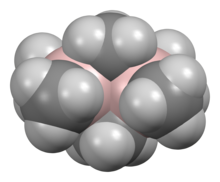
Struktura a lepení
Struktura a vazby v Al 2 R 6 a diboranu jsou analogické (R = alkyl). V Al 2 Me 6 jsou vzdálenosti Al-C (terminál) a Al-C (přemosťování) 1,97, respektive 2,14 Á. Centrum Al je čtyřboké. Atomy uhlíku přemosťujících methylových skupin jsou obklopeny pěti sousedy: třemi atomy vodíku a dvěma atomy hliníku. Methylové skupiny se snadno vyměňují intramolekulárně. Při vyšších teplotách dimer praskne na monomerní AlMe 3 .
Syntéza
TMA se připravuje ve dvou krocích, které lze shrnout takto:
- 2 Al + 6 CH 3 Cl + 6 Na → Al 2 (CH 3 ) 6 + 6 NaCl
Aplikace
Katalýza
Počínaje vynálezem Ziegler-Nattovy katalýzy mají organoaluminiové sloučeniny prominentní úlohu při výrobě polyolefinů , jako je polyethylen a polypropylen . Methylaluminoxan , který se vyrábí z TMA, je aktivátorem mnoha katalyzátorů přechodových kovů.
Polovodičové aplikace
TMA se také používá při výrobě polovodičů k nanášení tenkých vrstev, dielektrik s vysokým k, jako je Al 2 O 3, pomocí procesů chemického depozice par nebo depozice atomové vrstvy . TMA je výhodným prekurzorem pro organokovových plynné fáze epitaxe ( MOVPE ) z hliníku s obsahem sloučenin polovodičů , jako například : Ach , AlN , ALP , AlSb , AlGaAs , AlInGaAs , AlInGaP , AlGaN , AlInGaN , AlInGaNP atd Kritéria pro TMA kvality zaměřením na a) elementární nečistoty, b) okysličené a organické nečistoty.
Fotovoltaické aplikace
V depozičních procesech velmi podobných zpracování polovodičů se TMA používá k nanášení tenkých vrstev vrstev dielektrické vrstvy s nízkým k (neabsorbujícím) na Al 2 O 3 pomocí procesů chemické depozice par nebo depozice atomové vrstvy . Al 2 O 3 poskytuje vynikající povrchovou pasivaci p-dopovaných silikonových povrchů. Vrstva Al 2 O 3 je typicky spodní vrstvou s více vrstvami nitridu křemíku (Si x N y ) pro uzavření.
Reakce
Trimethylaluminium se snadno hydrolyzuje, dokonce nebezpečně:
- AlMe 3 + 1,5 H 2 O → 0,5 Al 2 O 3 + 3 CH 4
Za kontrolovaných podmínek může být reakce zastavena za vzniku methylaluminoxanu:
- AIMe 3 + H 2 O → 1 / n [AlMeO] n + 2 CH 4
Alkoholýza a aminolýza probíhají srovnatelně. Například dimethylamin poskytuje dimer diamidu dialuminia:
- 2 AIMe 3 + 2 HNMe 2 → [AIMe 2 NMe 2 ] 2 + 2 CH 4
Reakce s chloridy kovů
TMA reaguje s mnoha halogenidy kovů a instaluje alkylové skupiny. V kombinaci s chloridem galia poskytuje trimethylgallium . Al 2 Me 6 reaguje s chloridem hlinitým za vzniku (AlMe 2 Cl) 2 .
Reakce TMA/halogenidu kovu se objevily jako činidla v organické syntéze . Tebbeovo činidlo , které se používá k methylenaci esterů a ketonů , se připravuje z TMA a dichloridu titanocénu . V kombinaci s 20 až 100% mol Cp 2 ZrCl 2 ( zirkonocendichloridu ) je (CH 3 ) 2 Al-CH 3 dodává „přes“ alkyny, čímž se získá vinyl hliníkové sloučeniny, které jsou užitečné v organické syntéze v reakci, zvané carboalumination.
Adukty
Stejně jako u jiných sloučenin „elektronově deficitní“, trimethylaluminium dává adukty R 3 N . AlMe 3 . Vlastnosti Lewisovy kyseliny AlMe 3 byly kvantifikovány. Data z entalpie ukazují, že AlMe 3 je tvrdá kyselina a její parametry kyselosti v modelu ECW jsou E A = 8,66 a C A = 3,68.
Tyto adukty, např. Komplex s terciárním aminem DABCO , jsou bezpečnější pro manipulaci než samotný TMA.
NASA mise ATREX ( anomálního transportu Rocket Experiment ) použil bílý kouř, který TMA formy na kontaktu se vzduchem ke studiu vysoké nadmořské výšce tryskové proudění.
Syntetické činidlo
TMA je zdrojem methylových nukleofilů, podobného methyllithiu , ale méně reaktivní. Reaguje s ketony za vzniku terciárních alkoholů po hydrolytickém zpracování.
Bezpečnost
Trimethylaluminium je pyroforické, prudce reaguje se vzduchem a vodou.

