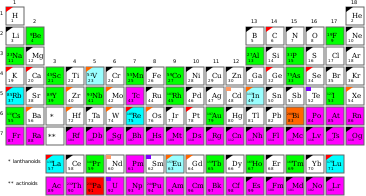
Mononukleidový prvek - Mononuclidic element
Mononuclidic prvek nebo monotopic prvek je jedním z 22 chemických prvků , které se přirozeně vyskytuje na Zemi v podstatě jako jediný nuklidu (které mohou, ale nemusí, být stabilní nuklid ). Tento jediný nuklid bude mít charakteristickou atomovou hmotnost . Přirozenému množství izotopů prvku tedy dominuje buď jeden stabilní izotop, nebo jeden izotop s velmi dlouhou životností. V první kategorii je 19 prvků (které jsou jak monoisotopické, tak mononukleidové) a 3 ( vizmut , thorium a protaktinium ) ve druhé kategorii (mononukleidové, ale nikoli monoisotopické, protože mají nulové, ne jeden, stabilní nuklidy). Seznam 22 mononukleidových prvků je uveden na konci tohoto článku.
Z 26 monoisotopických prvků, které podle definice mají pouze jeden stabilní izotop, existuje 7 (26 minus 19 = 7), které však nejsou považovány za mononukleidové, kvůli přítomnosti významné části velmi dlouhého trvání ( primordiální ) radioizotop vyskytující se v jejich přirozeném množství. Těmito prvky jsou vanad , rubidium , indium , lanthan , europium , rhenium a lutetium .
Obsah
Použití v metrologii
Mononukleidové prvky mají vědecký význam, protože jejich atomové hmotnosti lze měřit s vysokou přesností, protože v daném vzorku existuje minimální nejistota spojená s množstvím izotopů. Jiným způsobem, jak to vyjádřit, je to, že pro tyto prvky jsou standardní atomová hmotnost a atomová hmotnost stejné.
V praxi se ve standardní metrologii atomové hmotnosti používá pouze 11 mononukleidových prvků. Jedná se o hliník, vizmut, cesium, kobalt, zlato, mangan, fosfor, skandium, sodík, terbium a thorium.
V nukleární magnetické rezonanční spektroskopii (NMR) jsou třemi nejcitlivějšími stabilními jádry vodík-1 ( 1 H), fluor-19 ( 19 F) a fosfor-31 ( 31 P). Fluor a fosfor jsou monoisotopické, téměř s vodíkem. 1 H-NMR , 19 F NMR a 31 P NMR umožňují identifikaci a studium sloučenin, které obsahují tyto prvky.
Kontaminace nestabilními stopovými izotopy
Stopové koncentrace nestabilních izotopů některých mononukleidních prvků se nacházejí v přírodních vzorcích. Například beryllium-10 ( 10 Be), s poločasem 1,4 milionů let, je produkován kosmického záření v uživatelské Země ‚s horních vrstvách atmosféry ; jod-129 ( 129 I), s poločasem rozpadu 15,7 milionů let, je produkován různými kosmogenními a jadernými mechanismy; cesium-137 ( 137 Cs) s poločasem rozpadu 30 let je generováno jaderným štěpením . Takové izotopy se používají v různých analytických a forenzních aplikacích.
Kompletní seznam 22 mononukleidových prvků
Data z atomových vah a izotopových směsí vyd. JS Coursey, DJ Schwab a RA Dragoset, National Institute of Standards and Technology (2005).
| Živel | Nuklid | Z ( p ) | N ( n ) | Izotopová hmotnost ( u ) | Poznámky |
|---|---|---|---|---|---|
| berylium | 9 Buďte | 4 | 5 | 9.012 182 (3) | |
| fluor | 19 F. | 9 | 10 | 18,998 403 2 (5) | |
| sodík | 23 Na | 11 | 12 | 22,989 770 (2) | |
| hliník | 27 Al | 13 | 14 | 26,981 538 (2) | |
| fosfor | 31 P | 15 | 16 | 30 977 761 (2) | |
| skandium | 45 Sc | 21 | 24 | 44 955 910 (8) | |
| mangan | 55 Mn | 25 | 30 | 54 938 049 (9) | |
| kobalt | 59 Co | 27 | 32 | 58 933 200 (9) | |
| arsen | 75 As | 33 | 42 | 74,921 60 (2) | |
| yttrium | 89 Y | 39 | 50 | 88,905 85 (2) | |
| niob | 93 Nb | 41 | 52 | 92,906 38 (2) | |
| rhodium | 103 Rh | 45 | 58 | 102,905 50 (2) | |
| jód | 127 I | 53 | 74 | 126,904 47 (3) | |
| cesium | 133 Cs | 55 | 78 | 132,905 45 (2) | |
| praseodym | 141 Pr | 59 | 82 | 140,907 65 (2) | |
| terbium | 159 TB | 65 | 94 | 158,925 34 (2) | |
| holmium | 165 Ho | 67 | 98 | 164,930 32 (2) | |
| thulium | 169 Tm | 69 | 100 | 168.934 21 (2) | |
| zlato | 197 au | 79 | 118 | 196,966 55 (2) | |
| vizmut | 209 Bi | 83 | 126 | 208.980 38 (2) | (radioaktivní) |
| thorium | 232 čt | 90 | 142 | 232.038 1 (1) | (radioaktivní) |
| protactinium | 231 Pa | 91 | 140 | 231.035 88 (2) | (radioaktivní) |
Viz také
- Prvotní prvek
- Tabulka nuklidů tříděných podle poločasu rozpadu
- Tabulka nuklidů
- Izotopová geochemie
- Radionuklid
- Seznam prvků podle stability izotopů
- Seznam prvků podle jaderné stability