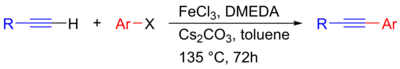Sonogashira spojka - Sonogashira coupling
| Sonogashira spojka | |
|---|---|
| Pojmenoval podle | Kenkichi Sonogashira |
| Typ reakce | Spojovací reakce |
| Identifikátory | |
| Portál organické chemie | sonogashira-spojka |
| ID ontologie RSC | RXNO: 0000137 |
| Příklady a související reakce | |
| Podobné reakce | Spojka Sonogashira bez mědi |
Sonogashirova reakce je zkřížený kapling použitý v organické syntéze , za vzniku vazby uhlík-uhlík . Využívá palladiový katalyzátor a měděný kokatalyzátor k vytvoření vazby uhlík-uhlík mezi koncovým alkynem a arylovým nebo vinylhalogenidem .
| Reakce Sonogashiry |
|---|
- R 1 : aryl
- R 2 : aryl nebo vinyl
- X: I, Br, Cl nebo OTf
Reakce Sonogashira s křížovou vazbou byla použita v celé řadě oblastí díky své užitečnosti při tvorbě vazeb uhlík-uhlík. Reakci je možno provádět za mírných podmínek, například při teplotě místnosti, ve vodném médiu a s mírnou zásadou, což umožnilo použití reakce křížové kopulace Sonogashira při syntéze komplexních molekul. Mezi její aplikace patří farmaceutika, přírodní produkty, organické materiály a nanomateriály. Specifické příklady zahrnují jeho použití při syntéze tazarotenu , což je léčba psoriázy a akné , a při přípravě SIB-1508Y, známého také jako Altinicline , agonista nikotinového receptoru .
Dějiny
Alkinylační Reakce arylhalogenidů za použití aromatické Acetyleny byl zaznamenán v roce 1975 ve třech nezávislých příspěvků Cassar, Dieck a Heckovy i Sonogashirova , Tohda a Hagihara. Všechny reakce používají palladiové katalyzátory k získání stejných reakčních produktů. Protokoly Cassara a Hecka se však provádějí výhradně za použití palladia a vyžadují drsné reakční podmínky (tj. Vysoké reakční teploty). Použití mědi a kokatalyzátoru kromě komplexů palladia v Sonogashirově postupu umožnilo, aby reakce probíhaly za mírných reakčních podmínek ve vynikajících výtěžcích. Následoval rychlý vývoj systémů Pd/Cu, který umožnil bezpočet syntetických aplikací, zatímco podmínky Cassar-Heck zůstaly, možná neprávem, téměř zapomenuty. Pozoruhodnou užitečnost reakce lze prokázat množstvím výzkumů, které se stále provádějí s cílem porozumět a optimalizovat její syntetické schopnosti, jakož i použitím postupů k přípravě různých sloučenin syntetického, lékařského nebo materiálového/průmyslového významu. Mezi reakcemi cross-coupling to vyplývá z počtu publikací hned po reakci Suzukiho a Hecka a hledání výrazu „Sonogashira“ ve Scifinderu poskytuje v letech 2007 až 2010 více než 1 500 odkazů na publikace časopisů.
Sonogashirova reakce se stala tak dobře známou, že často jsou všechny reakce, které používají moderní organokovový katalyzátor ke spojování alkinových motivů, označovány jako nějaká varianta „Sonogashirovy reakce“ , a to navzdory skutečnosti, že tyto reakce nejsou prováděny za skutečných Sonogashirových reakčních podmínek.
Mechanismus
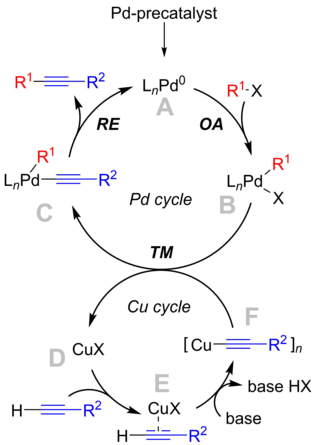
Mechanismus reakce není jasně pochopen, ale mechanismus učebnice se točí kolem cyklu palladia, který je v souladu s „klasickým“ mechanismem křížové vazby , a cyklu mědi, který je méně známý.
Cyklus palladia
- Palladium precatalyst druh je aktivován za reakčních podmínek, za vzniku reaktivního Pd 0 sloučeninu, A . Přesná identita katalytických druhů silně závisí na reakčních podmínkách. S jednoduchými fosfiny, jako je PPh 3 (n = 2), a v případě objemných fosfinů (tj. P ( o -Tol)
3) bylo prokázáno, že se tvoří monoligované druhy (n = 1). Některé výsledky dále poukazují na tvorbu aniontových druhů palladia, [L 2 Pd 0 Cl] - , což by mohly být skutečné katalyzátory v přítomnosti aniontů a halogenidů. - Aktivní Pd 0 katalyzátor se podílí na oxidační přidání kroku s arylovou nebo vinyl-halogenidu substrát pro výrobu Pd II druh B . Podobně jako ve výše uvedené diskusi závisí její struktura na použitých ligandech. Tento krok je považován za krok omezující rychlost reakce.
- Komplex B reaguje s acetylidem měďnatým, komplexem F , v transmetaličním kroku, čímž se získá komplex C a regeneruje se měděný katalyzátor.
- Struktura komplexu C závisí na vlastnostech ligandů. Aby mohlo dojít k snadné reduktivní eliminaci , musí být motivy substrátu v těsné blízkosti, tj. Cis-orientace, takže může být zapojena trans-cis izomerizace . Při reduktivní eliminaci se produktový tolan vytlačí z komplexu a regeneruje se aktivní katalytický druh Pd.
Cyklus mědi
- Cyklus mědi není úplně dobře popsán. Předpokládá se, že za přítomnosti zásady vede k tvorbě n-alkyn komplexu E . To zvyšuje kyselost koncového protonu a po deprotonaci vede k tvorbě acetylidu mědi, komplexu F.
- Acetylid F se pak podílí na transmetalací reakci s palladiovým meziproduktu B .
Mechanismus varianty Sonogashira bez mědi
Ačkoliv je to prospěšné pro účinnost reakce, použití solí mědi v „klasické“ Sonogashirově reakci je doprovázeno několika nevýhodami, jako je použití reagentů, která nejsou šetrná k životnímu prostředí, tvorba nežádoucího homocouplingu alkynů ( vedlejší produkty Glaser ) a nezbytnost přísného vyloučení kyslíku v reakční směsi. S cílem vyloučit měď z reakce bylo tedy vynaloženo velké úsilí ve vývoji reakce Sonogashira bez Cu. Spolu s vývojem nových reakčních podmínek se mnoho experimentálních a výpočetních studií zaměřilo na objasnění reakčního mechanismu. Až donedávna se diskutovalo o přesném mechanismu, kterým dochází k reakci bez Cu, přičemž kritické mechanické otázky nebyly zodpovězeny. V roce 2018 to prokázali Košmrlj et al. že reakce probíhá ve dvou propojených katalytických cyklech Pd 0 /Pd II .
| Mechanismus reakce Sonogashira bez Cu. |
|---|
- Podobně jako u původního mechanismu, cyklus Pd 0 začíná oxidačním přidáním arylhalogenidu nebo triflátu ke katalyzátoru Pd 0 , za vzniku komplexu B a aktivací arylhalogenidového substrátu pro reakci.
- Acetylen je aktivován ve druhém cyklu zprostředkovaném Pd II . Bylo prokázáno, že fenylacetylen tvoří Pd monoacetylidový komplex D a také Pd bisacetylidový komplex F za mírných reakčních podmínek.
- Oba aktivované druhy, a to komplexy B a F , se podílejí na transmetalací kroku tváření komplexní C a regenerační D .
- Výsledné produkty reduktivní eliminace , disubstituovaný alkynový produkt a regenerované katalytické druhy Pd 0 , dokončují katalytický cyklus Pd 0 .
Bylo ukázáno, že aminy jsou kompetitivní vůči fosfinům a mohou se také účastnit jako ligandy L v popsaných reakčních druzích. V závislosti na rychlosti soutěže mezi aminy a fosfiny se při použití různých koordinačních základů očekává dynamická a komplexní souhra.
Reakční podmínky
Sonogashirova reakce obvykle probíhá za mírných podmínek. Křížová kopulace se provádí při teplotě místnosti s bází, typicky aminem, jako je diethylamin , který také působí jako rozpouštědlo. Reakční médium musí být zásadité, aby neutralizovalo halogenovodík produkovaný jako vedlejší produkt této kopulační reakce, takže jako rozpouštědla se někdy používají alkylaminové sloučeniny, jako je triethylamin a diethylamin , ale také jako rozpouštědlo lze použít DMF nebo ether. Příležitostně se používají i jiné zásady, jako je uhličitan draselný nebo uhličitan česný. Kromě toho jsou pro kondenzační reakce Sonogashiry formálně zapotřebí odvzdušněné podmínky, protože komplexy palladia (0) jsou ve vzduchu nestabilní a kyslík podporuje tvorbu homocoupled acetylenů. V poslední době umožňuje vývoj organopalladiových katalyzátorů stabilních na vzduchu tuto reakci provádět v okolní atmosféře. Kromě toho RM Al-Zoubi a co-works úspěšně vyvíjejí metodu s vysoce regioselektivitou pro 1,2,3-trihaloarenové deriváty v dobrých až vysokých výtěžcích za okolních podmínek.
Katalyzátory
Pro tuto reakci jsou obvykle zapotřebí dva katalyzátory: zerovalentní komplex palladia a halogenidová sůl mědi. Mezi běžné příklady palladiových katalyzátorů patří katalyzátory obsahující fosfinové ligandy, jako je [Pd (PPh
3)
4] . Dalším běžně používaným zdrojem palladia je [ Pd (PPh
3)
2Cl
2] , ale komplexy obsahující bidentátní fosfinové ligandy , jako [Pd ( dppe ) Cl
2] , [Pd ( dppp ) Cl
2] a [Pd (dppf) Cl
2] byly také použity. Nevýhodou těchto katalyzátorů je potřeba vysokého množství palladia (až 5 mol %) spolu s větším množstvím měděného kokatalyzátoru. KomplexyPd II jsou ve skutečnosti předkatalyzátory, protože před zahájením katalýzy musí být redukovány na Pd (0). Pd II komplexy obecně vykazují vyšší stabilitu než Pd 0 komplexy a mohou být uloženy za běžných laboratorních podmínek po dobu měsíců. KatalyzátoryPd II sev reakční směsiredukují na Pd 0 aminem , fosfinovým ligandem nebo jiným reakčním činidlem ve směsi, což umožňuje pokračování reakce. Například oxidace trifenylfosfinu na trifenylfosfin oxid může vést k tvorbě Pd 0 in situ, když [Pd (PPh
3)
2Cl
2] se používá.
Soli mědi (I), jako je CuI , reagují s koncovým alkynem a vytvářejí acetylid mědi (I), který působí jako aktivovaný druh pro kopulační reakce. Cu (I) je v reakci kokatalyzátor a používá se ke zvýšení rychlosti reakce.
Arylhalogenidy a pseudohalidy
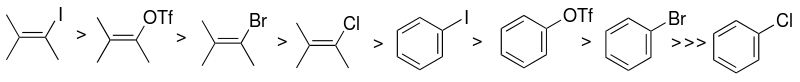
Volba arylhalogenidového nebo pseudohalidového substrátu (sp 2 -uhlík) je jedním z faktorů, které ovlivňují hlavně reaktivitu katalytického systému Sonogashira. Reaktivita halogenidů je vyšší vůči jodu a vinylové hallidy jsou reaktivnější než analogické arylhalogenidy.
Místo arylhalogenidů lze také použít aryltrifláty.
Prekurzory arenediazonia
Arenediazoniové soli byly hlášeny jako alternativa k arylhalogenidům pro Sonogashirovu kopulační reakci. Chlorid zlata (I) byl použit jako kokatalyzátor v kombinaci s chloridem palladnatým při kondenzaci solí arenediazonia s koncovými alkyny, což je proces prováděný za přítomnosti bis-2,6-diisopropylfenyl dihydroimidazolium chloridu (IPr NHC) (5%mol.) In situ generovat komplex NHC-palladium a 2,6-di-terc-butyl-4-methylpyridin (DBMP) jako bázi v acetonitrilu jako rozpouštědlo při pokojové teplotě. Tato kopulace může být provedena počínaje aniliny vytvořením diazoniové soli s následnou in situ Sonogashirovou kopulací, kde jsou aniliny transformovány na diazoniovou sůl a dále převedeny na alkyn kopulací s fenylacetylenem.
Alkyny
K získání požadovaných disubstituovaných produktů s uspokojivými výtěžky lze použít různé aromatické alkyny. Alifatické alkyny jsou obecně méně reaktivní.
Základy
Vzhledem k zásadní úloze báze musí být specifické aminy přidány v přebytku nebo jako rozpouštědlo, aby reakce pokračovala. Bylo zjištěno, že sekundární aminy, jako je piperidin, morfolin nebo diisopropylamin zejména může efektivně a reverzibilně reagovat s trans - RPdX (PPh
3)
2komplexy nahrazením jednoho PPh
3ligand. Rovnovážná konstanta této reakce závisí na R, X, faktoru zásaditosti, a na sterické překážce aminu. Výsledkem je kompetice mezi aminem a alkynovou skupinou pro tuto výměnu ligandů, a proto se amin obecně přidává v přebytku, aby se podpořila preferenční substituce.
Variace reakce
Spojka Sonogashira bez mědi
Zatímco k reakci se přidává měděný kokatalyzátor ke zvýšení reaktivity, přítomnost mědi může vést k tvorbě alkynových dimerů. To vede k takzvané Glaserově kondenzační reakci, což je nežádoucí tvorba homocouplingových produktů acetylenových derivátů při oxidaci . V důsledku toho je při provádění Sonogashirovy reakce s měděným kokatalyzátorem nutné provést reakci v inertní atmosféře, aby se zabránilo nežádoucí dimerizaci. Variace reakce Sonogashira bez mědi byly vyvinuty, aby se zabránilo tvorbě homocouplingových produktů. Existují i jiné případy, kdy je třeba se použití mědi vyhnout, jako jsou kopulační reakce zahrnující substráty, které potenciální měděné ligandy, například porfyriny na volné bázi .
Inverzní spojka Sonogashira
Při inverzní Sonogashirově kondenzaci jsou reakčními složkami aryl nebo vinylová sloučenina a alkynylhalogenid.
Variace katalyzátoru
Stříbrná kokatalýza
V některých případech lze místo CuI pro spojky Sonogashira bez mědi použít stechiometrická množství oxidu stříbrného .
Niklové katalyzátory
Nedávno byla vyvinuta niklově katalyzovaná spojka Sonogashira, která umožňuje navázání neaktivovaných alkylhalogenidů na acetylen bez použití palladia, i když je stále zapotřebí měděný kokatalyzátor. Bylo také popsáno, že zlato může být použit jako heterogenního katalyzátoru, která byla prokázána ve kopulace fenylacetylenu a jodbenzen s Au / ceo 2 katalyzátoru. V tomto případě dochází ke katalýze heterogenně na nanočásticích Au, přičemž aktivním místem je Au (0). Bylo také zjištěno, selektivita na žádoucí příčné kopulačního produktu se zvyšuje nosičích, jako CEO 2 a La 2 O 3 . Kromě toho byly spojky Sonogashira katalyzované železem zkoumány jako relativně levné a netoxické alternativy k palladiu. Zde, FeCl 3 se navrhuje působit jako přechodového kovu jako katalyzátoru a Cs 2 CO 3 jako báze, a tak teoreticky probíhal palladia bez a bez mědi mechanismem.
| Sonogashirova reakce bez paladia katalyzovaná železem |
|---|
I když se ukázalo, že mechanismus bez mědi je životaschopný, pokusy začlenit různé výše uvedené přechodné kovy jako méně nákladné alternativy k palladiovým katalyzátorům ukázaly špatnou historii úspěchu v důsledku kontaminace reagencií stopovým množstvím palladia, což naznačuje že těchto teoretických cest je extrémně nepravděpodobné, ne -li nemožné, dosáhnout.
Studie ukázaly, že organické a anorganické výchozí materiály mohou také obsahovat dostatek ( úrovně ppb ) palladia pro kopulaci.
Kokatalýza zlata a palladia
Byla popsána vysoce účinná kombinovaná metodika zlata a palladia pro Sonogashirovu vazbu široké škály elektronicky a strukturně rozmanitých arylových a heteroarylhalogenidů. Ortogonální reaktivita těchto dvou kovů vykazuje při spojování Sonogashira vysokou selektivitu a extrémní toleranci funkční skupiny. Stručná mechanistická studie ukazuje, že meziprodukt zlato-acetylid vstupuje do katalytického cyklu palladia v transmetalačním kroku.
Dendrimerické palladiové komplexy
Problémy týkající se regenerace často nákladného katalyzátoru po tvorbě produktu představují vážnou nevýhodu pro aplikace homogenní katalýzy ve velkém měřítku. Struktury známé jako metallodendrimery kombinují výhody homogenních a heterogenních katalyzátorů, protože jsou rozpustné a dobře definované na molekulární úrovni, a přesto je lze získat vysrážením, ultrafiltrací nebo ultracentrifugací. Lze nalézt několik nedávných příkladů použití katalyzátorů dendritických palladiových komplexů pro Sonogashirovu reakci bez mědi. Bylo tedy použito několik generací polyamino dendritických katalyzátorů bidentátních fosfinpalladium (II) solubilizovaných v triethylaminu pro kondenzaci aryljodidů a bromidů při 25 až 120 ° C a arylchloridů, ale ve velmi nízkých výtěžcích. Dendrimerické katalyzátory lze obvykle izolovat jednoduchým srážením a filtrací a znovu použít až pětkrát, přičemž je pozorována snížená aktivita způsobená rozkladem dendrimeru a nikoli vyluhováním palladia. Tyto dendrimerické katalyzátory vykazovaly negativní dendritický účinek; to znamená, že účinnost katalyzátoru klesá s rostoucí generací dendrimeru. Recyklovatelný polymerní fosfinový ligand zobrazený níže se získává polymerací norathenového derivátu s otevřením kruhu a byl použit při reakci katalyzované měďou Sonogashirou methyl piodobenzoátu a fenylacetylenu za použití Pd (dba)
2· CHCl
3jako zdroj palladia. Navzdory regeneraci filtrací se polymerní katalytická aktivita v každém recyklačním experimentu snížila přibližně o 4-8%.
Dusíkaté ligandy
Pyridiny a pyrimidiny vykazovaly dobré komplexační vlastnosti pro palladium a byly použity při tvorbě katalyzátorů vhodných pro Sonogashirovy spojky. Níže uvedený komplex dipyrimidyl-palladia byl použit při kopulaci jodu, bromu a chlorbenzenu bez mědi s fenylacetylenem za použití N-butylaminu jako báze v rozpouštědle THF při 65 ° C. Kromě toho byly všechny strukturní rysy tohoto komplexu charakterizovány rozsáhlou rentgenovou analýzou, která ověřovala pozorovanou reaktivitu.
Nověji byl získán komplex dipyridylpalladia, který byl použit při kopulační reakci Sonogashira bez mědi aryljodidů a bromidů v N-methylpyrrolidinonu (NMP) za použití tetra-n-butylamoniumacetátu (TBAA) jako báze při pokojové teplotě. Tento komplex byl také použit pro kopulaci aryljodidů a bromidů v refluxující vodě jako rozpouštědle a za přítomnosti vzduchu, za použití pyrrolidinu jako báze a TBAB jako aditiva, ačkoli jeho účinnost byla vyšší u N-methylpyrrolidinonu (NMP) jako rozpouštědla.
N -heterocyklický karben (NHC) palladiové komplexy
N -heterocyklické karbeny (NHC) se staly jedním z nejdůležitějších ligandů při katalýze přechodových kovů. Úspěch normálních NHC je do značné míry přičítán jejich vynikajícím schopnostem darování σ ve srovnání s fosfiny, což je ještě větší u abnormálních protějšků NHC. NHC, které se používají jako ligandy v palladiových komplexech, významně přispěly ke stabilizaci a aktivaci předběžných katalyzátorů, a proto našly uplatnění v mnoha oblastech organokovové homogenní katalýzy, včetně spojek Sonogashira.
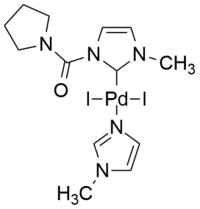
| Příklad komplexu odvozeného od palladia (II) s normálním ligandem NHC. | Účinný i PEPPSI katalyzátor pro reakci Cu bez Sonogashiry ve vodě. |
Zajímavé příklady abnormálních NHC jsou založeny na mezoionické struktuře 1,2,3-triazol-5-ylidenu. Účinný, kationtové katalyzátor na bázi palladia z PEPPSI typu, tj, i PEPPSI ( i nternal p yridine- e nhanced p recatalyst p reparačním y tabilization a i nitiation) bylo prokázáno, že účinně katalyzovat mědi bez Sonogashirovy reakce, ve vodě jako rozpouštědla pouze za aerobních podmínek za nepřítomnosti mědi, aminů, fosfinů a dalších přísad.
Aplikace v syntéze
Spojky Sonogashira se používají v široké škále syntetických reakcí, především díky jejich úspěchu při zajišťování následujících náročných transformací:
Alkynylační reakce
Spojení koncového alkynu a aromatického kruhu je klíčovou reakcí, když hovoříme o aplikacích Sonogashirovy reakce podporované mědí nebo bez mědi. Seznam případů, kde byla použita typická Sonogashirova reakce za použití arylhalogenidů, je velký a vybrat názorné příklady je obtížné. Nedávné použití této metodiky je ukázáno níže pro kondenzaci jodovaného fenylalaninu s koncovým alkynem odvozeným od d -biotinu za použití in situ generovaných druhů Pd (0) jako katalyzátoru, což umožnilo přípravu alkylenem napojeného derivátu fenylalaninu pro bioanalytické aplikace. Existují také příklady vazebných partnerů, kteří jsou oba navázáni na alylové pryskyřice, přičemž katalyzátor Pd (0) působí štěpení substrátů a následnou Sonogashirovu kopulaci v roztoku.
Přírodní produkty
Mnoho metabolitů nacházejících se v přírodě obsahuje alkynové nebo eninové skupiny, a proto Sonogashirova reakce našla v jejich syntézách časté využití. Několik nejnovějších a nejslibnějších aplikací této spojovací metodologie k celkové syntéze přírodních produktů používalo výhradně typickou reakci měď-kokatalyzovaná.
Příklad kondenzace aryljodidu na aryl acetylen lze vidět na reakci jodovaného alkoholu a tris (isopropyl) silylacetylenu, za vzniku alkinu, meziproduktu v celkové syntéze benzindenoazepinového alkaloidu bulgaraminu.
Existují i další nedávné příklady použití aryljodidů pro přípravu meziproduktů za typických podmínek Sonogashiry, které po cyklizaci poskytují přírodní produkty, jako je benzylisochinolin nebo indolové alkaloidy. Příkladem je syntéza benzylisochinolinových alkaloidů (+)-( S ) -laudanosin a (-)-( S ) -xylopinin. Syntéza těchto přírodních produktů zahrnovala použití křížové vazby Sonogashira k vytvoření uhlíkové páteře každé molekuly.
Enynes a enediynes
Část 1,3-enynu je důležitou strukturní jednotkou pro biologicky aktivní a přírodní sloučeniny. Může být odvozen z vinylových systémů a koncových acetylenů pomocí stereospecifického postupu s retencí konfigurace, jako je reakce Sonogashira. Vinyljodidy jsou nejreaktivnějšími vinylhalogenidy na oxidační adici Pd 0 , a jejich použití je proto nejčastější pro reakce křížové kopulace Sonogashira kvůli obvykle používaným mírnějším podmínkám. Některé příklady zahrnují:
- Vazba 2-jod-prop-2-enolu na širokou škálu acetylenů.
- Příprava alk-2-ynylbuta-1,3-dienů z křížové kopulace dijodidu a fenylacetylenu, jak je ukázáno níže.
Farmaceutický průmysl
Všestrannost reakce Sonogashira z ní činí široce používanou reakci při syntéze různých sloučenin. Jedna taková farmaceutická aplikace je v syntéze SIB-1508Y, který je běžněji známý jako Altinicline . Altinicline je agonista nikotinového acetylcholinového receptoru , který prokázal potenciál při léčbě Parkinsonovy choroby, Alzheimerovy choroby, Touretteova syndromu, schizofrenie a poruchy pozornosti s hyperaktivitou (ADHD). V roce 2008 prošel Altinicline klinickými zkouškami fáze II.
Křížovou kopulační reakci Sonogashira lze použít při syntéze derivátů imidazopyridinu.

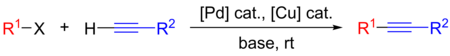
![Mechanismus reakce Sonogashira bez Cu. [13] [14]](https://upload.wikimedia.org/wikipedia/commons/thumb/9/90/Cu-free-mechanism.png/642px-Cu-free-mechanism.png)