Borohydrid sodný - Sodium borohydride

|
|||

|
|||
|
|
|||
| Jména | |||
|---|---|---|---|
|
Název IUPAC
Tetrahydridoboritan sodný (1–)
|
|||
|
Systematický název IUPAC
Boranuid sodný |
|||
| Identifikátory | |||
|
3D model ( JSmol )
|
|||
| ChEBI | |||
| ChemSpider | |||
| Informační karta ECHA |
100,037,262 |
||
| Číslo ES | |||
| 23167 | |||
| Pletivo | Sodík + borohydrid | ||
|
PubChem CID
|
|||
| Číslo RTECS | |||
| UNII | |||
| UN číslo | 1426 | ||
|
Řídicí panel CompTox ( EPA )
|
|||
|
|||
|
|||
| Vlastnosti | |||
| NaBH 4 | |||
| Molární hmotnost | 37,83 g / mol | ||
| Vzhled | bílé krystaly hygroskopické |
||
| Hustota | 1,07 g / cm 3 | ||
| Bod tání | 400 ° C (752 ° F; 673 K) (rozkládá se) | ||
| 550 g / l | |||
| Rozpustnost | rozpustný v kapalném amoniaku , aminech , pyridinu | ||
| Struktura | |||
| Kubický (NaCl), cF8 | |||
| Fm 3 m, č. 225 | |||
a = 0,6157 nm
|
|||
| Nebezpečí | |||
| H260 , H301 , H311 , H314 | |||
| P223 , P231 , P232 , P280 , P301 + 310 , P370 + 378 , P422 | |||
| NFPA 704 (ohnivý diamant) | |||
| Bod vzplanutí | 70 ° C (158 ° F; 343 K) | ||
| ca. 220 ° C (428 ° F; 493 K) | |||
| Výbušné limity | 3% | ||
| Smrtelná dávka nebo koncentrace (LD, LC): | |||
|
LD 50 ( střední dávka )
|
160 mg / kg (orálně - krysa) 230 mg / kg (dermálně - králík) |
||
| Související sloučeniny | |||
|
Jiné anionty
|
Kyanoborohydrid sodný Hydrid sodný Boritan sodný Borax Sodiumaluminiumhydrid |
||
|
Jiné kationty
|
Borohydrid lithný | ||
|
Související sloučeniny
|
Lithiumaluminiumhydrid triacetoxyborohydrid sodný |
||
|
Pokud není uvedeno jinak, jsou uvedeny údaje o materiálech v jejich standardním stavu (při 25 ° C [77 ° F], 100 kPa). |
|||
|
|
|||
| Reference Infoboxu | |||
Borohydrid sodný , také známý jako tetrahydridoboritanu sodného a tetrahydridoboritanu sodného , je anorganická sloučenina se vzorcem Na BH 4 . Tato bílá pevná látka, se kterou se obvykle setkáváme jako prášek, je redukční činidlo, které nachází uplatnění v chemii, a to jak v laboratoři, tak v průmyslovém měřítku. Byl testován jako předúprava na rozvlákňování dřeva, ale je příliš nákladný na to, aby byl komercializován. Sloučenina je rozpustná v alkoholech , určitých etherech a vodě, i když pomalu hydrolyzuje.
Sloučenina byla objevena ve 40. letech 20. století HI Schlesingerem , který vedl tým hledající těkavé sloučeniny uranu. Výsledky tohoto válečného výzkumu byly odtajněny a zveřejněny v roce 1953.
Vlastnosti
| Solventní | Rozpustnost (g / 100 ml) |
|---|---|
| MeOH | 13 |
| EtOH | 3.16 |
| Diglyme | 5.15 |
| Et 2 O | nerozpustný |
Borohydrid sodný je bílý až šedobílý mikrokrystalický prášek bez zápachu, který často vytváří hrudky. Může být čištěn rekrystalizací z teplého (50 ° C) diglymu . Borohydrid sodný je rozpustný v protických rozpouštědlech, jako je voda a nižší alkoholy. To také reaguje s těmito protická rozpouštědla produkovat H 2 ; tyto reakce jsou však poměrně pomalé. Úplný rozklad methanolového roztoku vyžaduje téměř 90 minut při 20 ° C. Rozkládá se v neutrálních nebo kyselých vodných roztocích, ale je stabilní při pH 14.
Struktura
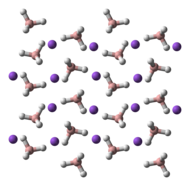
NaBH 4 je sůl, která se skládá z tetraedrických [BH 4 ] - aniontů. Je známo, že pevná látka existuje jako tři polymorfy : α , β a γ . Stabilní fáze při pokojové teplotě a tlaku je α -NaBH 4 , který je krychlový a přijímá NaCl -type strukturu, v Fm 3 m prostorové grupy . Při tlaku 6,3 GPa se struktura změní na tetragonální β- NaaBH 4 (vesmírná skupina P42 1 c ) a při 8,9 GPa se ortorombický y- NaaBH 4 (vesmírná skupina Pnma ) stane nejstabilnějším.
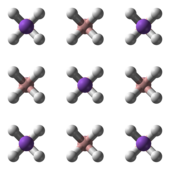 |
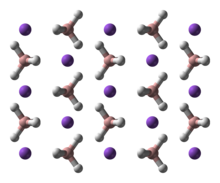 |
 |
|
|
Syntéza a manipulace
Pro komerční výrobu NaBH 4 jsou nejoblíbenější metodou Brown-Schlesingerův proces a Bayerův proces . V Brown-Schlesinger borohydrid proces sodný se průmyslově připravuje z hydridu sodného (vyrábí reakcí Na a H 2 ) a trimethylborátu při 250-270 ° C:
- B (OCH 3 ) 3 + 4 NaH → NaBH 4 + 3 NaOCH 3
Vyrábí se miliony kilogramů ročně, což výrazně převyšuje úroveň výroby jakéhokoli jiného hydridového redukčního činidla. Může být také vyroben z anorganických boritanů, včetně borosilikátového skla a boraxu (Na 2 B 4 O 7 ):
- Na 2 B 4 O 7 + 16 Na + 8 H 2 + 7 SiO 2 → 4 NaBH 4 + 7 Na 2 SiO 3
Hořčík je levnější redukční činidlo a lze jej v zásadě použít místo:
- 8 MgH 2 + Na 2 B 4 O 7 + Na 2 CO 3 → 4 NaBH 4 + 8 MgO + CO 2
a
- 2 MgH 2 + NaBO 2 → NaBH 4 + 2 MgO
Reaktivita
Organická syntéza
NaBH 4 snižuje mnoho organických karbonyly , v závislosti na přesných podmínkách. Nejtypičtěji se používá v laboratoři pro přeměnu ketonů a aldehydů na alkoholy. To účinně snižuje acylchloridy , anhydridy , a-hydroxy laktony , thioestery a iminy při teplotě místnosti nebo nižší. Redukuje estery pomalu a neúčinně s přebytečným činidlem a / nebo zvýšenými teplotami, zatímco karboxylové kyseliny a amidy nejsou redukovány vůbec. NaBH 4 reaguje s vodou a alkoholy, s vývojem plynného vodíku a vytvořením odpovídajícího boritanu, přičemž reakce se obzvláště rychle při nízkém pH.
Nicméně alkohol, často methanol nebo ethanol, je obecně rozpouštědlem volby pro redukci borohydridu sodného na ketony a aldehydy. Mechanismus redukce ketonů a aldehydů byl zkoumán kinetickými studiemi a na rozdíl od populárních vyobrazení v učebnicích tento mechanismus nezahrnuje čtyřčlenný přechodný stav, jako je hydroborace alkenu, nebo šestičlenný přechodný stav zahrnující molekulu alkoholu solventní. Aktivace vodíkových vazeb je nutná, protože v aprotickém rozpouštědle, jako je diglym, nedochází k redukci. Avšak rychlostní pořadí v alkoholu je 1,5, zatímco karbonylová sloučenina a borohydrid jsou oba prvního řádu, což naznačuje mechanismus složitější než ten, který zahrnuje šestičlenný přechodný stav, který zahrnuje pouze jednu molekulu alkoholu. Bylo navrženo, že dochází k simultánní aktivaci karbonylové sloučeniny a borohydridu prostřednictvím interakce s alkoholem a alkoxidovým iontem, a že reakce probíhá v otevřeném přechodovém stavu.
α, p-Nenasycené ketony mají tendenci být snížena o NaBH 4 v 1,4-smysl, když směsi jsou často tvořeny. Přídavek chloridu ceričitého zlepšuje selektivitu pro 1,2-redukci nenasycených ketonů ( Luche redukce ). α, p-nenasycené estery rovněž podstoupit 1,4-redukcí v přítomnosti NaBH 4 .
NaBH 4 -MeOH systém, vytvořený přidáním methanolu do borohydridem sodným v refluxujícím THF, snižuje estery na odpovídající alkoholy. Smícháním vody nebo alkoholu s borohydridem se část z ní převede na nestabilní ester hydridu, který je účinnější při redukci, ale redukční činidlo se nakonec spontánně rozloží na plynný vodík a boritany. Stejná reakce může také nastat intramolekulárně: α-ketoester se přemění na diol, protože vyrobený alkohol napadá borohydrid za vzniku esteru borohydridu, který pak redukuje sousední ester.
Reaktivita NaBH 4 může být zvýšena, nebo doplněny řadou sloučenin.
Oxidace
Oxidací jodem v tetrahydrofuranu se získá boran-tetrahydrofuran , který může redukovat karboxylové kyseliny.
Částečná oxidace borohydridu jodem poskytuje oktahydrotriborát :
- 3 BH 4 - + I 2 → B 3 H 8 - + 2 H 2 + 2 I -
Koordinační chemie
BH 4 - je ligand pro ionty kovů. Takové borohydridu komplexy jsou často připravovány působením NaBH 4 (nebo LIBH 4 ) na odpovídající halogenid kovu. Jedním příkladem je derivát titanocenu :
- 2 (C 5 H 5 ) 2 TiCl 2 + 4 NaBH 4 → 2 (C 5 H 5 ) 2 TiBH 4 + 4 NaCl + B 2 H 6 + H 2
Protonolýza a hydrolýza
V přítomnosti kovových katalyzátorů borohydrid sodný hydrolyzuje za uvolňování vodíku. S využitím této reaktivity byl borohydrid sodný použit v prototypech přímého borohydridového palivového článku .
- NaBH 4 + 2 H 2 O → NaBO 2 + 4 H 2 (ΔH <0)
Aplikace
Hlavní aplikací borohydridu sodného je výroba dithioničitanu sodného z oxidu siřičitého: Dithioničitan sodný se používá jako bělidlo pro dřevní buničinu a v barvivovém průmyslu.
Borohydrid sodný redukuje aldehydy a ketony za vzniku souvisejících alkoholů . Tato reakce se používá při výrobě různých antibiotik, včetně chloramfenikolu , dihydrostreptomycinu a thiofenikolu . Různé steroidy a vitamin A se připravují za použití borohydridu sodného v alespoň jednom kroku.
Borohydrid sodný byl považován za kandidáta na skladování vodíku v pevném stavu . Přestože nebylo dosaženo praktických teplot a tlaků pro skladování vodíku, v roce 2012 byla úspěšně použita nanostruktura borohydridu sodného typu jádro-obal pro skladování, uvolňování a reabsorpci vodíku za mírných podmínek.
Borohydrid sodný lze použít ke snížení lišivosti ve starých knihách a dokumentech. Toto ošetření by měl provádět pouze zkušený profesionální konzervátor / restaurátor, protože při nesprávném použití redukčního činidla, jako je například bělení a bublání papíru, může dojít k poškození papíru.
Bezpečnost
Borohydrid sodný je zdrojem vodíku nebo diboranu , které jsou hořlavé. Spontánní vznícení může vzniknout z roztoku borohydridu sodného v dimethylformamidu . Sypké roztoky borohydridu sodného se často připravují s přebytkem hydroxidu sodného, který je korozivní.
Viz také
Mnoho derivátů a analogů borohydridu sodného vykazuje modifikovanou reaktivitu v organické syntéze.
- Triacetoxyborohydrid sodný , mírnější redukční činidlo v důsledku přítomnosti více acetátu odvádějícího elektrony místo hydridu.
- Triethylborohydrid sodný , silnější redukční činidlo v důsledku přítomnosti ethylových skupin poskytujících elektrony místo hydridu.
- kyanoborohydrid sodný , mírnější redukční činidlo v důsledku přítomnosti více kyanidu odvádějícího elektrony místo hydridu. Užitečné pro redukční aminace.
- Lithiumborohydrid , silněji redukující činidlo.
- L-selektrid (lithium tri- sec- butylborohydrid), silněji redukující deriváty.
- Lithiumaluminiumhydrid , silněji redukující činidlo, schopné redukovat estery a amidy.