Ketene - Ketene
Ketenu je organická sloučenina ve tvaru R'R "C = C = O, kde R a R‘ jsou dva libovolné monovalentní chemické skupiny (nebo dvě oddělené substituční místa ve stejné molekule). Název může také odkazovat na konkrétní sloučeninu ethenon H
2C = C = O , nejjednodušší keten.
Ačkoli jsou velmi užitečné, většina ketenů je nestabilní . Pokud se používají jako činidla v chemickém postupu, jsou obvykle generovány v případě potřeby a spotřebovány, jakmile (nebo během) jsou vyrobeny.
Dějiny
Keteny byly poprvé studovány jako třídu Hermannem Staudingerem před rokem 1905.
Keteny byly systematicky zkoumány Hermannem Staudingerem v roce 1905 ve formě difenylketenu (konverze -chlorodifenylacetylchloridu se zinkem). Staudinger byl inspirován prvními příklady reaktivních organických meziproduktů a stabilních radikálů objevených Mosesem Gombergem v roce 1900 (sloučeniny s trifenylmethylovou skupinou).
Vlastnosti
Keteny jsou vysoce elektrofilní na atomu uhlíku spojeném s heteroatomem, vzhledem k jeho sp charakteru. Keten může být vytvořen s různým heteroatomem navázaným na atom uhlíku sp , jako je O , S nebo Se , respektive pojmenovaný keten , thioketen a selenoketen .
Ethenon , nejjednodušší keten , má různé experimentální délky pro každou z dvojných vazeb; vazba C = O je 1 160 Á a vazba C = C je 1 314 Á. Úhel mezi dvěma atomy H je 121,5 °, podobně jako teoreticky ideální úhel vytvořený v alkenech mezi atomem uhlíku sp 2 a substituenty H.
Keteny jsou nestabilní a nelze je skladovat. V nepřítomnosti nukleofilů, se kterými by reagoval, etenon dimerizuje za vzniku beta-laktonu , cyklického esteru . Pokud je keten disubstituován, je produktem dimerizace substituovaný cyklobutadion. U monosubstituovaných ketenů by dimerizace mohla poskytnout buď esterový nebo diketonový produkt.
Syntéza
Ethenon může být generován pyrolýzou (tepelným krakováním) acetonu :
- CH 3 −CO − CH 3 → CH 2 = C = O + CH 4
Tato reakce se nazývá Schmidlinova syntéza ketenu.
Další keteny mohou být připraveny z acylchloridy pomocí eliminační reakce , ve které HCl se ztrácí:
V této reakci báze, obvykle triethylamin , odstraní kyselý proton alfa na karbonylovou skupinu, což vyvolá tvorbu dvojné vazby uhlík-uhlík a ztrátu chloridového iontu:
Keteny mohou být také vytvořeny z a- diazoketonů podle Wolff přesmyku .
Dalším způsobem, jak vytvářet keteny, je rychlá vakuová termolýza (FVT) s 2- pyridylaminy . Plüg a Wentrup vyvinuli v roce 1997 metodu, která zlepšila reakce FVT za vzniku ketenů se stabilním FVT, který je citlivý na vlhkost, za mírných podmínek (480 ° C). N-pyridylaminy se připraví kondenzací s R- malonáty s N-amino ( pyriden ) a DCC jako rozpouštědlem.
Silnější Způsob přípravy keteny je karbonylace z kovových karbeny , a in situ reakci takto vyrobených vysoce reaktivních keteny s vhodným reakčním činidlem, jako jsou iminy , aminy nebo alkoholy . Tento způsob je účinný v jedné nádobě tandem protokol o karbonylaci α-diazocarbonyl sloučenin a různých N -tosylhydrazones katalyzovaná Co (II) - porfyrin metalloradicals vedoucí k tvorbě keteny, která následně reaguje s různými nukleofilními činidly a iminy za vzniku esterů , amidů a β ‐ laktamů . Tento systém má široký rozsah substrátů a lze jej použít na různé kombinace prekurzorů karbenu , nukleofilů a iminů .
Reakce a aplikace
Díky jejich kumulovaným dvojitým vazbám jsou keteny velmi reaktivní.
Tvorba esterů karboxylových kyselin
Reakcí s alkoholy , estery karboxylových kyselin se tvoří:
Tvorba anhydridů karboxylových kyselin
Keteny reagují s karboxylovými kyselinami za vzniku anhydridů karboxylových kyselin :
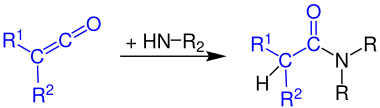
Tvorba amidů karboxylových kyselin
Keteny reagují s amoniakem na primární amidy :
Reakcí ketenů s primárními aminy vznikají sekundární amidy :
Keteny reagují se sekundárními aminy za vzniku terciárních amidů:
Hydrolýza
Reakcí s vodou vznikají z ketenů karboxylové kyseliny
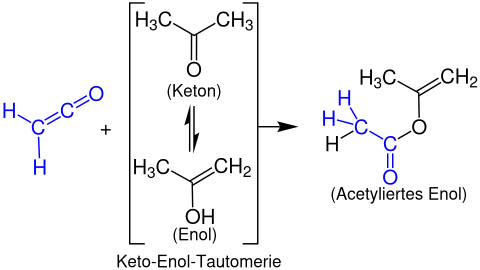
Tvorba esterů enolů
Enolestery jsou tvořeny z ketenů s enolisovatelnými karbonylovými sloučeninami . Následující příklad ukazuje reakci ethenonu s acetonem za vzniku propen-2- ylacetátu :
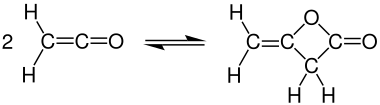
Dimerizace
Při pokojové teplotě se keten rychle dimerizuje na diketen , ale keten lze získat zpět zahřátím:
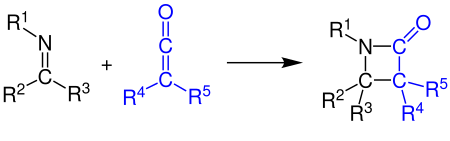
[2+2] -Cykloadice
Keteny mohou reagovat s alkeny , karbonylovými sloučeninami , karbodiimidy a iminy v [2+2] cykloadici . Příklad ukazuje syntézu beta-laktamu reakcí ketenu s iminem (viz Staudingerova syntéza ):
Aplikace
Keteny jsou obecně velmi reaktivní a účastní se různých cykloadic . Jedním důležitým procesem je dimerizace za vzniku propiolaktonů . Specifickým příkladem je dimerizace ketenu kyseliny stearové za vzniku alkylketenových dimerů , které jsou široce používány v papírenském průmyslu. AKD reagují s hydroxylovými skupinami na celulóze esterifikační reakcí.
Rovněž podstoupí [2+2] cykloadiční reakce s elektrony bohatými na alkyny za vzniku cyklobutenonů nebo karbonylových skupin za vzniku beta- laktonů . S iminy se tvoří beta-laktamy . Toto je Staudingerova syntéza , snadná cesta k této důležité třídě sloučenin. S acetonem reaguje keten za vzniku isopropenylacetátu .
Jako nukleofily se může přidat řada hydroxylových sloučenin za vzniku enolových nebo esterových produktů. Molekula vody se například snadno přidává ke ketenu za vzniku 1,1-dihydroxyethenu a anhydrid kyseliny octové se vyrábí reakcí kyseliny octové s ketenem. Reakce mezi dioly (HO − R − OH) a bis-keteny (O = C = CH − R′ − CH = C = O) poskytují polyestery s opakující se jednotkou (−O − R − O − CO − R'− CO).
Etylacetoacetát , důležitý výchozí materiál v organické syntéze, lze připravit za použití diketenu v reakci s ethanolem . Přímo tvoří ethyl -acetoacetát a výtěžek je vysoký, pokud se provádí za kontrolovaných okolností; tato metoda se proto používá průmyslově.
Viz také
Reference
externí odkazy
-
 Média související s Ketenes na Wikimedia Commons
Média související s Ketenes na Wikimedia Commons