Fosforylchlorid - Phosphoryl chloride
|
|||
|
|
|||

|
|||
| Jména | |||
|---|---|---|---|
|
Preferovaný název IUPAC
Fosforyl trichlorid |
|||
| Ostatní jména
Oxychlorid
fosforečný Trichlorfosfát trichlorid fosforečný |
|||
| Identifikátory | |||
|
3D model ( JSmol )
|
|||
| ČEBI | |||
| ChemSpider | |||
| Informační karta ECHA |
100,030,030 |
||
| Číslo ES | |||
|
PubChem CID
|
|||
| Číslo RTECS | |||
| UNII | |||
| UN číslo | 1810 | ||
|
CompTox Dashboard ( EPA )
|
|||
|
|||
|
|||
| Vlastnosti | |||
| POCl 3 | |||
| Molární hmotnost | 153,33 g/mol | ||
| Vzhled | bezbarvá kapalina, výpary ve vlhkém vzduchu | ||
| Zápach | štiplavý a zatuchlý | ||
| Hustota | 1,645 g / cm 3 , kapalný | ||
| Bod tání | 1,25 ° C (34,25 ° F; 274,40 K) | ||
| Bod varu | 105,8 ° C (222,4 ° F; 378,9 K) | ||
| Reaguje | |||
| Rozpustnost | vysoce rozpustný v benzenu , chloroformu , CS 2 , CCl 4 | ||
| Tlak páry | 40 mmHg (27 ° C) | ||
|
Index lomu ( n D )
|
1,460 | ||
| Struktura | |||
| čtyřboká | |||
| 2,54 D | |||
| Termochemie | |||
|
Tepelná kapacita ( C )
|
84,35 J/mol K | ||
|
Standardní entalpie
tvorby (Δ f H ⦵ 298 ) |
-568,4 kJ/mol | ||
| Nebezpečí | |||
| Bezpečnostní list |
Viz: datová stránka ICSC 0190 |
||
|
Klasifikace EU (DSD) (zastaralá)
|
Vysoce toxický ( T+ ) Zdraví škodlivý ( Xn ) Žíravý ( C ) |
||
| R-věty (zastaralé) | R14 , R22 , R26 , R35 , R48/23 | ||
| S-věty (zastaralé) | (S1/2) , S7/8 , S26 , S36/37/39 , S45 | ||
| NFPA 704 (ohnivý diamant) | |||
| Smrtelná dávka nebo koncentrace (LD, LC): | |||
|
LD 50 ( střední dávka )
|
36 mg/kg (krysa, orální) | ||
| NIOSH (limity expozice USA pro zdraví): | |||
|
PEL (přípustné)
|
žádný | ||
|
REL (doporučeno)
|
PEL 0,1 ppm (0,6 mg/m 3 ) ST 0,5 ppm (3 mg/m 3 ) | ||
|
IDLH (bezprostřední nebezpečí)
|
ND | ||
| Související sloučeniny | |||
|
Související sloučeniny
|
Thiofosforylchlorid Oxybromid fosforečný Chlorid fosforitý Pentachlorid fosforečný |
||
| Stránka doplňkových údajů | |||
|
Index lomu ( n ), dielektrická konstanta (ε r ) atd. |
|||
|
Termodynamická
data |
Fázové chování pevná látka – kapalina – plyn |
||
| UV , IR , NMR , MS | |||
|
Pokud není uvedeno jinak, jsou údaje uvedeny pro materiály ve standardním stavu (při 25 ° C [77 ° F], 100 kPa). |
|||
|
|
|||
| Reference na infobox | |||
Fosforylchlorid (běžně nazývaný oxychlorid fosforečný ) je bezbarvá kapalina vzorce P O Cl 3 . Ve vlhkém vzduchu hydrolyzuje a uvolňuje kyselinu fosforečnou a výpary chlorovodíku . Průmyslově se vyrábí ve velkém z chloridu fosforitého a kyslíku nebo oxidu fosforečného . Používá se hlavně k výrobě esterů fosfátů, jako je tricresylfosfát .
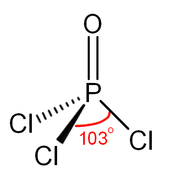
Struktura

Stejně jako fosfát má fosforylchlorid čtyřboký tvar. Obsahuje tři vazby P -Cl a jednu silnou dvojnou vazbu P = O s odhadovanou disociační energií vazby 533,5 kJ/mol. Na základě délky vazby a elektronegativity Schomakerovo-Stevensonovo pravidlo naznačuje, že forma dvojné vazby je dominantní, na rozdíl od případu POF 3 . Vazba P = O zahrnuje darování osamocených párových elektronů na kyslíkových p -orbitálech do kombinací protivazeb spojených s vazbami fosforu a chloru, čímž se vytvoří vazba π .

Fosforylchlorid existuje jako neutrální molekuly POCl 3 v pevném , kapalném a plynném stavu. To je na rozdíl od chloridu fosforečného , který existuje jako neutrální PCL 5 molekul v plynné a kapalné stavy, ale přijímá iontovou formu [PCI 4 + ] [PCI 6 - ] v pevném stavu. Průměrné délky vazeb v krystalové struktury z POCI 3 jsou 1,98 Á pro P-Cl a 1,46 Á pro P = O.
Fyzikální vlastnosti
S bodem tuhnutí 1 ° C a bodem varu 106 ° C je rozsah kapaliny POCl 3 spíše podobný vodě. Také jako voda se POCl 3 autoionizuje díky reverzibilní tvorbě POCl 2 + , Cl - .
Chemické vlastnosti
POCl 3 reaguje s vodou za vzniku chlorovodíku a kyseliny fosforečné :
- O = PCl 3 + 3 H 2 O → O = P (OH) 3 + 3 HCl
Meziprodukty při konverzi byly izolovány, včetně pyrofosforylchloridu , P 2 O 3 Cl 4 .
Po působení přebytečných alkoholů a fenolů poskytuje POCl 3 estery fosfátu :
- O = PCl 3 + 3 ROH → O = P (OR) 3 + 3 HCl
Takové reakce se často provádějí v přítomnosti akceptoru HCl, jako je pyridin nebo amin .
POCl 3 může také působit jako Lewisova báze , přičemž tvoří adukty s řadou Lewisových kyselin, jako je například chlorid titaničitý :
- Cl 3 PO + TiCl 4 → Cl 3 POTiCl 4
Chlorid hlinitý adukt (POCh 3 · AlCl 3 ) je poměrně stabilní, a proto POCI 3 může být použita pro odstranění AlCl 3 z reakční směsi, například na konci Friedel-Craftsovy reakce .
POCI 3 reaguje s bromovodíkem v přítomnosti Lewis-kyselých katalyzátorů pro výrobu POBr 3 .
Příprava
Fosforylchlorid lze připravit mnoha způsoby. Fosforylchlorid byl poprvé zaznamenán v roce 1847 francouzským chemikem Adolphem Wurtzem reakcí chloridu fosforečného s vodou.
Oxidací
Komerční způsob zahrnuje oxidaci chloridu fosforitého s kyslíkem :
- 2 PCl 3 + O 2 → 2 POCl 3
Alternativní metoda zahrnuje oxidaci chloridu fosforitého chlorečnanem draselným :
- 3 PCl 3 + KClO 3 → 3 POCl 3 + KCl
Oxygenace
Reakce chloridu fosforečného (PCl 5 ) s oxidem fosforečným (P 4 O 10 ).
- 6 PCl 5 + P 4 O 10 → 10 POCl 3
Reakce může být zjednodušena chlorací směsi PCL 3 a P 4 O 10 , generování PCL 5 in situ . Reakce chloridu fosforečného s kyselinou boritou nebo kyselinou šťavelovou :
Jiné metody
Redukce trikalciumfosfátu uhlíkem za přítomnosti plynného chloru :
- Ca 3 (PO 4 ) 2 + 6 C + 6 Cl 2 → 3 CaCl 2 + 6 CO + 2 POCl 3
Uvádí se také reakce oxidu fosforečného s chloridem sodným :
- 2 P 2 O 5 + 3 NaCl → 3 NaPO 3 + POCl 3 .
Využití
V jedné komerční aplikaci se fosforylchlorid používá při výrobě esterů fosfátu. Triarylphosphates, jako je trifenylfosfát a trikresylfosfát se používají jako látky zpomalující hoření a plastifikátory pro PVC . Trialkylfosfáty, jako je tributylfosfát, se používají jako rozpouštědla pro extrakci kapalina -kapalina v jaderném přepracování a jinde.
V polovodičovém průmyslu se POCl 3 používá jako bezpečný zdroj kapalného fosforu v difúzních procesech. Fosfor působí jako dopant sloužící k vytváření vrstev typu n na křemíkové destičce.
Jako činidlo
V laboratoři je POCl 3 reagentem při dehydrataci. Jeden příklad zahrnuje konverzi formamidů na izonitrily (isokyanidy); primární amidy na nitrily :
- RC (O) NH 2 + POCI 3 → RCN + "PO 2 Cl" + 2 HCl
V podobné reakci lze určité aryl-substituované amidy cyklizovat pomocí Bischler-Napieralského reakce .
Předpokládá se, že takové reakce probíhají přes imidoylchlorid . V určitých případech je konečným produktem imidoylchlorid. Například pyridony a pyrimidony lze převést na chlorderiváty, jako jsou 2-chlorpyridiny a 2-chlorpyrimidiny, které jsou meziprodukty ve farmaceutickém průmyslu.
V reakci Vilsmeier-Haack , POCI 3 reaguje s amidy vyrobit „Vilsmeierova činidla“, což je chlor- iminové soli, která následně reaguje s elektronově bohatých aromatických sloučenin k výrobě aromatických aldehydů po vodném zpracování.
Reference
Další čtení
- Handbook of Chemistry and Physics (71. ed.). Ann Arbor, MI: CRC Press. 1990.
- Stecher, Paul G. (1960). Merck Index of Chemicals and Drugs (7. vydání). Rahway: Merck & Co . OCLC 3653550 .
- Wade, LG, Jr. (2005). Organic Chemistry (6. vydání). Upper Saddle River, New Jersey: Pearson/Prentice Hall. p. 477.
- Walker, BJ (1972). Organofosforová chemie . Harmondsworth: Penguin. s. 101–116.
- „CDC - kapesní průvodce NIOSH k chemickým nebezpečím“ .