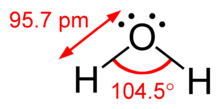
Teorie VSEPR - VSEPR theory
Valence shell elektronový pár teorie odpuzování , nebo VSEPR teorie ( / V ɛ s p ər , v ə s ɛ p ər / VESP -ər , və- září -ər ), je model, použitý v chemii předpovědět geometrii jednotlivých molekuly z počtu párů elektronů obklopujících jejich centrální atomy. Je také pojmenována podle teorie Gillespie-Nyholm podle jejích dvou hlavních vývojářů, Ronalda Gillespie a Ronalda Nyholma .
Předpokladem VSEPR je, že valenční elektronové páry obklopující atom mají tendenci se navzájem odpuzovat, a proto přijmou uspořádání, které toto odpuzování minimalizuje. To zase snižuje energii molekuly a zvyšuje její stabilitu, což určuje molekulární geometrii . Gillespie zdůraznil, že odpuzování elektronů a elektronů v důsledku Pauliho vylučovacího principu je důležitější při určování molekulární geometrie než elektrostatické odpuzování.
Pohledy teorie VSEPR jsou odvozeny z topologické analýzy elektronové hustoty molekul. Mezi takové metody kvantové chemické topologie (QCT) patří funkce lokalizace elektronů (ELF) a kvantová teorie atomů v molekulách (AIM nebo QTAIM). VSEPR tedy nesouvisí s metodami založenými na vlnových funkcích, jako je orbitální hybridizace v teorii valenčních vazeb .
Dějiny
Myšlenka korelace mezi molekulární geometrií a počtem valenčních elektronových párů (sdílené i nesdílené páry) byla původně navržena v roce 1939 Ryutarem Tsuchidou v Japonsku a byla nezávisle prezentována v Bakerské přednášce v roce 1940 Nevilem Sidgwickem a Herbertem Powellem z University of Oxford . V roce 1957 Ronald Gillespie a Ronald Sydney Nyholm z University College London vylepšili tento koncept na podrobnější teorii, která je schopna volit mezi různými alternativními geometriemi.
Přehled
Teorie VSEPR se používá k předpovědi uspořádání elektronových párů kolem centrálních atomů v molekulách, zejména jednoduchých a symetrických molekul. Centrální atom je v této teorii definován jako atom, který je vázán na dva nebo více dalších atomů, zatímco koncový atom je vázán pouze na jeden další atom. Například v molekule methylisokyanátu (H 3 C-N = C = O), jsou dva atomy uhlíku a jeden atom dusíku, jsou centrální atomy, a tři atomy vodíku a jeden atom kyslíku, jsou koncové atomy. Geometrie centrálních atomů a jejich nevázající se páry elektronů zase určují geometrii větší celé molekuly.
Počet párů elektronů ve valenčním obalu centrálního atomu je určen po nakreslení Lewisovy struktury molekuly a jejím rozbalením tak, aby se zobrazily všechny vazebné skupiny a osamocené páry elektronů. V teorii VSEPR je dvojná vazba nebo trojná vazba považována za jednoduchou vazebnou skupinu. Součet počtu atomů vázaných na centrální atom a počtu osamocených párů tvořených jeho nevázajícími valenčními elektrony je znám jako sterické číslo centrálního atomu.
Předpokládá se, že páry elektronů (nebo skupiny, jsou -li přítomny vícenásobné vazby) leží na povrchu koule se středem na centrálním atomu a mají tendenci zaujímat polohy, které minimalizují jejich vzájemné odpuzování maximalizací vzdálenosti mezi nimi. Počet párů elektronů (nebo skupin) tedy určuje celkovou geometrii, kterou přijmou. Například když jsou dva páry elektronů obklopující centrální atom, jejich vzájemné odpuzování je minimální, když leží na opačných pólech koule. Proto se předpokládá, že centrální atom přijme lineární geometrii. Pokud jsou kolem centrálního atomu 3 páry elektronů, jejich odpuzování je minimalizováno jejich umístěním na vrcholy rovnostranného trojúhelníku se středem na atomu. Proto je predikovaná geometrie trigonální . Stejně tak pro 4 páry elektronů je optimální uspořádání čtyřboké .
Jako nástroj při předpovídání geometrie přijaté s daným počtem elektronových párů často používaná fyzická demonstrace principu minimálního odpuzování elektronových párů využívá nafouknuté balónky. Manipulací získávají balónky mírný povrchový elektrostatický náboj, který má za následek přijetí zhruba stejných geometrií, když jsou svázány dohromady na svých stoncích jako odpovídající počet elektronových párů. Například, pět balónky svázané přijímat trigonální bipyramidálních geometrie, stejně tak jako pět vazebných párů PCL 5 molekuly.
Sterické číslo
Sterický počet centrálního atomu v molekule je počet atomů vázaných na tento centrální atom, nazývaný jeho koordinační číslo , plus počet osamocených párů valenčních elektronů na centrálním atomu. Například v molekule SF 4 má centrální atom síry čtyři ligandy ; koordinační číslo síry je čtyři. Kromě čtyř ligandů má síra v této molekule také jeden osamocený pár. Sterické číslo je tedy 4 + 1 = 5.
Stupeň odpudivosti
Celková geometrie je dále upřesněna rozlišováním mezi vazebnými a nevázanými elektronovými páry. Vazebný elektronový pár sdílený ve vazbě sigma se sousedním atomem leží dále od centrálního atomu než nevazující (osamělý) pár tohoto atomu, který je držen v blízkosti svého kladně nabitého jádra. Teorie VSEPR proto považuje odpuzování osamělého páru za větší než odpuzování spojovacím párem. Když má molekula 2 interakce s různým stupněm odpudivosti, teorie VSEPR předpovídá strukturu, kde osamělé páry zaujímají polohy, které jim umožní zažít menší odpuzování. Odpory osamělého páru – osamělého páru (lp – lp) jsou považovány za silnější než odpuzování osamělého páru (lp – bp), které jsou zase považovány za silnější než odpuzování spojujícího páru – páru (bp – bp), rozdíly, které pak vedou rozhodnutí o celkové geometrii, když jsou možné 2 nebo více neekvivalentních poloh. Například když 5 valenčních elektronových párů obklopí centrální atom, přijmou trigonální bipyramidovou molekulární geometrii se dvěma kolineárními axiálními polohami a třemi ekvatoriálními polohami. Elektronový pár v axiální poloze má tři blízké rovníkové sousedy vzdálené pouze 90 ° a čtvrtý mnohem dále při 180 °, zatímco ekvatoriální elektronový pár má pouze dva sousední páry při 90 ° a dva při 120 °. Odraz od blízkých sousedů při 90 ° je důležitější, takže osové polohy zažívají větší odpuzování než rovníkové polohy; proto, když existují osamělé páry, mají tendenci zaujímat rovníkové polohy, jak je znázorněno na diagramech následující části pro sterické číslo pět.
Rozdíl mezi osamělými páry a spojovacími páry lze také použít k racionalizaci odchylek od idealizovaných geometrií. Například, H 2 O molekula má čtyři dvojice elektronů ve své valence skořápky: dva osamocené páry a dva páry obligací. Čtyři páry elektronů jsou rozloženy tak, aby směřovaly zhruba k vrcholům čtyřstěnu. Úhel vazby mezi oběma vazbami O – H je však pouze 104,5 °, spíše než 109,5 ° pravidelného čtyřstěnu, protože dva osamocené páry (jejichž obaly hustoty nebo pravděpodobnosti leží blíže k jádru kyslíku) vyvíjejí větší vzájemné odpuzování než dva páry vazeb.
Vazba vyššího řádu vazby také vykazuje větší odpudivost, protože elektrony elektronové vazby pí přispívají. Například v isobutylenu je (H 3 C) 2 C = CH 2 úhel H 3 C − C = C (124 °) větší než úhel H 3 C − C − CH 3 (111,5 °). V uhličitanovém iontu však CO2-
3, všechny tři C -O vazby jsou ekvivalentní s úhly 120 ° kvůli rezonanci .
Metoda AX
Při aplikaci teorie VSEPR se běžně používá „metoda AX“ počítání elektronů. Elektronové páry kolem centrálního atomu jsou reprezentovány vzorcem AX n E m , kde A představuje centrální atom a má vždy implikovaný dolní index. Každý X představuje ligand (atom vázaný na A). Každý E představuje osamocený pár elektronů na centrálním atomu. Celkový počet X a E je znám jako sterické číslo. Například v molekule AX 3 E 2 má atom A sterické číslo 5.
Pokud atomy substituentu (X) nejsou všechny stejné, geometrie je stále přibližně platná, ale úhly vazby se mohou mírně lišit od těch, kde jsou všechny vnější atomy stejné. Například uhlíky s dvojnou vazbou v alkenech jako C 2 H 4 jsou AX 3 E 0 , ale úhly vazby nejsou všechny přesně 120 °. Podobně SOCl 2 je AX 3 E 1 , ale protože X substituenty nejsou identické, úhly X – A – X nejsou všechny stejné.
Na základě sterického počtu a distribuce X s a E s, teorie VSEPR dělá předpovědi v následujících tabulkách.
Prvky hlavní skupiny
Pro prvky hlavní skupiny existují stereochemicky aktivní osamělé páry E, jejichž počet se může pohybovat mezi 0 až 3. Všimněte si, že geometrie jsou pojmenovány pouze podle atomových poloh a ne podle elektronového uspořádání. Například popis AX 2 E 1 jako ohnuté molekuly znamená, že tři atomy AX 2 nejsou v jedné přímce, ačkoli osamocený pár pomáhá určit geometrii.
| Sterické číslo |
Molekulární geometrie 0 osamocených párů |
Molekulární geometrie 1 osamělý pár |
Molekulární geometrie 2 osamocené páry |
Molekulární geometrie 3 osamocené páry |
|---|---|---|---|---|
| 2 |
|
|||
| 3 |
 |
 |
||
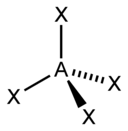
| 4 |
 |
 |
 |
|
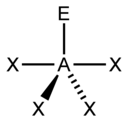
| 5 |
 |
 |
 |
 |
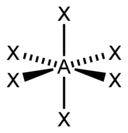
| 6 |
 |
 |
 |
|
| 7 |
 |
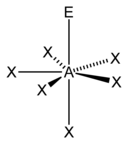 |
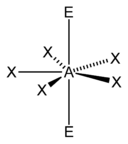 |
|
| 8 |
|
|
Typ molekuly |
Tvar | Elektronové uspořádání včetně osamocených párů, znázorněno bledě žlutou barvou |
Geometrie bez osamocených párů |
Příklady |
|---|---|---|---|---|
| AX 2 E 0 | Lineární |
|
|
BeCl 2 , CO 2 |
| AX 2 E 1 | Ohnutý |

|

|
NE- 2, SO 2 , O 3 , CCl 2 |
| AX 2 E 2 | Ohnutý |
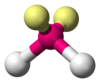
|

|
H 2 O , OF 2 |
| AX 2 E 3 | Lineární |

|
|
XeF 2 , I- 3, XeCl 2 |
| AX 3 E 0 | Trigonální planární |

|

|
BF 3 , CO2- 3, NE- 3, SO 3 |
| AX 3 E 1 | Trigonální pyramidální |

|

|
NH 3 , PCl 3 |
| AX 3 E 2 | Ve tvaru T. |

|

|
ClF 3 , BrF 3 |
| AX 4 E 0 | Čtyřboká |
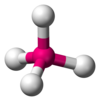
|

|
CH 4 , PO3- 4, SO2- 4, ClO- 4, XeO 4 |
| AX 4 E 1 | Houpačka nebo disphenoidální |

|
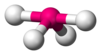
|
SF 4 |
| AX 4 E 2 | Čtvercový rovinný |

|

|
XeF 4 |
| AX 5 E 0 | Trigonální bipyramidové |

|

|
PCl 5 |
| AX 5 E 1 | Čtvercové pyramidální |
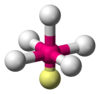
|

|
CLF 5 , Rámec 5 , XeOF 4 |
| AX 5 E 2 | Pětiúhelníkový rovinný |

|

|
XeF- 5 |
| AX 6 E 0 | Octahedral |
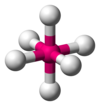
|

|
SF 6 |
| AX 6 E 1 | Pentagonální pyramidální |

|

|
XeOF- 5, IOF2- 5 |
| AX 7 E 0 | Pětiúhelníkový bipyramidový |
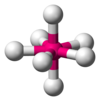
|

|
IF 7 |
| AX 8 E 0 | Náměstí antiprismatické |

|

|
LI- 8 |
Přechodové kovy (Kepertův model)
Osamělé páry na atomech přechodných kovů jsou obvykle stereochemicky neaktivní, což znamená, že jejich přítomnost nemění molekulární geometrii. Například hexaaquo komplexy M (H 2 O) 6 jsou všechny oktaedrické pro M = V 3+ , Mn 3+ , Co 3+ , Ni 2+ a Zn 2+ , a to navzdory skutečnosti, že elektronické konfigurace centrálního kovu ion jsou d 2 , d 4 , d 6 , d 8 a d 10 , resp. Kepertův model ignoruje všechny osamocené páry na atomech přechodových kovů, takže geometrie kolem všech takových atomů odpovídá geometrii VSEPR pro AX n s 0 osamocenými páry E. To se často píše ML n , kde M = kov a L = ligand. Kepertův model předpovídá následující geometrie pro koordinační čísla 2 až 9:
Typ molekuly |
Tvar | Geometrie | Příklady |
|---|---|---|---|
| AX 2 | Lineární |
|
HgCl 2 |
| AX 3 | Trigonální planární |

|
|
| AX 4 | Čtyřboká |

|
NiCl2- 4 |
| AX 5 | Trigonální bipyramidové |

|
Fe (CO) 5 |
| Čtvercové pyramidální |

|
MnCl 5 2− | |
| AX 6 | Octahedral |

|
WCl 6 |
| AX 7 | Pětiúhelníkový bipyramidový |

|
ZrF3- 7 |
| Uzávěr oktaedrický |

|
MF- 7 |
|
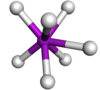
| Omezené trigonální prizmatické |
|
TaF2- 7 |
|
| AX 8 | Náměstí antiprismatické |

|
ReF- 8 |
| Dodekedrální |

|
Mo (CN)4 8 |
|
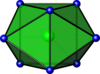
| Postižený trigonální prizmatický |
|
ZrF4 8 |
|
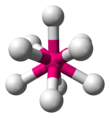
| AX 9 | Odtržený trigonální prizmatický |
|
ReH2- 9 |
| Uzavřené čtvercové antiprismatické |

|
Příklady
Methan molekula (CH 4 ) je čtyřboký, protože tam jsou čtyři páry elektronů. Čtyři atomy vodíku jsou umístěny ve vrcholech čtyřstěnu a úhel vazby je cos −1 ( - 1 / 3 ) ≈ 109 ° 28 ′. Toto je označováno jako typ molekuly AX 4 . Jak bylo uvedeno výše, A představuje centrální atom a X představuje vnější atom.
Amoniaku molekula (NH 3 ) má tři páry elektronů zapojených do lepení, ale je volný elektronový pár na atomu dusíku. Není spojen s jiným atomem; odpuzováním však ovlivňuje celkový tvar. Stejně jako v metanu výše existují čtyři oblasti elektronové hustoty. Celková orientace oblastí elektronové hustoty je proto čtyřboká. Na druhé straně existují pouze tři vnější atomy. To se označuje jako AX 3 typu E molekuly, protože volný pár je reprezentován definice E. Podle molekulární tvar nebo geometrii popisuje geometrické uspořádání pouze atomových jader, což je trigonální-pyramidový pro NH 3 .
Sterická čísla 7 a vyšší jsou možná, ale jsou méně běžná. Sterický počet 7 se vyskytuje v jodovém heptafluoridu (IF 7 ); základní geometrie pro sterický počet 7 je pětiúhelníkový bipyramidový. Nejběžnější geometrií pro sterický počet 8 je čtvercová antiprismatická geometrie. Mezi příklady patří octacyanomolybdate ( Mo (CN)4
8) a oktafluorozirkonát ( ZrF4
8) anionty. Nonahydridorhenátový ion ( ReH2-
9) v nonahydridorhenátu draselném je vzácný příklad sloučeniny se sterickým číslem 9, která má trojúhelníkovou trigonální prizmatickou geometrii.
Možné geometrie pro sterická čísla 10, 11, 12 nebo 14 jsou bicapped square antiprismatic (nebo bicapped dodecadeltahedral ), octadecahedral , icosahedral a bicapped hexagonal antiprismatic , resp. Neexistují žádné sloučeniny se sterickými čísly s tak vysokým obsahem monodentátních ligandů a sloučeniny zahrnující víceidentní ligandy lze často analyzovat jednodušeji jako komplexy s nižšími sterickými čísly, když jsou některé víceidentní ligandy považovány za jednotku.
Výjimky
Existují skupiny sloučenin, kde VSEPR nedokáže předpovědět správnou geometrii.
Některé molekuly AX 2 E 0
Tvary těžších analogů alkinu prvku skupiny 14 (RM≡MR, kde M = Si, Ge, Sn nebo Pb) byly vypočteny tak, aby byly ohnuty.
Některé molekuly AX 2 E 2
Jeden příklad AX 2 E 2 geometrie je molekulární oxid lithný Li 2 O, lineární spíše než ohnutý struktura, která je připisována svých vazeb je v podstatě iontové a silný lithium-lithium odpuzování, že výsledky. Dalším příkladem je O (SiH 3 ) 2 s úhlem Si – O – Si 144,1 °, což je srovnatelné s úhly v Cl 2 O (110,9 °), (CH 3 ) 2 O (111,7 °) a N (CH 3 ) 3 (110,9 °). Gillespie a Robinson racionalizují úhel vazby Si – O – Si na základě pozorované schopnosti osamoceného páru ligandu nejvíce odpuzovat jiné páry elektronů, když je elektronegativita ligandu větší nebo stejná jako u centrálního atomu. V O (SiH 3 ) 2 je centrální atom více elektronegativní a osamocené páry jsou méně lokalizované a slabě odpudivé. Větší úhel vazby Si – O – Si vyplývá z tohoto a silného odpuzování ligand -ligand relativně velkým ligandem -SiH 3 . Burford et al prostřednictvím rentgenových difrakčních studií prokázali, že Cl 3 Al – O – PCl 3 má lineární úhel vazby Al – O – P, a je tedy molekulou, která není VSEPR.
Některé molekuly AX 6 E 1 a AX 8 E 1

Některé molekuly AX 6 E 1 , např. Hexenfluorid xenonu (XeF 6 ) a anionty Te (IV) a Bi (III), TeCl2-
6, TeBr2-
6, BiCl3
6, BiBr3
6a BiI3
6, jsou oktaedry, spíše než pětiúhelníkové pyramidy, a osamělý pár neovlivňuje geometrii do míry předpovídané VSEPR. Podobně ion oktafluoroxenátu ( XeF2-
8) v nitrosonium oktafluoroxenátu (VI) je čtvercový antiprism a ne narušený trigonální hranol (jak předpovídala teorie VSEPR pro molekulu AX 8 E 1 ), přestože má osamocený pár. Jedna racionalizace spočívá v tom, že sterické shlukování ligandů poskytuje malý nebo žádný prostor pro nevázaný osamocený pár; další racionalizace je efekt inertního páru .
Čtvercové planární přechodové kovové komplexy
Kepertův model předpovídá, že molekuly přechodových kovů AX 4 mají čtyřboký tvar a nedokáže vysvětlit tvorbu čtvercových rovinných komplexů. Většina takových komplexů vykazuje ad 8 konfiguraci jako u tetrachlorproplatinátu ( PtCl2-
4) ion. Vysvětlení tvaru čtvercových rovinných komplexů zahrnuje elektronické efekty a vyžaduje použití teorie krystalového pole .
Komplexy se silným d-příspěvkem

Některé komplexy přechodových kovů s nízkým počtem elektronů d mají neobvyklé geometrie, které lze připsat interakci d subshell bonding Interaction. Gillespie zjistil, že tato interakce vytváří spojovací páry, které také zabírají příslušné antipodální body (proti ligandu) sféry. Tento jev je elektronický efekt vyplývající z dvojúhelníkového tvaru podkladových hybridních orbitálů sd x . Odpudení těchto obousměrných spojovacích párů vede k jiné sadě tvarů.
| Typ molekuly | Tvar | Geometrie | Příklady |
|---|---|---|---|
| AX 2 | Ohnutý |

|
VO+ 2 |
| AX 3 | Trigonální pyramidální |

|
CrO 3 |
| AX 4 | Čtyřboká |

|
TiCl 4 |
| AX 5 | Čtvercové pyramidální |

|
Ta (CH 3 ) 5 |
| AX 6 | C 3v Trigonální prizmatický |

|
W (CH 3 ) 6 |
Struktury triatomických halogenidů těžších členů skupiny 2 v plynné fázi (tj. Halogenidy vápníku, stroncia a barya, MX 2 ) nejsou lineární, jak se předpokládalo, ale jsou ohnuté (přibližné úhly X – M – X: CaF 2 (145 °; SrF 2 , 120 °; BaF 2 , 108 °; SrCl 2 , 130 °; BaCl 2 , 115 °; BaBr 2 , 115 °; BaI 2 , 105 °). Gillespie navrhl, že je to také způsobeno vazebnou interakcí ligandů s d subshell kovového atomu, což ovlivňuje molekulární geometrii.
Super těžké prvky
Předpokládá se, že relativistické efekty na elektronové orbitaly supertěžkých prvků ovlivní molekulární geometrii některých sloučenin. Například elektrony 6d 5/2 v nihoniu hrají nečekaně silnou roli ve vazbě, takže NhF 3 by měl předpokládat geometrii ve tvaru T namísto trigonální planární geometrie, jako je její lehčí kongener BF 3 . Naproti tomu se předpokládá extra stabilita 7p 1/2 elektronů v tennessinu, aby se TsF 3 stal trigonálním planárním, na rozdíl od geometrie ve tvaru T pozorované pro IF 3 a předpovídané pro At F 3 ; podobně Og F 4 by měl mít čtyřstěnnou geometrii, zatímco XeF 4 má čtvercovou planární geometrii a Rn F 4 se předpovídá, že bude mít stejnou.
Molekuly lichých elektronů
Teorii VSEPR lze rozšířit na molekuly s lichým počtem elektronů tak, že s nepárovým elektronem budeme zacházet jako s „polovičním elektronovým párem“ - například Gillespie a Nyholm navrhli, že snížení úhlu vazby v sérii NO+
2(180 °), NO 2 (134 °), NO-
2(115 °) naznačuje, že daná sada párů vazebných elektronů působí slabším odpuzováním na jeden nevazebný elektron než na pár nevázajících elektronů. Ve skutečnosti považovali oxid dusičitý za molekulu AX 2 E 0,5 s geometrií mezi NO+
2a NE-
2. Podobně je oxid chloričitý (ClO 2 ) molekulou AX 2 E 1,5 s geometrickým meziproduktem mezi ClO+
2a ClO-
2.
Konečně, methylovou skupinu (CH 3 ), se předpokládá, že trigonální pyramidální jako methyl aniontu ( CH-
3), ale s větším úhlem vazby (jako v trigonálním planárním methylovém kationtu ( CH+
3)). V tomto případě však předpověď VSEPR není tak docela pravdivá, protože CH 3 je ve skutečnosti planární, i když jeho zkreslení na pyramidovou geometrii vyžaduje velmi málo energie.
Viz také
- The Valence Bond Theory (VBT)
- Molekulární orbitální teorie (MOT)
- Bentovo pravidlo (účinek elektronegativity ligandu)
- Lineární kombinace atomových orbitálů
- Molekulární geometrie
- Molekulární modelování
- Software pro molekulární modelování
- Thomsonův problém
- Vzorec valenční interakce
Reference
Další čtení
- Lagowski, JJ, ed. (2004). Chemie: Základy a aplikace . 3 . New York: Macmillan. s. 99–104 . ISBN 978-0-02-865721-9.
externí odkazy
- VSEPR AR - 3D vizualizace teorie VSEPR s aplikací rozšířené reality
- 3D Chem - chemie, struktury a 3D molekuly
- IUMSC - Centrum molekulární struktury Indiana University