Polonium - Polonium
 | |||||||||||||||||||||||||
| Polonium | |||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Výslovnost |
/ P ə l oʊ n i ə m / ( pə- LOH -nee-əm ) |
||||||||||||||||||||||||
| Allotropes | α, β | ||||||||||||||||||||||||
| Vzhled | stříbřitý | ||||||||||||||||||||||||
| Hromadné číslo | [209] | ||||||||||||||||||||||||
| Polonium v periodické tabulce | |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| Atomové číslo ( Z ) | 84 | ||||||||||||||||||||||||
| Skupina | skupina 16 (chalkogeny) | ||||||||||||||||||||||||
| Doba | období 6 | ||||||||||||||||||||||||
| Blok | p-blok | ||||||||||||||||||||||||
| Konfigurace elektronů | [ Xe ] 4f 14 5d 10 6s 2 6p 4 | ||||||||||||||||||||||||
| Elektrony na skořápku | 2, 8, 18, 32, 18, 6 | ||||||||||||||||||||||||
| Fyzikální vlastnosti | |||||||||||||||||||||||||
| Fáze na STP | pevný | ||||||||||||||||||||||||
| Bod tání | 527 K (254 ° C, 489 ° F) | ||||||||||||||||||||||||
| Bod varu | 1235 K (962 ° C, 1764 ° F) | ||||||||||||||||||||||||
| Hustota (blízko rt ) | alfa: 9,196 g / cm 3 beta: 9,398 g / cm 3 |
||||||||||||||||||||||||
| Teplo fúze | ca. 13 kJ/mol | ||||||||||||||||||||||||
| Teplo odpařování | 102,91 kJ/mol | ||||||||||||||||||||||||
| Molární tepelná kapacita | 26,4 J/(mol · K) | ||||||||||||||||||||||||
Tlak páry
| |||||||||||||||||||||||||
| Atomové vlastnosti | |||||||||||||||||||||||||
| Oxidační stavy | -2 , +2 , +4 , +5, +6 ( amfoterní oxid) | ||||||||||||||||||||||||
| Elektronegativita | Paulingova stupnice: 2,0 | ||||||||||||||||||||||||
| Ionizační energie | |||||||||||||||||||||||||
| Atomový poloměr | empirické: 168 hod | ||||||||||||||||||||||||
| Kovalentní poloměr | 140 ± 16 hodin | ||||||||||||||||||||||||
| Van der Waalsův poloměr | 197 hodin | ||||||||||||||||||||||||
| Spektrální linie polonia | |||||||||||||||||||||||||
| Další vlastnosti | |||||||||||||||||||||||||
| Přirozený výskyt | z rozkladu | ||||||||||||||||||||||||
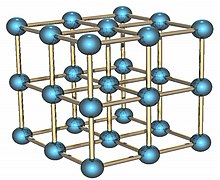
| Krystalická struktura | krychlový
α-Po |
||||||||||||||||||||||||
| Krystalická struktura | rhombohedral
β-Po |
||||||||||||||||||||||||
| Teplotní roztažnost | 23,5 µm/(m⋅K) (při 25 ° C) | ||||||||||||||||||||||||
| Tepelná vodivost | 20 W/(m⋅K) (?) | ||||||||||||||||||||||||
| Elektrický odpor | α: 0,40 µΩ⋅m (při 0 ° C) | ||||||||||||||||||||||||
| Magnetické uspořádání | nemagnetický | ||||||||||||||||||||||||
| Číslo CAS | 7440-08-6 | ||||||||||||||||||||||||
| Dějiny | |||||||||||||||||||||||||
| Pojmenování | po Polonia , latina pro Polsko , vlast Marie Curie | ||||||||||||||||||||||||
| Objev | Pierre a Marie Curie (1898) | ||||||||||||||||||||||||
| První izolace | Willy Marckwald (1902) | ||||||||||||||||||||||||
| Hlavní izotopy polonia | |||||||||||||||||||||||||
| |||||||||||||||||||||||||
Polonium je chemický prvek se symbolem Po a atomovým číslem 84. Polonium je chalkogen . Polonium je vzácný a vysoce radioaktivní kov bez stabilních izotopů , je chemicky podobný selenu a teluru , ačkoli jeho kovový charakter se podobá horizontálním sousedům v periodické tabulce : thallium , olovo a vizmut . Vzhledem ke krátkému poločasu rozpadu všech jeho izotopů je jeho přirozený výskyt omezen na drobné stopy letmého polonia-210 (s poločasem rozpadu 138 dní) v uranových rudách , protože je předposlední dcerou přírodního uranu- 238 . Ačkoli existují izotopy o něco delší životnosti, jejich výroba je mnohem obtížnější. Dnes je polonium se obvykle vyrábí v miligram množství podle neutronového záření z bismutu . Kvůli své intenzivní radioaktivitě, která má za následek radiolýzu chemických vazeb a radioaktivní samovolné zahřívání, byla její chemie většinou zkoumána pouze ve stopovém měřítku.
Polonium objevili v červenci 1898 Marie a Pierre Curieovi , když bylo extrahováno ze smoliny uranové rudy a identifikovalo se pouze podle silné radioaktivity: byl to první prvek, který byl takto objeven. Polonium bylo pojmenováno podle vlasti Polska Marie Curie . Polonium má jen málo aplikací a ty souvisejí s jeho radioaktivitou: ohřívače ve vesmírných sondách , antistatická zařízení , zdroje neutronů a alfa částic a jed . Je to pro člověka extrémně nebezpečné.
Charakteristika
210 Po je alfa zářič, který má poločas rozpadu 138,4 dní; rozpadá se přímo na svůj stabilní dceřiný izotop , 206 Pb . Miligram (5 curies ) 210 Po emituje asi tolik alfa částic za sekundu jako 5 gramů 226 Ra . Několik curies (1 curie se rovná 37 gigabecquerelům , 1 Ci = 37 GBq) 210 Po vyzařuje modrou záři, která je způsobena ionizací okolního vzduchu.
Přibližně jedna ze 100 000 emisí alfa způsobí v jádru excitaci, která pak vyústí v emisi gama záření s maximální energií 803 keV.
Solid state forma
Polonium je radioaktivní prvek, který existuje ve dvou kovových alotropech . Alfa forma je jediným známým příkladem jednoduché krychlové krystalové struktury na bázi jednoho atomu na STP s délkou okraje 335,2 pikometrů ; beta forma je kosočtverečná . Struktura polonia byla charakterizována rentgenovou difrakcí a elektronovou difrakcí .
210 Po (společně s 238 Pu ) má schopnost snadno se přenášet vzduchem : pokud se vzorek zahřeje na vzduchu na 55 ° C (131 ° F), 50% z něj se odpaří za 45 hodin za vzniku diatomických molekul Po 2 , přestože teplota tání polonia je 254 ° C (489 ° F) a jeho bod varu je 962 ° C (1764 ° F). Existuje více než jedna hypotéza, jak to polonium dělá; Jedním z návrhů je, že alfa shluky atomů polonia jsou odloučeny rozpadem alfa.
Chemie
Chemie polonia je podobná jako u teluru , i když díky svému kovovému charakteru také vykazuje určité podobnosti s jeho sousedním bismutem . Polonium se snadno rozpouští ve zředěných kyselinách, ale je jen málo rozpustné v zásadách . Roztoky polonia jsou nejprve zbarveny do růžova ionty Po 2+ , ale pak rychle zžloutnou, protože alfa záření z polonia ionizuje rozpouštědlo a převádí Po 2+ na Po 4+ . Jelikož polonium také po rozpadu emituje alfa-částice, je tento proces doprovázen bubláním a emisí tepla a světla skleněným zbožím v důsledku absorbovaných alfa částic; v důsledku toho jsou roztoky polonia těkavé a pokud nejsou uzavřeny, odpaří se během několika dní. Při pH asi 1, polonium ionty se snadno hydrolyzují a v komplexu s kyselinami, jako je kyselina šťavelová , kyselina citrónová a kyselina vinná .
Sloučeniny
Polonium nemá žádné běžné sloučeniny a téměř všechny jeho sloučeniny jsou vytvářeny synteticky; více než 50 z nich je známo. Nejstabilnější třídou sloučenin polonia jsou polonidy , které se připravují přímou reakcí dvou prvků. Na 2 Po má antifluorite strukturu, polonides z Ca , Ba , Hg , Pb a lanthanoidů tvoří mřížku NaCl, Bepo a CdPo mají wurtzite a MgPo nikl arsenid struktura. Většina polonidů se rozkládá po zahřátí na přibližně 600 ° C, kromě HgPo, který se rozkládá při ~ 300 ° C, a lanthanoidových polonidů, které se nerozkládají, ale tají při teplotách nad 1000 ° C. Například PrPo taje při 1250 ° C a TmPo při 2200 ° C. PbPo je jednou z mála přirozeně se vyskytujících sloučenin polonia, protože polonium alfa se rozpadá za vzniku olova .
Poloniumhydrid ( PoH
2) je těkavá kapalina při pokojové teplotě náchylná k disociaci; je tepelně nestabilní. Voda je jediným dalším známým vodíkovým chalkogenidem, který je při pokojové teplotě kapalný; je to však způsobeno vodíkovými vazbami. Tyto tři oxidy, PoO , PoO 2 a PoO 3 , jsou produkty oxidace polonia.
Halogenidy struktury PoX 2 , PoX 4 a PoF 6 jsou známy. Jsou rozpustné v odpovídajících halogenovodících, tj. PoCl X v HCl, PoBr X v HBr a PoI 4 v HI. Polonium dihalogenidy jsou tvořeny přímou reakcí prvků nebo redukcí POCI 4 SO 2, a s PoBr 4 s H 2 S při teplotě místnosti. Tetrahalogenidy lze získat reakcí oxidu polonium s HCl, HBr nebo HI.
Další sloučeniny polonia zahrnují polonit draselný jako polonit , polonát , acetát , bromičnan , uhličitan , citrát , chromát , kyanid, mravenčan , (II) a (IV) hydroxidy, dusičnan , selenát , selenit , monosulfid, síran , disulfát a siřičitan .
Omezený organopolonium chemie je známo, většinou omezeny na dialkyl a diaryl polonides (R 2 PO), triarylpolonium halogenidy (Ar 3 neštovice), a diarylpolonium dihalogenidy (Ar 2 Pox 2 ). Polonium také tvoří rozpustné sloučeniny s některými chelatačními činidly , jako je 2,3-butandiol a thiomočovina .
| Vzorec | Barva | teplota tání (° C) |
Sublimační teplota (° C) |
Symetrie | Pearsonův symbol | Vesmírná skupina | Ne | a (odpoledne) | b (odp.) | c (odp.) | Z | ρ (g/cm 3 ) | čj |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Hovínko | Černá | ||||||||||||
| PoO 2 | světle žlutá | 500 (pros.) | 885 | fcc | cF12 | Fm 3 m | 225 | 563,7 | 563,7 | 563,7 | 4 | 8,94 | |
| PoH 2 | -35,5 | ||||||||||||
| PoCl 2 | tmavě rubínově červená | 355 | 130 | ortorombický | oP3 | Pmmm | 47 | 367 | 435 | 450 | 1 | 6,47 | |
| PoBr 2 | purpurově hnědá | 270 (prosinec) | |||||||||||
| PoCl 4 | žlutá | 300 | 200 | monoklinický | |||||||||
| PoBr 4 | Červené | 330 (prosinec) | fcc | cF100 | Fm 3 m | 225 | 560 | 560 | 560 | 4 | |||
| PoI 4 | Černá |
|
Oxidy |
Hydridy |
|
Izotopy
Polonium má 42 známých izotopů, z nichž všechny jsou radioaktivní . Mají atomovou hmotnost, která se pohybuje od 186 do 227 u . 210 Po (poločas rozpadu 138,376 dní) je nejrozšířenější a je získáván pomocí zachycování neutronů přirozeným bizmutem . Delší životnost 209 Po (poločas rozpadu125,2 ± 3,3 roku, nejdelší životnost ze všech izotopů polonia) a 208 Po (poločas rozpadu 2,9 roku) lze provést pomocí alfa, protonového nebo deuteronového bombardování olova nebo vizmutu v cyklotronu .
Dějiny
Předběžně nazvaný „ radium F “, polonium objevili Marie a Pierre Curie v červenci 1898 a bylo pojmenováno podle rodné země Marie Curie v Polsku ( latinsky : Polonia ). Polsko v té době bylo pod ruskou , německou a rakousko-uherskou divizí a neexistovalo jako nezávislá země. Curie doufala, že pojmenování živlu po její rodné zemi bude propagovat jeho nedostatek nezávislosti. Polonium může být prvním prvkem pojmenovaným pro zvýraznění politické kontroverze.
Tento prvek byl prvním, který Curie objevili, když zkoumali příčinu radioaktivity smolné směsi . Pitchblende, po odstranění radioaktivních prvků uranu a thoria , byl radioaktivnější než uran a thorium dohromady. To přimělo Curie hledat další radioaktivní prvky. Poprvé oddělili polonium od smolince v červenci 1898 a o pět měsíců později také izolovali radium . Německý vědec Willy Marckwald úspěšně izoloval 3 miligramy polonia v roce 1902, ačkoli v té době věřil, že jde o nový prvek, který nazval „radio-telur“, a teprve v roce 1905 se ukázalo, že je stejný jako polonium .
Ve Spojených státech, polonium byl vyroben jako součást Projektu Manhattan ‚s Dayton projektu během druhé světové války . Polonium a berylium byly klíčovými složkami iniciátoru ' Urchin ' ve středu sférické jámy bomby . „Urchin“ zahájil jadernou řetězovou reakci v okamžiku okamžité kritičnosti, aby zajistil, že zbraň nevyprskne . „Urchin“ byl použit v raných amerických zbraních; následující americké zbraně používaly ke stejnému účelu pulzní neutronový generátor.
Velká část základní fyziky polonia byla klasifikována až po válce. Skutečnost, že byl použit jako iniciátor, byla klasifikována až do 60. let minulého století.
Komise pro atomovou energii a projekt Manhattan financovaly lidské experimenty s použitím polonia na pěti lidech na univerzitě v Rochesteru v letech 1943 až 1947. Lidem bylo podáno 9 až 22 mikrocuries (330 a 810 kBq ) polonia za účelem studia jeho vylučování .
Výskyt a produkce
Polonium je v přírodě velmi vzácný prvek kvůli krátkým poločasům rozpadu všech jeho izotopů. Sedm izotopy se vyskytují v stopy jako produkty rozpadu : 210 Po, 214 Po, a 218 Po vyskytují v rozpadovém řetězci o 238 U ; 211 Po a 215 Po se vyskytují v rozpadovém řetězci 235 U ; 212 Po a 216 Po se vyskytují v rozpadovém řetězci 232 Th . Z nich je 210 Po jediným izotopem s poločasem delším než 3 minuty.
Polonium lze v uranových rudách nalézt v množství přibližně 0,1 mg na metrickou tunu (1 díl z 10 10 ), což je přibližně 0,2% množství radia. Množství v zemské kůře není škodlivé. Polonium bylo nalezeno v tabákovém kouři z tabákových listů pěstovaných s fosfátovými hnojivy.
Protože je přítomna v malých koncentracích, je izolace polonia z přírodních zdrojů únavný proces. Největší šarže prvku, která kdy byla extrahována, provedená v první polovině 20. století, obsahovala pouze 40 Ci (1,5 TBq) (9 mg) polonia-210 a byla získána zpracováním 37 tun zbytků z produkce radia. Polonium se nyní obvykle získává ozařováním vizmutu vysoce energetickými neutrony nebo protony.
V roce 1934 experiment ukázal, že když je přírodní 209 Bi bombardováno neutrony , vytvoří se 210 Bi, které se pak rozpadne na 210 Po pomocí beta-minus rozpadu. Konečné čištění se provádí pyrochemicky a následují extrakční metody kapalina-kapalina. Polonium lze nyní vyrábět v miligramových množstvích tímto postupem, který využívá vysoké neutronové toky nalezené v jaderných reaktorech . Ročně se vyrobí jen asi 100 gramů, prakticky všechno v Rusku, takže polonium je mimořádně vzácné.
Tento proces může způsobit problémy v olova, bismutu na bázi tekutého kovu chlazený jaderných reaktorů , jako jsou ty používané v sovětské námořnictvo ‚s K-27 . V těchto reaktorech musí být přijata opatření, která zabrání nechtěné možnosti uvolnění 210 Po z chladicí kapaliny.
Izotopy polonia s delší životností, 208 Po a 209 Po, mohou být vytvořeny protonovým nebo deuteronovým bombardováním vizmutu pomocí cyklotronu . Ozařováním platiny uhlíkovými jádry lze vytvořit další neutronově deficitnější a nestabilnější izotopy .
Aplikace
V bývalém Sovětském svazu byly vyráběny zdroje alfa částic na bázi polonia . Tyto zdroje byly použity pro měření tloušťky průmyslových povlaků prostřednictvím zeslabení záření alfa.
Kvůli intenzivnímu záření alfa se jeden gram vzorku 210 Po spontánně zahřeje na teplotu vyšší než 500 ° C (932 ° F) a vytvoří asi 140 wattů energie. Proto je 210 Po používán jako atomový zdroj tepla k napájení radioizotopových termoelektrických generátorů prostřednictvím termoelektrických materiálů. Například v Měsíčních roverech Lunokhod 1 (1970) a Lunokhod 2 (1973) bylo použito 210 Po tepelných zdrojů, aby jejich vnitřní součásti byly během lunárních nocí v teple, stejně jako satelity Kosmos 84 a 90 (1965).
Částice alfa emitované poloniem lze převést na neutrony pomocí oxidu berylnatého rychlostí 93 neutronů na milion částic alfa. Tak Po-BeO směsi nebo slitiny se používají jako zdroj neutronů , například, v neutronové spoušť nebo iniciátor pro jaderných zbraní a pro kontroly ropných vrtech. V Sovětském svazu bylo ročně použito asi 1500 zdrojů tohoto typu s individuální aktivitou 1850 Ci (68 TBq).
Polonium bylo také součástí štětců nebo složitějších nástrojů, které před nanášením povlaků eliminovaly statické náboje ve fotografických deskách, textilních továrnách, papírových rolích, plastových fóliích a na substrátech (například v automobilovém průmyslu). Částice alfa emitované poloniem ionizují molekuly vzduchu, které neutralizují náboje na blízkých površích. Některé antistatické kartáče obsahují až 500 mikrocuri (20 MBq) 210 Po jako zdroj nabitých částic pro neutralizaci statické elektřiny. V USA lze zařízení s nejvýše 500 μCi (19 MBq) (zapečetěných) 210 Po na jednotku zakoupit v libovolném množství pod „obecnou licencí“, což znamená, že kupujícího nemusí registrovat žádné úřady. Polonium je potřeba v těchto zařízeních téměř každý rok vyměnit, protože má krátký poločas; je také vysoce radioaktivní, a proto byl většinou nahrazen méně nebezpečnými zdroji beta částic .
V laboratoři a pro účely výuky se někdy používá malé množství 210 Po nebo polymerní matrice - jsou často osvobozeny od licencování ze strany NRC a podobných úřadů, protože nejsou považovány za nebezpečné. Malá množství 210 Po jsou vyráběna k prodeji veřejnosti ve Spojených státech jako „jehlové zdroje“ pro laboratorní experimenty a jsou v maloobchodě vědeckými dodavatelskými společnostmi. Polonium je vrstva pokovování, která je zase pokovena materiálem, jako je zlato, který umožňuje průchod záření alfa (používá se v experimentech, jako jsou oblačné komory) a zároveň zabraňuje uvolňování polonia a představuje toxické nebezpečí. Podle United Nuclear obvykle prodávají čtyři až osm takových zdrojů ročně.
Poloniové zapalovací svíčky byly prodávány firmou Firestone v letech 1940 až 1953. Zatímco množství radiace ze zátek bylo nepatrné a neohrožovalo spotřebitele, výhody těchto svíček se přibližně po měsíci rychle snížily kvůli krátkému poločasu polonia a proto, že nahromadění na vodičích by blokovalo záření, které zlepšovalo výkon motoru. (Předpokladem zapalovací svíčky polonium, stejně jako prototypové radiové zástrčky Alfreda Matthewa Hubbarda, která jí předcházela, bylo, že záření zlepší ionizaci paliva ve válci a umožní tak motoru rychleji a efektivněji střílet.)
Biologie a toxicita
Přehled
Polonium může být nebezpečné a nemá žádnou biologickou roli. Hmotnostně je polonium-210 přibližně 250 000krát toxičtější než kyanovodík ( LD 50 pro 210 Po je pro průměrného dospělého člověka menší než 1 mikrogram (viz níže) ve srovnání s přibližně 250 miligramy pro kyanovodík). Hlavním nebezpečím je jeho intenzivní radioaktivita (jako alfa zářič), což ztěžuje bezpečnou manipulaci. I v množství mikrogramů je manipulace s 210 Po extrémně nebezpečná, vyžaduje speciální vybavení (podtlakový box na rukavice s vysokým tlakem vybavený vysoce výkonnými filtry), adekvátní monitorování a přísné manipulační postupy, aby se zabránilo kontaminaci. Částice alfa emitované poloniem snadno poškodí organickou tkáň, pokud je polonium požito, vdechnuto nebo absorbováno, přestože nepronikají do pokožky, a proto nejsou nebezpečné, pokud částice alfa zůstávají mimo tělo. Povinným opatřením k zamezení transkutánní difúze polonia přímo přes kůži je nošení chemicky odolných a neporušených rukavic . Polonium dodávané v koncentrované kyselině dusičné může snadno difundovat neadekvátními rukavicemi (např. Latexovými rukavicemi ) nebo kyselina může rukavice poškodit.
Polonium nemá toxické chemické vlastnosti.
Bylo oznámeno, že někteří mikrobi mohou methylovat polonium působením methylkobalaminu . To je podobné způsobu, jakým jsou rtuť , selen a telur metylovány v živých organismech za vzniku organokovových sloučenin. Studie zkoumající metabolismus polonia-210 u potkanů ukázaly, že pouze 0,002 až 0,009% požitého polonia-210 je vyloučeno jako těkavé polonium-210.
Akutní účinky
Střední letální dávka (LD 50 ) pro expozici akutní záření je asi 4,5 Sv . Úvazek efektivní dávka ekvivalentní 210 Po je 0,51 μSv / Bq požití, a 2,5 μSv / Bq při vdechování. Smrtelná dávka 4,5 Sv může být způsobena požitím 8,8 MBq (240 μCi), přibližně 50 nanogramů (ng) nebo vdechnutím 1,8 MBq (49 μCi), přibližně 10 ng. Jeden gram 210 Po by tak teoreticky mohl otrávit 20 milionů lidí, z nichž 10 milionů by zemřelo. Skutečná toxicita 210 Po je nižší než tyto odhady, protože radiační zátěž rozložená na několik týdnů ( biologický poločas polonia u lidí je 30 až 50 dní) je o něco méně škodlivá než okamžitá dávka. Odhaduje se, že střední letální dávka z 210 Po 15 megabecquerelů (0,41 mCi), nebo 0,089 mikrogramů (ug), stále ještě velmi malé množství. Pro srovnání, jedno zrnko kuchyňské soli je asi 0,06 mg = 60 μg.
Dlouhodobé (chronické) účinky
Kromě akutních účinků přináší ozáření (vnitřní i vnější) dlouhodobé riziko úmrtí na rakovinu 5–10% na Sv. Obecná populace je vystavena malému množství polonia jako radonové dcery ve vnitřním vzduchu; předpokládá se, že izotopy 214 Po a 218 Po způsobují každoročně většinu odhadovaných 15 000–22 000 úmrtí na rakovinu plic v USA, které byly přičítány radonu v interiéru. Kouření tabáku způsobuje další expozici polonia.
Regulační limity expozice a manipulace
Maximální přípustná tělesná zátěž pro požitých 210 Po je pouze 1,1 kBq (30 nCi), což je ekvivalent částic o hmotnosti pouze 6,8 pikogramů. Maximální přípustná koncentrace na pracovišti ve vzduchu 210 Po je asi 10 Bq/m 3 (3 × 10 −10 µCi/cm 3 ). Cílovými orgány pro polonium u lidí jsou slezina a játra . Vzhledem k tomu, že slezina (150 g) a játra (1,3 až 3 kg) jsou mnohem menší než zbytek těla, je -li polonium koncentrováno v těchto životně důležitých orgánech, představuje větší ohrožení života než dávka, která by byla utrpěna. (v průměru) celým tělem, pokud by bylo rovnoměrně rozloženo po celém těle, stejným způsobem jako cesium nebo tritium (jako T 2 O).
210 Po je široce používán v průmyslu a je snadno dostupný s malou regulací nebo omezením. V USA byl v roce 2007 implementován sledovací systém, který provozuje Nuclear Regulatory Commission, za účelem registrace nákupů více než 16 curies (590 GBq) polonia-210 (dost na vytvoření 5 000 smrtelných dávek). MAAE „prý zvažuje zpřísnění předpisů ... Mluví se o tom, že by to mohlo zpřísnit požadavek na hlášení polonia o faktor 10, na 1,6 curie (59 GBq)“. Od roku 2013 je to stále jediný dostupný alfa produkt emitující vedlejší produkty jako osvobozené množství NRC, který může být držen bez licence na radioaktivní materiál.
S poloniem a jeho sloučeninami je třeba zacházet v odkládací přihrádce , která je dále uzavřena v jiném boxu, udržovaném při mírně vyšším tlaku než v odkládací přihrádce, aby se zabránilo úniku radioaktivních materiálů. Rukavice z přírodního kaučuku neposkytují dostatečnou ochranu před zářením z polonia; jsou nutné chirurgické rukavice. Neoprenové rukavice chrání záření z polonia lépe než přírodní kaučuk.
Případy otravy
Navzdory vysoce nebezpečným vlastnostem prvku jsou okolnosti, za nichž může dojít k otravě poloniem, vzácné. Jeho extrémní nedostatek v přírodě, krátké poločasy rozpadu všech jeho izotopů, specializovaná zařízení a vybavení potřebné k získání jakéhokoli významného množství a bezpečnostní opatření proti laboratorním nehodám způsobují, že škodlivé expozice jsou nepravděpodobné. Jako taková byla potvrzena pouze hrstka případů radiační otravy specificky způsobené expozicí polonia.
20. století
V reakci na obavy z rizik expozice pracovního polonia byla v letech 1944 až 1947 podána pěti lidským dobrovolníkům na univerzitě v Rochesteru množství 210 Po, aby se studovalo její biologické chování. Tyto studie byly financovány z projektu Manhattan a AEC. Zúčastnili se čtyři muži a žena, všichni trpěli rakovinou v terminálním stadiu, a pohybovali se ve věku od třicítky do začátku čtyřicítky; všichni byli vybráni, protože experimentátoři chtěli subjekty, které nebyly vystaveny poloniu ani při práci, ani při úrazu. 210 Po bylo injekčně podáno čtyřem hospitalizovaným pacientům a orálně byl podán pětině. Žádná z podaných dávek (všechny v rozmezí 0,17-0,30 μ Ci kg -1 ) se nepřiblížila smrtelným množstvím.
K první zdokumentované smrti přímo v důsledku otravy poloniem došlo v Sovětském svazu dne 10. července 1954. Neidentifikovaný 41letý muž byl předložen k lékařskému ošetření 29. června s těžkým zvracením a horečkou; předchozího dne pracoval pět hodin v oblasti, ve které, aniž by to tehdy věděl, kapsle obsahující 210 Po odtlakovala a začala se rozptylovat ve formě aerosolu. V průběhu tohoto období, jeho celkový příjem polétavého 210 Pádu byla odhadnuta na zhruba 0,11 GBq (téměř 25krát odhadované LD 50 inhalací 4,5 MBq). Navzdory léčbě se jeho stav stále zhoršoval a smrt nastala 13 dní po expozici.
Rovněž bylo navrženo, že smrt Irene Joliot-Curie v roce 1956 na leukémii byla způsobena radiačními účinky polonia. Byla náhodně odhalena v roce 1946, když na její laboratorní lavici explodovala zapečetěná kapsle prvku.
Rovněž bylo údajně několik úmrtí v Izraeli v letech 1957–1969 způsobeno expozicí 210 Po. V laboratoři Weizmannova institutu byl v roce 1957 objeven únik . Stopy 210 Po byly nalezeny na rukou profesora Drora Sadeha, fyzika, který zkoumal radioaktivní materiály. Lékařské testy neukázaly žádné poškození, ale testy nezahrnovaly kostní dřeň. Sadeh, jeden z jeho studentů, a dva kolegové zemřeli v následujících letech na různé druhy rakoviny . Problém byl vyšetřován tajně, ale nikdy nebylo formálně přiznáno spojení mezi únikem a smrtí.
21. století
Příčinou úmrtí 2006 o Alexandra Litviněnka , bývalého Ruská FSB agent, který přeběhl do Spojeného království v roce 2001, bylo zjištěno, které mají být otrava s letální dávkou 210 Po; následně bylo zjištěno, že 210 Po mu pravděpodobně záměrně podali dva ruští bývalí bezpečnostní agenti Andrey Lugovoy a Dmitrij Kovtun . Litviněnkova smrt jako taková byla prvním (a dosud jediným) potvrzeným případem, kdy byla extrémní toxicita polonia použita se zlovolným úmyslem.
V roce 2011 se objevilo obvinění, že smrt palestinského vůdce Jásira Arafata , který zemřel 11. listopadu 2004 na nejisté příčiny, byla také důsledkem úmyslné otravy poloniem a v červenci 2012 byly v Arafatových šatech a osobním oblečení zjištěny abnormálně vysoké koncentrace 210 Po věci Institut de Radiophysique v Lausanne, Švýcarsko . Mluvčí Institutu však zdůraznil, že navzdory těmto testům nebyly Arafatovy lékařské zprávy v souladu s otravou 210 Po a vědecká novinářka Deborah Blum navrhla, že za to mohl spíše tabákový kouř, protože jak Arafat, tak mnoho jeho kolegů byli silní kuřáci; následné testy francouzských i ruských týmů určily, že zvýšené hladiny 210 Po nebyly výsledkem úmyslné otravy a nezpůsobily Arafatovu smrt.
Léčba
Bylo navrženo, že k dekontaminaci lidí lze použít chelatační činidla , jako je britský anti-Lewisit ( dimerkaprol ). V jednom experimentu byla krysám podána smrtelná dávka 1,45 MBq/kg (8,7 ng/kg) 210 Po; všechny neošetřené krysy byly mrtvé po 44 dnech, ale 90% krys ošetřených chelatačním činidlem HOEtTTC zůstalo naživu po dobu 5 měsíců.
Detekce v biologických vzorcích
Polonium-210 lze kvantifikovat v biologických vzorcích spektrometrií alfa částic k potvrzení diagnózy otravy u hospitalizovaných pacientů nebo k poskytnutí důkazů při vyšetřování medikolegální smrti. Výchozí vylučování polonia-210 močí u zdravých osob v důsledku rutinní expozice environmentálním zdrojům je normálně v rozmezí 5–15 mBq/den. Úrovně přesahující 30 mBq/den naznačují nadměrné vystavení radionuklidu.
Výskyt u lidí a biosféry
Polonium-210 je díky své poloze v řetězci rozpadu uranu-238 rozšířeno v biosféře , včetně lidských tkání . Přírodní uran-238 v zemské kůře se rozpadá řadou pevných radioaktivních meziproduktů včetně radia-226 na radioaktivní vzácný plyn radon-222 , z nichž některé během svého 3,8denního poločasu difundují do atmosféry. Tam se rozpadá několika dalšími kroky na polonium-210, z nichž velká část je během svého 138denního poločasu odplavena zpět na zemský povrch, čímž se dostává do biosféry, než se nakonec rozpadne na stabilní olovo-206 .
Již ve dvacátých letech dvacátého století francouzský biolog Antoine Lacassagne pomocí polonia, které poskytla jeho kolegyně Marie Curie , ukázal, že prvek má specifický vzorec absorpce v králičích tkáních, s vysokými koncentracemi, zejména v játrech , ledvinách a varlatech . Novější důkazy naznačují, že toto chování vyplývá z polonia, které nahrazuje jeho kongenerovou síru, také ve skupině 16 periodické tabulky, v aminokyselinách obsahujících síru nebo příbuzných molekulách a že podobné vzorce distribuce se vyskytují v lidských tkáních. Polonium je vskutku prvek přirozeně přítomný u všech lidí, který významně přispívá k přirozené dávce pozadí, s širokými geografickými a kulturními odchylkami a zvláště vysokou úrovní například u obyvatel Arktidy.
Tabák
Polonium-210 v tabáku přispívá k mnoha případům rakoviny plic na celém světě. Většina tohoto polonia pochází z olova 210 uloženého na tabákových listech z atmosféry; olovo-210 je produkt radonu-222 , jehož velká část pochází z rozpadu radia-226 z hnojiv aplikovaných na tabákové půdy.
Přítomnost polonia v tabákovém kouři je známá od počátku 60. let minulého století. Některé z největších světových tabákových firem zkoumaly způsoby, jak tuto látku odstranit-bezvýsledně-po dobu 40 let. Výsledky nebyly nikdy zveřejněny.
Jídlo
Polonium se nachází v potravinovém řetězci, zejména v mořských plodech.
Viz také
Reference
Bibliografie
- Bagnall, KW (1962). „Chemie polonia“ . Pokroky v anorganické chemii a radiochemii . 4 . New York: Academic Press . s. 197–226. doi : 10,1016/S0065-2792 (08) 60268-X . ISBN 978-0-12-023604-6. Citováno 14. června 2012 .
- Greenwood, Norman N .; Earnshaw, Alan (1997). Chemistry of the Elements (2. vyd.). Butterworth – Heinemann. ISBN 978-0080379418.
externí odkazy
- Polonium v periodické tabulce videí (University of Nottingham)